2025年新中考集训测试评估卷九年级化学全一册鲁教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年新中考集训测试评估卷九年级化学全一册鲁教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第43页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
14. (2024·济宁期中)在反应 $2A + 3B = C + 2D$ 中,$C$、$D$ 的相对分子质量之比为 $7:8$,若 $3.6g\ A$ 与 $B$ 完全反应后,生成 $6.4g\ D$,则反应中 $B$ 和 $D$ 的质量比为(
A.$7:1$
B.$7:8$
C.$7:16$
D.$7:32$
B
)A.$7:1$
B.$7:8$
C.$7:16$
D.$7:32$
答案:
14.B 解析:在反应$2\mathrm{A} + 3\mathrm{B} = \mathrm{C} + 2\mathrm{D}$中,C、D的相对分子质量之比为$7:8$,$3.6\mathrm{g}$A与B完全反应后生成$6.4\mathrm{g}\mathrm{D}$;设C、D的相对分子质量分别为$7a$和$8a$,生成C的质量为x。
$2\mathrm{A} + 3\mathrm{B} = \mathrm{C} + 2\mathrm{D}$
$\frac{7a}{16a} = \frac{x}{6.4\mathrm{g}}$
$x = 2.8\mathrm{g}$。
由质量守恒定律可知,参加反应的B的质量为$2.8\mathrm{g} + 6.4\mathrm{g} - 3.6\mathrm{g} = 5.6\mathrm{g}$,则反应中B和D的质量比为$5.6\mathrm{g}:6.4\mathrm{g} = 7:8$。
$2\mathrm{A} + 3\mathrm{B} = \mathrm{C} + 2\mathrm{D}$
$\frac{7a}{16a} = \frac{x}{6.4\mathrm{g}}$
$x = 2.8\mathrm{g}$。
由质量守恒定律可知,参加反应的B的质量为$2.8\mathrm{g} + 6.4\mathrm{g} - 3.6\mathrm{g} = 5.6\mathrm{g}$,则反应中B和D的质量比为$5.6\mathrm{g}:6.4\mathrm{g} = 7:8$。
15. (8 分)请运用“守恒”
(1)若某物质受热分解生成 $CO_2$ 和 $H_2O$,则组成该物质的元素是
(2)将 $10g\ A$ 和 $15g\ B$ 混合加热充分反应,生成 $8g\ C$ 和 $4g\ D$,则剩余物质的质量为
(3)古代“银针验毒”的原理是 $4Ag + 2H_2S + O_2 = 2X + 2H_2O$,根据
的
思想回答下列问题。(1)若某物质受热分解生成 $CO_2$ 和 $H_2O$,则组成该物质的元素是
C、O、H
。(2)将 $10g\ A$ 和 $15g\ B$ 混合加热充分反应,生成 $8g\ C$ 和 $4g\ D$,则剩余物质的质量为
13
g。(3)古代“银针验毒”的原理是 $4Ag + 2H_2S + O_2 = 2X + 2H_2O$,根据
质量守恒定律
,推出 $X$ 的化学式为Ag2S
。
答案:
15.
(1)$\mathrm{C}$、$\mathrm{O}$、$\mathrm{H}$
(2)13
(3)质量守恒定律 $\mathrm{Ag_2S}$
解析:
(1)根据质量守恒定律,化学反应前后元素种类不变,若某物质受热分解生成$\mathrm{CO_2}$和$\mathrm{H_2O}$,则该物质中一定含有碳、氢、氧元素。
(2)剩余物质的质量$= 10\mathrm{g} + 15\mathrm{g} - 8\mathrm{g} - 4\mathrm{g} = 13\mathrm{g}$。
(3)根据质量守恒定律,在反应前后各元素原子的个数不变,从$4\mathrm{Ag} + 2\mathrm{H_2S} + \mathrm{O_2} = 2\mathrm{X} + 2\mathrm{H_2O}$,推出X的化学式为$\mathrm{Ag_2S}$。
(1)$\mathrm{C}$、$\mathrm{O}$、$\mathrm{H}$
(2)13
(3)质量守恒定律 $\mathrm{Ag_2S}$
解析:
(1)根据质量守恒定律,化学反应前后元素种类不变,若某物质受热分解生成$\mathrm{CO_2}$和$\mathrm{H_2O}$,则该物质中一定含有碳、氢、氧元素。
(2)剩余物质的质量$= 10\mathrm{g} + 15\mathrm{g} - 8\mathrm{g} - 4\mathrm{g} = 13\mathrm{g}$。
(3)根据质量守恒定律,在反应前后各元素原子的个数不变,从$4\mathrm{Ag} + 2\mathrm{H_2S} + \mathrm{O_2} = 2\mathrm{X} + 2\mathrm{H_2O}$,推出X的化学式为$\mathrm{Ag_2S}$。
16. (8 分)依据下列要求,写出有关化学反应的化学方程式。
(1)有黑色固体生成的化合反应:
(2)紫红色金属在空气中加热:
(3)商店里出售的打火机里装的不是汽油,而是液体丁烷$(C_4H_{10})$,丁烷在空气中完全燃烧后生成二氧化碳和水蒸气,写出丁烷完全燃烧的化学方程式:
(4)一种独特的锂氮电池可以为新能源汽车提供动力,该电池的主要反应原理是金属锂和空气中的氮气在常温下反应生成氮化锂($Li$ 为 $+1$ 价),写出该反应的化学方程式:
(1)有黑色固体生成的化合反应:
3Fe + 2O2 =点燃= Fe3O4
。(2)紫红色金属在空气中加热:
2Cu + O2 =△= 2CuO
。(3)商店里出售的打火机里装的不是汽油,而是液体丁烷$(C_4H_{10})$,丁烷在空气中完全燃烧后生成二氧化碳和水蒸气,写出丁烷完全燃烧的化学方程式:
2C4H10 + 13O2 =点燃= 8CO2 + 10H2O
。(4)一种独特的锂氮电池可以为新能源汽车提供动力,该电池的主要反应原理是金属锂和空气中的氮气在常温下反应生成氮化锂($Li$ 为 $+1$ 价),写出该反应的化学方程式:
6Li + N2 = 2Li3N
。
答案:
16.
(1)$3\mathrm{Fe} + 2\mathrm{O_2}\stackrel{点燃}{=}\mathrm{Fe_3O_4}$
(2)$2\mathrm{Cu} + \mathrm{O_2}\stackrel{\triangle}{=}2\mathrm{CuO}$
(3)$2\mathrm{C_4H_{10}} + 13\mathrm{O_2}\stackrel{点燃}{=}8\mathrm{CO_2} + 10\mathrm{H_2O}$
(4)$6\mathrm{Li} + \mathrm{N_2} = 2\mathrm{Li_3N}$
(1)$3\mathrm{Fe} + 2\mathrm{O_2}\stackrel{点燃}{=}\mathrm{Fe_3O_4}$
(2)$2\mathrm{Cu} + \mathrm{O_2}\stackrel{\triangle}{=}2\mathrm{CuO}$
(3)$2\mathrm{C_4H_{10}} + 13\mathrm{O_2}\stackrel{点燃}{=}8\mathrm{CO_2} + 10\mathrm{H_2O}$
(4)$6\mathrm{Li} + \mathrm{N_2} = 2\mathrm{Li_3N}$
17. (12 分)从宏观、微观、符号相结合的视角探究物质及其变化规律是化学独特的研究方法。根据所给信息,回答下列问题:
宏观辨识
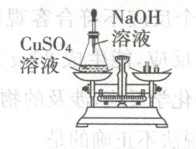
(1)通过科学探究可以认识化学反应中各物质质量之间的关系,如下图实验中,将 $NaOH$ 溶液滴入锥形瓶中,反应结束后,再次称量,观察到托盘天平的指针
微观探析
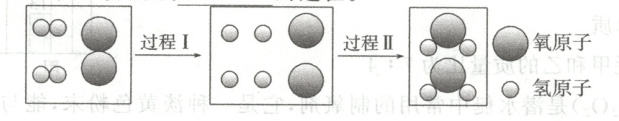
(2)下图是氢气在空气中燃烧的微观示意图,反应的基本反应类型为
符号表征
(3)氢化镁$(MgH_2)$是一种很有发展前景的贮氢材料,能与水反应生成氢氧化镁和一种常见的气体,反应的化学方程式为 $MgH_2 + 2H_2O = Mg(OH)_2 +$
依据一:化学反应前后原子的种类和
依据二:
宏观辨识
(1)通过科学探究可以认识化学反应中各物质质量之间的关系,如下图实验中,将 $NaOH$ 溶液滴入锥形瓶中,反应结束后,再次称量,观察到托盘天平的指针
不
(填“向左”“向右”或“不”)偏转。
微观探析
(2)下图是氢气在空气中燃烧的微观示意图,反应的基本反应类型为
化合
反应。从微观角度分析,过程Ⅰ表示分子分解成原子
的过程。
符号表征
(3)氢化镁$(MgH_2)$是一种很有发展前景的贮氢材料,能与水反应生成氢氧化镁和一种常见的气体,反应的化学方程式为 $MgH_2 + 2H_2O = Mg(OH)_2 +$
2H2
$\uparrow$。请补全反应的化学方程式并写出补全依据。依据一:化学反应前后原子的种类和
数目
不变。依据二:
每个氢分子由2个氢原子构成
。
答案:
17.
(1)不
(2)化合 原子
(3)$2\mathrm{H_2}$ 数目 每个氢分子由2个氢原子构成
解析:
(1)氢氧化钠和硫酸铜反应生成氢氧化铜沉淀和硫酸钠,根据质量守恒定律,化学反应前后,物质的总质量不变,反应结束后,再次称量,观察到托盘天平的指针不偏转。
(2)由题图可知,反应是氢气和氧气在点燃的条件下反应生成水,符合“多变一”的特点,属于化合反应;过程Ⅰ中氢分子分为氢原子,氧分子分为氧原子,是分子分解成原子的过程。
(3)根据质量守恒定律,化学反应前后,原子的种类和数目不变,反应物中含$\mathrm{Mg}$、$\mathrm{H}$、$\mathrm{O}$的个数分别是1、6、2,生成物中含$\mathrm{Mg}$、$\mathrm{H}$、$\mathrm{O}$的个数分别是1、2、2,生成物中还应含4个$\mathrm{H}$,每个氢分子由2个氢原子构成,应补充$2\mathrm{H_2}$;由以上分析可知,依据一:化学反应前后,原子的种类和数目不变;依据二:每个氢分子由2个氢原子构成。
(1)不
(2)化合 原子
(3)$2\mathrm{H_2}$ 数目 每个氢分子由2个氢原子构成
解析:
(1)氢氧化钠和硫酸铜反应生成氢氧化铜沉淀和硫酸钠,根据质量守恒定律,化学反应前后,物质的总质量不变,反应结束后,再次称量,观察到托盘天平的指针不偏转。
(2)由题图可知,反应是氢气和氧气在点燃的条件下反应生成水,符合“多变一”的特点,属于化合反应;过程Ⅰ中氢分子分为氢原子,氧分子分为氧原子,是分子分解成原子的过程。
(3)根据质量守恒定律,化学反应前后,原子的种类和数目不变,反应物中含$\mathrm{Mg}$、$\mathrm{H}$、$\mathrm{O}$的个数分别是1、6、2,生成物中含$\mathrm{Mg}$、$\mathrm{H}$、$\mathrm{O}$的个数分别是1、2、2,生成物中还应含4个$\mathrm{H}$,每个氢分子由2个氢原子构成,应补充$2\mathrm{H_2}$;由以上分析可知,依据一:化学反应前后,原子的种类和数目不变;依据二:每个氢分子由2个氢原子构成。
查看更多完整答案,请扫码查看


