第9页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
7. 向一定量硫酸铜溶液中逐滴加入氢氧化钠溶液,产生沉淀的质量与加入氢氧化钠溶液的质量关系如图所示。下列说法正确的是(
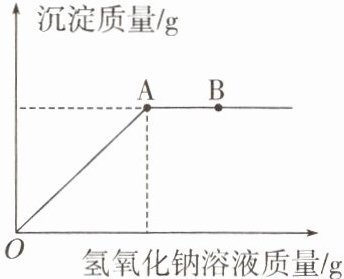
A.产生的沉淀为红褐色
B.A点时溶液中有两种溶质
C.B点时溶液 $ {pH}=7 $
D.A点到B点硫酸钠质量不变
D
)
A.产生的沉淀为红褐色
B.A点时溶液中有两种溶质
C.B点时溶液 $ {pH}=7 $
D.A点到B点硫酸钠质量不变
答案:
D
8. 石灰浆抹的墙壁上掉下一块白色固体,小科为探究其成分,进行了如下实验,由此所得出的结论中正确的是(
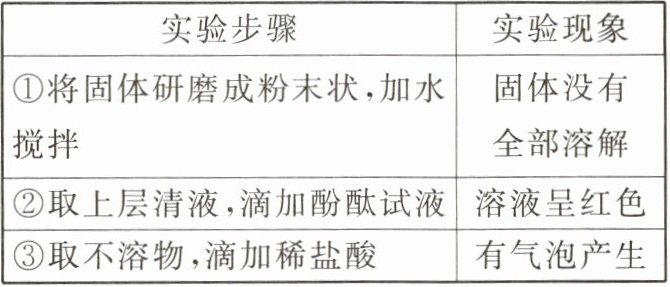
A.一定含有 $ {CaCO_{3}} $ 和 $ {Ca(OH)_{2}} $
B.一定含有 $ {Ca(OH)_{2}} $,可能含有 $ {CaCO_{3}} $
C.一定没有 $ {CaCO_{3}} $ 和 $ {Ca(OH)_{2}} $
D.一定含有 $ {CaCO_{3}} $,可能含有 $ {Ca(OH)_{2}} $
A
)
A.一定含有 $ {CaCO_{3}} $ 和 $ {Ca(OH)_{2}} $
B.一定含有 $ {Ca(OH)_{2}} $,可能含有 $ {CaCO_{3}} $
C.一定没有 $ {CaCO_{3}} $ 和 $ {Ca(OH)_{2}} $
D.一定含有 $ {CaCO_{3}} $,可能含有 $ {Ca(OH)_{2}} $
答案:
A
9. 氢氧化钙俗称熟石灰,在生产和生活中有广泛的用途。
(1)熟石灰可由生石灰溶于水制得,反应的化学方程式是
(2)用石灰浆粉刷墙壁,干燥后墙面变硬,反应的化学方程式是
(3)用熟石灰粉与草木灰(主要成分是 $ {K_{2}CO_{3}} $)按一定比例混合可制得高效环保农药“黑白粉”。“黑白粉”比熟石灰杀虫效果更好,是由于生成了碱性更强的 $ {KOH} $,反应的化学方程式是
(1)熟石灰可由生石灰溶于水制得,反应的化学方程式是
CaO+H₂O=Ca(OH)₂
;测量其溶液 $ {pH} $ 的操作是用洁净的玻璃棒蘸取少量待测液滴在干燥的pH试纸上
,再用标准比色卡比较试纸显示的颜色,读取该溶液的 $ {pH} $。(2)用石灰浆粉刷墙壁,干燥后墙面变硬,反应的化学方程式是
CO₂+Ca(OH)₂=CaCO₃↓+H₂O
。(3)用熟石灰粉与草木灰(主要成分是 $ {K_{2}CO_{3}} $)按一定比例混合可制得高效环保农药“黑白粉”。“黑白粉”比熟石灰杀虫效果更好,是由于生成了碱性更强的 $ {KOH} $,反应的化学方程式是
Ca(OH)₂+K₂CO₃=CaCO₃↓+2KOH
。
答案:
(1)CaO+H₂O=Ca(OH)₂ 用洁净的玻璃棒蘸取少量待测液滴在干燥的pH试纸上
(2)CO₂+Ca(OH)₂=CaCO₃↓+H₂O
(3)Ca(OH)₂+K₂CO₃=CaCO₃↓+2KOH
(1)CaO+H₂O=Ca(OH)₂ 用洁净的玻璃棒蘸取少量待测液滴在干燥的pH试纸上
(2)CO₂+Ca(OH)₂=CaCO₃↓+H₂O
(3)Ca(OH)₂+K₂CO₃=CaCO₃↓+2KOH
10. 小科学习了碱的性质后,将少量硫酸铜溶液滴入2毫升氢氧化钠溶液中,没有观察到预期的蓝色絮状沉淀,这是为什么呢?他进行如下探究实验。
【猜想】猜想一:氢氧化钠与硫酸铜反应放热,使氢氧化铜的溶解度增大;
猜想二:生成的氢氧化铜继续与氢氧化钠发生反应。
【实验】实验操作及现象如图所示:
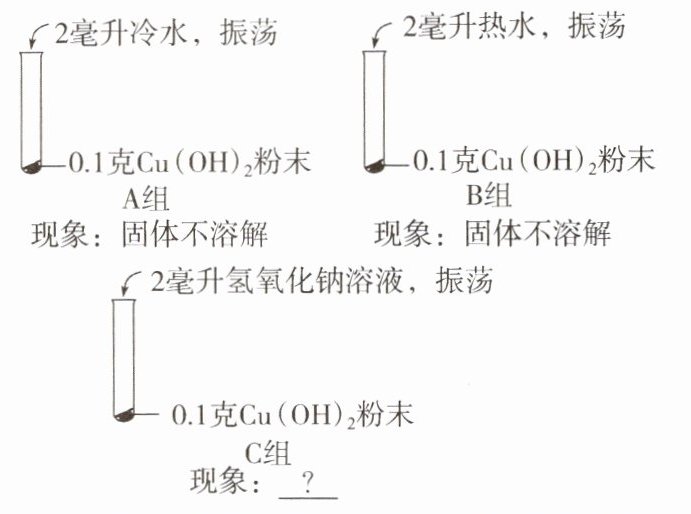
(1)为了验证猜想一,小科应选择
(2)若猜想二正确,则C中“?”处应填写的现象是
(3)查阅资料得知:氢氧化铜能与氢氧化钠溶液发生反应,生成可溶物。
【猜想】猜想一:氢氧化钠与硫酸铜反应放热,使氢氧化铜的溶解度增大;
猜想二:生成的氢氧化铜继续与氢氧化钠发生反应。
【实验】实验操作及现象如图所示:

(1)为了验证猜想一,小科应选择
A、B
两组实验进行对比。根据实验结果,猜想一不成立
(填“成立”或“不成立”)。(2)若猜想二正确,则C中“?”处应填写的现象是
固体消失
。(3)查阅资料得知:氢氧化铜能与氢氧化钠溶液发生反应,生成可溶物。
答案:
(1)A、B 不成立
(2)固体消失
(1)A、B 不成立
(2)固体消失
查看更多完整答案,请扫码查看


