第15页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
6. 小明发现盛有氢氧化钠溶液的试剂瓶瓶口周围有一些白色固体,他怀疑氢氧化钠溶液已经变质,于是进行了如下实验探究。
【提出问题】氢氧化钠溶液是否变质?
【作出猜想】
猜想①:该氢氧化钠溶液没有变质。
猜想②:该氢氧化钠溶液部分变质。
猜想③:该氢氧化钠溶液全部变质。
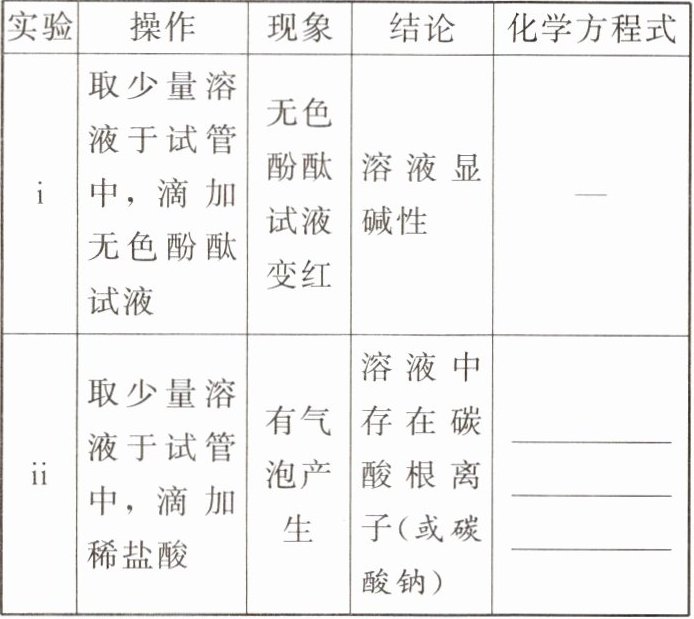
【实验验证】
【讨论】小明认为,根据上述实验i和ii可推断猜想②正确。而小张则认为猜想③也可能正确,理由是
(1)取原溶液少量于试管中,逐滴加入BaCl₂溶液至
(2)取(1)中上层清液少许于试管中,向其中加入CuSO₄溶液,若有蓝色沉淀产生,则说明氢氧化钠溶液部分变质,化学方程式为
【反思】该氢氧化钠溶液变质的原因可能是
【提出问题】氢氧化钠溶液是否变质?
【作出猜想】
猜想①:该氢氧化钠溶液没有变质。
猜想②:该氢氧化钠溶液部分变质。
猜想③:该氢氧化钠溶液全部变质。
【实验验证】
【讨论】小明认为,根据上述实验i和ii可推断猜想②正确。而小张则认为猜想③也可能正确,理由是
碳酸钠溶液呈碱性,也能使酚酞试液变红(合理即可)
。于是小张设计了如下补充实验:(1)取原溶液少量于试管中,逐滴加入BaCl₂溶液至
不再产生沉淀
,静置,分层。(2)取(1)中上层清液少许于试管中,向其中加入CuSO₄溶液,若有蓝色沉淀产生,则说明氢氧化钠溶液部分变质,化学方程式为
CuSO₄+2NaOH=Na₂SO₄+Cu(OH)₂↓
。若无蓝色沉淀产生,则说明氢氧化钠溶液已经全部变质。【反思】该氢氧化钠溶液变质的原因可能是
2NaOH+CO₂=Na₂CO₃+H₂O
(用化学方程式表示)。
答案:
6.【实验验证】Na₂CO₃+2HCl=2NaCl+H₂O+CO₂↑
【讨论】碳酸钠溶液呈碱性,也能使酚酞试液变红(合理即可)
(1)不再产生沉淀
(2)CuSO₄+2NaOH=Na₂SO₄+Cu(OH)₂↓
【反思】2NaOH+CO₂=Na₂CO₃+H₂O
【讨论】碳酸钠溶液呈碱性,也能使酚酞试液变红(合理即可)
(1)不再产生沉淀
(2)CuSO₄+2NaOH=Na₂SO₄+Cu(OH)₂↓
【反思】2NaOH+CO₂=Na₂CO₃+H₂O
7. 某实验小组做完实验得到甲、乙两种废液,共含有8种离子,分别为H⁺、K⁺、Ba²⁺、Ag⁺、OH⁻、Cl⁻、CO₃²⁻和NO₃⁻(不考虑H₂O解离出H⁺和OH⁻),且两种废液里所含的离子种数相同但种类不同,已知向甲废液里滴入紫色石蕊试液,溶液变成红色。
(1)甲废液呈
(2)若直接将甲废液排入铸铁管下水道,会造成的危害是
(1)甲废液呈
酸性
(填“酸性”“碱性”或“中性”),乙废液里含有的离子是K⁺、OH⁻、Cl⁻、CO₃²⁻
(填离子符号)。(2)若直接将甲废液排入铸铁管下水道,会造成的危害是
腐蚀下水道
。
答案:
7.(1)酸性 K⁺、OH⁻、Cl⁻、CO₃²⁻ (2)腐蚀下水道
8. 某溶液中可能含有Cl⁻、CO₃²⁻、SO₄²⁻、H⁺、Cu²⁺和Mg²⁺6种离子中的几种,小明通过以下实验进行了检验。
①取少量溶液于试管中,观察到溶液呈无色。再向试管中逐滴滴加氢氧化钠溶液,一开始无明显现象,一段时间后有白色沉淀生成。
②另取少量溶液于试管中,向其中滴加氯化钡溶液,无明显现象。
③再取少量溶液于试管中,滴加硝酸银溶液,产生白色沉淀,加稀硝酸后沉淀不溶解。
(1)原溶液中一定没有Cu²⁺的依据是
(2)通过上述实验现象可知,原溶液中一定大量存在的离子有
(3)有同学认为步骤③可以省略,理由是
①取少量溶液于试管中,观察到溶液呈无色。再向试管中逐滴滴加氢氧化钠溶液,一开始无明显现象,一段时间后有白色沉淀生成。
②另取少量溶液于试管中,向其中滴加氯化钡溶液,无明显现象。
③再取少量溶液于试管中,滴加硝酸银溶液,产生白色沉淀,加稀硝酸后沉淀不溶解。
(1)原溶液中一定没有Cu²⁺的依据是
溶液呈无色
。(2)通过上述实验现象可知,原溶液中一定大量存在的离子有
H⁺、Mg²⁺、Cl⁻
。(3)有同学认为步骤③可以省略,理由是
溶液不显电性,溶液中既有阴离子又有阳离子,步骤②向废液中加入BaCl₂溶液无明显现象,说明溶液中一定没有SO₄²⁻和CO₃²⁻,故溶液中一定含有Cl⁻
。
答案:
8.(1)溶液呈无色 (2)H⁺、Mg²⁺、Cl⁻
(3)溶液不显电性,溶液中既有阴离子又有阳离子,步骤②向废液中加入BaCl₂溶液无明显现象,说明溶液中一定没有SO₄²⁻和CO₃²⁻,故溶液中一定含有Cl⁻
(3)溶液不显电性,溶液中既有阴离子又有阳离子,步骤②向废液中加入BaCl₂溶液无明显现象,说明溶液中一定没有SO₄²⁻和CO₃²⁻,故溶液中一定含有Cl⁻
查看更多完整答案,请扫码查看


