第19页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
6. 向一定质量的稀硫酸中不断加入铁粉,下列有关图像表示不正确的是(
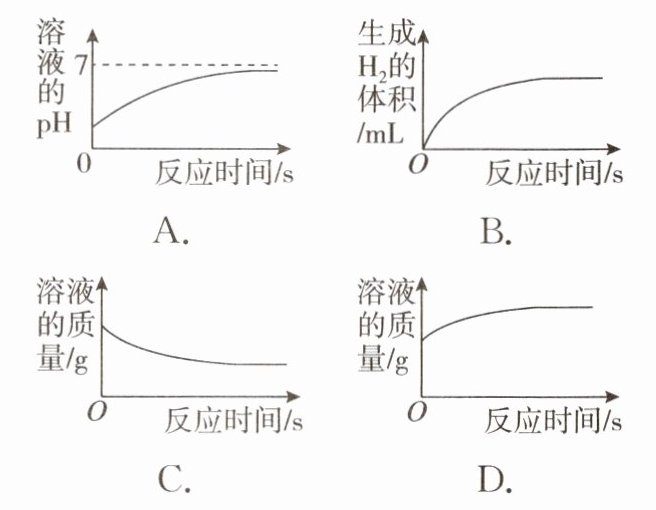
C
)
答案:
6. C
7. 下列各组化合物能用对应金属与同一种酸反应制取的是(
A.CuCl₂、AlCl₃
B.ZnCl₂、MgCl₂
C.Fe₂(SO₄)₃、FeSO₄
D.NaCl、K₂SO₄
B
)A.CuCl₂、AlCl₃
B.ZnCl₂、MgCl₂
C.Fe₂(SO₄)₃、FeSO₄
D.NaCl、K₂SO₄
答案:
7. B
8. 一包质量为6g的铁粉,可能含有某种杂质,与足量盐酸反应生成0.2g氢气,金属无剩余,则铁粉中含有的杂质为(
A.Cu
B.Zn
C.Al
D.Mg
B
)A.Cu
B.Zn
C.Al
D.Mg
答案:
8. B
9. 同学们在练习“金属的化学性质”实验操作时,发现几支试管中气泡产生的速度有快有慢,于是进行如下探究。
【提出问题】金属与酸反应的快慢受哪些因素影响呢?
【提出猜想】猜想一:可能与酸的浓度有关;
猜想二:可能与金属的种类有关;
猜想三:可能与金属的形状有关。
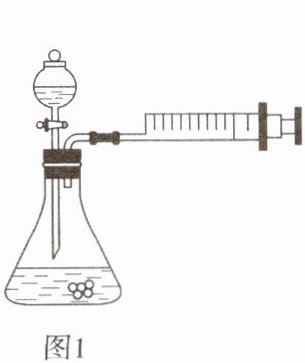
【设计并进行实验】用图1所示的装置进行四组实验。
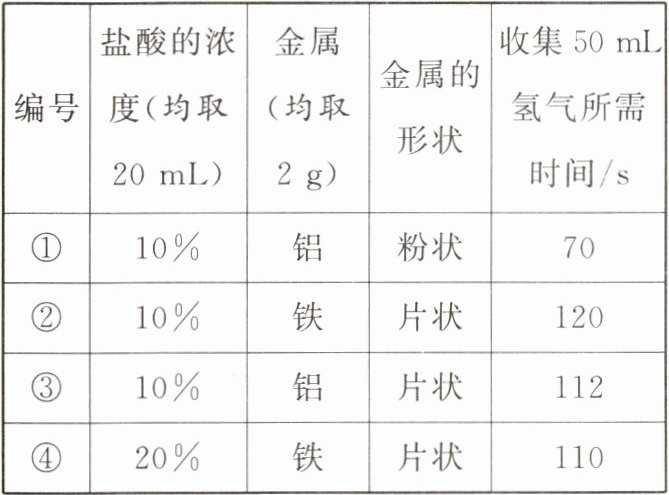
(1)检查图1装置气密性的方法:关闭分液漏斗活塞,将注射器活塞向右拉动一段距离,松手后,若观察到
(2)要比较金属的形状对反应快慢的影响,应选择的实验编号是
(3)实验①中试管外壁发烫,说明铝与盐酸的反应是放热反应,实验测得该反应中产生气体的反应速度与反应时间的关系如图2所示,你认为在t₂~t₃时间段内反应速度逐渐减小的主要原因是

【提出问题】金属与酸反应的快慢受哪些因素影响呢?
【提出猜想】猜想一:可能与酸的浓度有关;
猜想二:可能与金属的种类有关;
猜想三:可能与金属的形状有关。
【设计并进行实验】用图1所示的装置进行四组实验。

(1)检查图1装置气密性的方法:关闭分液漏斗活塞,将注射器活塞向右拉动一段距离,松手后,若观察到
活塞回到原位
,则表明装置气密性良好。(2)要比较金属的形状对反应快慢的影响,应选择的实验编号是
①③
(填序号)。(3)实验①中试管外壁发烫,说明铝与盐酸的反应是放热反应,实验测得该反应中产生气体的反应速度与反应时间的关系如图2所示,你认为在t₂~t₃时间段内反应速度逐渐减小的主要原因是
铝与盐酸反应消耗了盐酸,盐酸的浓度变小,反应速度逐渐减小
。

答案:
9.
(1)活塞回到原位
(2)①③
(3)铝与盐酸反应消耗了盐酸,盐酸的浓度变小,反应速度逐渐减小
(1)活塞回到原位
(2)①③
(3)铝与盐酸反应消耗了盐酸,盐酸的浓度变小,反应速度逐渐减小
查看更多完整答案,请扫码查看


