2025年效率暑假江苏人民出版社九年级化学沪教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年效率暑假江苏人民出版社九年级化学沪教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第65页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
1. 已知某尿素样品中含有不含氮素的杂质,经测定该化肥样品含氮量为40%,则该化肥样品尿素的纯度接近 ( )
A.40%
B.50%
C.86%
D.98%
A.40%
B.50%
C.86%
D.98%
答案:
C 解析:设化肥样品质量为 m,尿素[CO(NH₂)₂]的纯度接近 x%,则有 m×40%=m×x%×$\frac{28}{60}$×100%,解得 x%≈86%,选项 C 正确。
2. 一份质量为4 g的合金,与足量的盐酸完全反应生成$0.2 g H_2,$则该合金可能是( )
A.Fe-Zn合金
B.Fe-Cu合金
C.Fe-Mg合金
D.Mg-Al合金
A.Fe-Zn合金
B.Fe-Cu合金
C.Fe-Mg合金
D.Mg-Al合金
答案:
C 解析:根据活泼金属能与盐酸反应生成氢气,当生成0.2 g的氢气时,需要铁5.6 g、锌6.5 g、镁2.4 g、铝1.8 g,因为铜与盐酸不反应,相当于需要无穷大。利用平均值原理可知,这4 g合金只能是铁-镁合金,故本题正确答案为 C。
3. 喜树中含有一种被称为喜树碱的生物碱,这种碱的相对分子质量在300~400之间,实验分析得知其元素组成为:C占69.0%、O占18.4%,且O含量为H的4倍,其余为N,则一个喜树碱分子中含有的原子总数为 ( )
A.41
B.42
C.43
D.44
A.41
B.42
C.43
D.44
答案:
B 解析:由O占18.4%,且O含量为H的4倍,则H元素的含量为4.6%,N元素的含量为1-69.0%-4.6%-18.4%=8%,则该物质中C、H、O、N的原子个数比为$\frac{69.0\%}{12}:\frac{4.6\%}{1}:\frac{18.4\%}{16}:\frac{8\%}{14}=10:8:2:1$,则该物质的化学式为$(C_{10}H_{8}O_{2}N)_{n}$,又喜树碱分子的相对分子质量在300~400之间,$300<(12×10+1×8+16×2+14)×n<400$,则n=2符合,即物质的化学式为$C_{20}H_{16}O_{4}N_{2}$,则1个分子中含有20+16+4+2=42个原子,故选:B。
4. 20℃时$,Na_2CO_3$溶解度为$21.8 g,NaHCO_3$溶解度为9.6 g。20℃时,将$21.2 g Na_2CO_3$溶于103.6 g水中配成溶液,然后向此溶液中通入足量$CO_2,$则析出晶体的质量为 ( )
A.36 g
B.12 g
C.24 g
D.44 g
A.36 g
B.12 g
C.24 g
D.44 g
答案:
C 解析:根据碳酸钠的溶解度,求出103.6 g水中最多溶解$Na_{2}CO_{3}$质量为$21.8×103.6/100g=22.6>21.2$,说明此碳酸钠溶液不是饱和溶液,$Na_{2}CO_{3}$与$CO_{2}$发生:$Na_{2}CO_{3}+CO_{2}+H_{2}O=2NaHCO_{3}$,21.2 g$Na_{2}CO_{3}$生成$NaHCO_{3}$的质量为$\frac{2×84×21.2}{106}g=33.6g$,根据碳酸氢钠的溶解度,103.6 g水中最多溶解碳酸氢钠的质量为$9.6×103.6/100g=9.9g$,则析出晶体的质量为(33.6-9.9)g=23.7,约为24 g,故选项C正确。
5. 我国景德镇生产的瓷器在世界上享有盛誉,瓷器主要成分为$Al_2(Si_2O_5)(OH)_4,$则化学式中氢元素与氧元素的质量之比为 ( )
A.1∶16
B.1∶24
C.1∶36
D.4∶9
A.1∶16
B.1∶24
C.1∶36
D.4∶9
答案:
C 解析:由化学式$Al_{2}(Si_{2}O_{5})(OH)_{4}$,则化学式中氢元素与氧元素的质量之比为4:[(5+4)×16]=1:36。
6. 甲、乙、丙、丁四种物质在反应前后的质量关系如图所示,下列说法错误的是 ( )
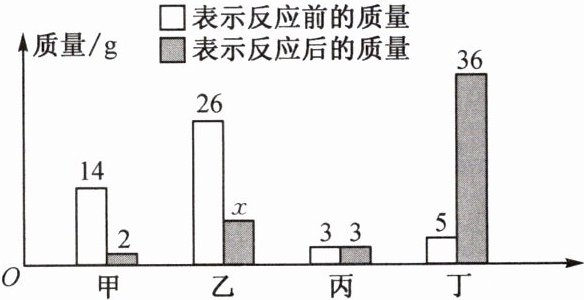
A.参加反应的甲、乙质量之比为2∶7
B.丙可能是该反应的催化剂
C.丁一定是化合物
D.x的值是7

A.参加反应的甲、乙质量之比为2∶7
B.丙可能是该反应的催化剂
C.丁一定是化合物
D.x的值是7
答案:
A 解析:由质量守恒知(14-2)+(26-x)=36-5,得x=7,D项正确;参加反应的甲、乙质量之比为(14-2):(26-7)=12:19,A项错误;由于反应中丙的质量没有变化,丙可能是催化剂,B项正确;丁是甲和乙化合形成,因此是化合物,C项正确。
7. 工业上制金刚砂(SiC)的化学反应为$SiO_2 + 3C \xlongequal{高温} SiC + 2CO↑,$在这个氧化还原反应中,氧化剂与还原剂的物质的量之比是 ( )
A.1∶2
B.2∶1
C.1∶1
D.3∶5
A.1∶2
B.2∶1
C.1∶1
D.3∶5
答案:
A 解析:碳元素化合价从0价部分升高到+2价,部分降低到-4价,其他元素的化合价不变,CO是氧化产物,SiC是还原产物,所以根据方程式可知氧化剂与还原剂的物质的量之比是1:2,答案选A。
8. 铜粉和碳粉的混合物在空气中充分灼烧后,最终得到的黑色物质与原混合物质量相等,则碳粉在原混合物中的质量分数为 ( )
A.15.8%
B.20%
C.80%
D.84.2%
A.15.8%
B.20%
C.80%
D.84.2%
答案:
B 解析:加热碳和铜的混合物反应生成二氧化碳气体和氧化铜固体,固体质量不变相当产生氧化铜的质量等于反应物碳和铜的质量,因此碳粉的质量分数等于氧化铜中氧元素的质量分数,则有$\frac{16}{80}×100\% =20\%$。
9. 2.3 g纯净金属钠在干燥空气中被氧化后得到3.5 g固体,由此可判断出产物是 ( )
$A. Na_2O B. Na_2O_2 C. Na_2O$和$Na_2O_2$的混合物 D. 无法确定
$A. Na_2O B. Na_2O_2 C. Na_2O$和$Na_2O_2$的混合物 D. 无法确定
答案:
C 解析:设金属钠氧化产物中氧化钠为x mol,过氧化钠为y mol,根据方程式可知4Na+O₂=2Na₂O,2Na+O₂=Na₂O₂2x mol x mol 2y mol y mol则2x+2y=2.3 g÷23,62x+78y=3.5解得:x=0.025,y=0.025,所以$Na_{2}O$和$Na_{2}O_{2}$均存在。
10. 一定条件下,在一个密闭容器中发生某反应,测得反应过程中物质的质量如下表所示:
|物质|X|Y|Z|Q|
|第一次测得的质量/g|68|16|4.4|3.6|
|第二次测得的质量/g|4|未测|48.4|39.6|
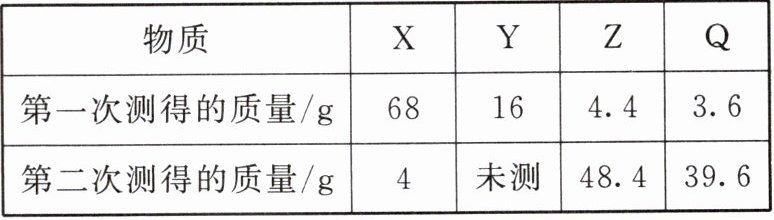
下列判断错误的是 ( )
A.该反应可能是化合反应
B.若X为氧气,则该反应为氧化反应
C.第二次测量时,Y已完全参加反应
D.该反应中Z与Q质量变化之比为11∶9
|物质|X|Y|Z|Q|
|第一次测得的质量/g|68|16|4.4|3.6|
|第二次测得的质量/g|4|未测|48.4|39.6|

下列判断错误的是 ( )
A.该反应可能是化合反应
B.若X为氧气,则该反应为氧化反应
C.第二次测量时,Y已完全参加反应
D.该反应中Z与Q质量变化之比为11∶9
答案:
A 解析:由表中数据知X减少64 g,Z增加44 g,Q增加36 g,则Y减少16 g,因此反应质量变化关系如下:X + Y=Z + Q64 g 16 g 44 g 36 g因此反应不是化合反应,A项错误;若X是氧气,反应为氧化反应,B项正确;第二次测量时Y的质量为0 g,C项正确;反应中Z与Q质量变化之比为44:36=11:9,D项正确。
查看更多完整答案,请扫码查看


