2025年效率暑假江苏人民出版社九年级化学沪教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年效率暑假江苏人民出版社九年级化学沪教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第41页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
23. 下图中的每个方格表示有关的一种反应物或生成物,M分解生成A、B、C的物质的量之比为1∶1∶1,其中A和C为无色气体。

(1)物质M是______(写名称),C是______(写化学式)。
(2)M与盐酸反应生成A的离子方程式:______。
(3)反应②的离子方程式:______。
(4)G与木炭反应的化学方程式:______。
(5)F生成G的化学方程式:______。

(1)物质M是______(写名称),C是______(写化学式)。
(2)M与盐酸反应生成A的离子方程式:______。
(3)反应②的离子方程式:______。
(4)G与木炭反应的化学方程式:______。
(5)F生成G的化学方程式:______。
答案:
(1)碳酸氢铵$NH_{3}$
(2)$H^{+}+HCO_{3}^{-}=$$C{O}_{2}\uparrow +{H}_{2}O$
(3)$3Cu+8{H}^{+}+2N{O}_{3}^{-}=$$3C{u}^{2+}+2NO\uparrow +4{H}_{2}O$
(4)$C+4HN{O}_{3}(浓)\xlongequal{\triangle }C{O}_{2}\uparrow +4N{O}_{2}\uparrow +2{H}_{2}O$
(5)$3N{O}_{2}+{H}_{2}O=2HN{O}_{3}+NO$解析:由题给条件可知,M 为化合物,与 NaOH反应生成 C,C 为气体,则 C 为$NH_{3}$,即 M 为铵盐,C 与 D 在催化剂的作用下生成 E,应为氨气的催化氧化,$4N{H}_{3}+5{O}_{2}\frac{\underline{催化剂}}{\triangle }4NO+6{H}_{2}O,$即 D 为$O_{2}$,E 为 NO,NO 与氧气反应生成$NO_{2},$即 F 为$NO_{2}$,G 能与木炭、铜发生反应,且 G 是由 F生成,则 G 为$HNO_{3}$,木炭与硝酸反应生成$CO_{2}$、$NO_{2}$、$H_{2}O$,即 A 为$CO_{2}$,因为 M 受热分解生成 A、B、C 物质的量之比为$1:1:1$,则 M 为$NH_{4}HCO_{3}$。
(1)根据上述分析,M 为碳酸氢铵,C为$NH_{3}$;
(2)$NH_{4}HCO_{3}$与盐酸的反应:$HCO_{3}^{-}+H^{+}=CO_{2}\uparrow +H_{2}O$;
(3)反应②是铜与稀硝酸的反应,其离子反应方程式为:$3Cu+$$8H^{+}+2NO_{3}^{-}=3Cu^{2+}+2NO\uparrow +4H_{2}O;$
(4)木炭与硝酸反应:$C+4HN{O}_{3}(浓)\xlongequal{\triangle }$$CO_{2}\uparrow +4NO_{2}\uparrow +2H_{2}O$;
(5)$NO_{2}$生成硝酸,是$NO_{2}$与水的反应,反应方程式为:$3NO_{2}+H_{2}O=$$2HNO_{3}+NO$。
(2)$H^{+}+HCO_{3}^{-}=$$C{O}_{2}\uparrow +{H}_{2}O$
(3)$3Cu+8{H}^{+}+2N{O}_{3}^{-}=$$3C{u}^{2+}+2NO\uparrow +4{H}_{2}O$
(4)$C+4HN{O}_{3}(浓)\xlongequal{\triangle }C{O}_{2}\uparrow +4N{O}_{2}\uparrow +2{H}_{2}O$
(5)$3N{O}_{2}+{H}_{2}O=2HN{O}_{3}+NO$解析:由题给条件可知,M 为化合物,与 NaOH反应生成 C,C 为气体,则 C 为$NH_{3}$,即 M 为铵盐,C 与 D 在催化剂的作用下生成 E,应为氨气的催化氧化,$4N{H}_{3}+5{O}_{2}\frac{\underline{催化剂}}{\triangle }4NO+6{H}_{2}O,$即 D 为$O_{2}$,E 为 NO,NO 与氧气反应生成$NO_{2},$即 F 为$NO_{2}$,G 能与木炭、铜发生反应,且 G 是由 F生成,则 G 为$HNO_{3}$,木炭与硝酸反应生成$CO_{2}$、$NO_{2}$、$H_{2}O$,即 A 为$CO_{2}$,因为 M 受热分解生成 A、B、C 物质的量之比为$1:1:1$,则 M 为$NH_{4}HCO_{3}$。
(1)根据上述分析,M 为碳酸氢铵,C为$NH_{3}$;
(2)$NH_{4}HCO_{3}$与盐酸的反应:$HCO_{3}^{-}+H^{+}=CO_{2}\uparrow +H_{2}O$;
(3)反应②是铜与稀硝酸的反应,其离子反应方程式为:$3Cu+$$8H^{+}+2NO_{3}^{-}=3Cu^{2+}+2NO\uparrow +4H_{2}O;$
(4)木炭与硝酸反应:$C+4HN{O}_{3}(浓)\xlongequal{\triangle }$$CO_{2}\uparrow +4NO_{2}\uparrow +2H_{2}O$;
(5)$NO_{2}$生成硝酸,是$NO_{2}$与水的反应,反应方程式为:$3NO_{2}+H_{2}O=$$2HNO_{3}+NO$。
24. 如图,A、B、C、D、E分别代表氧化铁、稀盐酸、一氧化碳、碳酸钠溶液、氯化钡溶液中的一种。一定条件下相连环的物质间能发生反应,不相连环的物质间不发生反应,且B的相对分子质量小于D。请填空:

(1)写出下列物质的化学式:A______,B______。
(2)写出D与E反应的化学方程式:______。

(1)写出下列物质的化学式:A______,B______。
(2)写出D与E反应的化学方程式:______。
答案:
(1)$BaCl_{2}$$Na_{2}CO_{3}$
(2)$3CO+F{e}_{2}{O}_{3}\xlongequal{高温}$$2Fe+3CO_{2}$解析:由题给反应要求及所给物质种类,结合酸、碱、盐、氧化物间反应规律,知 A 是氯化钡、B 是碳酸钠、C 是稀盐酸、D 是氧化铁、E是一氧化碳。
(1)$BaCl_{2}$$Na_{2}CO_{3}$
(2)$3CO+F{e}_{2}{O}_{3}\xlongequal{高温}$$2Fe+3CO_{2}$解析:由题给反应要求及所给物质种类,结合酸、碱、盐、氧化物间反应规律,知 A 是氯化钡、B 是碳酸钠、C 是稀盐酸、D 是氧化铁、E是一氧化碳。
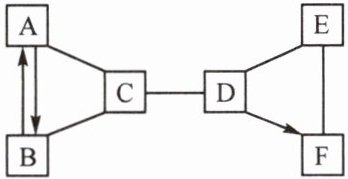
25. A~F是初中化学常见的物质,已知A、B、C、D、E是五种不同类别的物质,A是空气中含有的一种气体,E是地壳中含量最多的金属元素组成的单质,F中各元素质量之比为2∶1∶2,六种物质之间的反应与转化关系均为初中化学常见的化学反应,图中“—”表示相连的物质能相互反应,“→”表示一种物质转化成另一种物质(部分反应物、生成物及反应条件已略去)。请回答下列问题:
(1)E物质的化学式为______。
(2)A和C反应的化学方程式为______。
(3)E和F反应的化学方程式为______。
(4)如图所示的化学反应中涉及的基本反应类型有______种。
(1)E物质的化学式为______。
(2)A和C反应的化学方程式为______。
(3)E和F反应的化学方程式为______。
(4)如图所示的化学反应中涉及的基本反应类型有______种。

答案:
(1) Al
(2)$Ca(OH)_{2}+CO_{2}=CaCO_{3}\downarrow +H_{2}O$
(3)$2Al+3CuSO_{4}=Al_{2}(SO_{4})_{3}+3Cu$
(4) 2解析:E 是地壳中含量最多的金属元素组成的单质,故 E 是铝,F 中各元素质量之比为$2:1:2,$能与铝反应,故 F 只能是硫酸铜,D 能生成硫酸铜,能与铝反应,故 D 是硫酸,A 是空气中含有的一种气体,能与 B 相互转化,能与 C 反应,故 A可能是二氧化碳,B 是碳酸钠,C 可能是氢氧化钙,代入框图,推断合理。
(1)E 物质是铝,故填:Al。
(2)A 和C 反应是氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,化学方程式为$Ca(OH)_{2}+$$CO_{2}=CaCO_{3}\downarrow +H_{2}O$,故填:$Ca(OH)_{2}+$$CO_{2}=CaCO_{3}\downarrow +H_{2}O$。
(3)E 和 F 反应是铝和硫酸铜反应生成硫酸铝和铜,化学方程式为$2Al+3CuSO_{4}=Al_{2}(SO_{4})_{3}+3Cu$,故填:$2Al+3CuSO_{4}=Al_{2}(SO_{4})_{3}+3Cu$。
(4)如图的化学反应中涉及到 的基本反应类型有置换反应和复分解反应两种,故填:2。
(1) Al
(2)$Ca(OH)_{2}+CO_{2}=CaCO_{3}\downarrow +H_{2}O$
(3)$2Al+3CuSO_{4}=Al_{2}(SO_{4})_{3}+3Cu$
(4) 2解析:E 是地壳中含量最多的金属元素组成的单质,故 E 是铝,F 中各元素质量之比为$2:1:2,$能与铝反应,故 F 只能是硫酸铜,D 能生成硫酸铜,能与铝反应,故 D 是硫酸,A 是空气中含有的一种气体,能与 B 相互转化,能与 C 反应,故 A可能是二氧化碳,B 是碳酸钠,C 可能是氢氧化钙,代入框图,推断合理。
(1)E 物质是铝,故填:Al。
(2)A 和C 反应是氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,化学方程式为$Ca(OH)_{2}+$$CO_{2}=CaCO_{3}\downarrow +H_{2}O$,故填:$Ca(OH)_{2}+$$CO_{2}=CaCO_{3}\downarrow +H_{2}O$。
(3)E 和 F 反应是铝和硫酸铜反应生成硫酸铝和铜,化学方程式为$2Al+3CuSO_{4}=Al_{2}(SO_{4})_{3}+3Cu$,故填:$2Al+3CuSO_{4}=Al_{2}(SO_{4})_{3}+3Cu$。
(4)如图的化学反应中涉及到 的基本反应类型有置换反应和复分解反应两种,故填:2。
查看更多完整答案,请扫码查看


