第64页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
8 氢化钙($CaH_2$)遇水发生化学反应,生成氢氧化钙和氢气($CaH_2 + 2H_2O \xlongequal{} Ca(OH)_2 + 2H_2↑$)。为了测定某样品中氢化钙的含量,进行了如图所示实验,请计算:
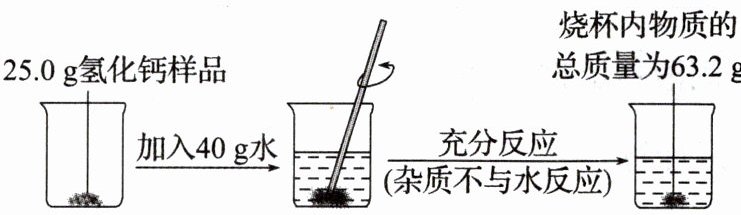
(25.0g氢化钙样品加入40g水,充分反应(杂质不与水反应),烧杯内物质的总质量为63.2g)
(1)生成氢气的质量是
(2)计算该样品中氢化钙的质量。(要求写出计算过程)

(25.0g氢化钙样品加入40g水,充分反应(杂质不与水反应),烧杯内物质的总质量为63.2g)
(1)生成氢气的质量是
1.8
g。(2)计算该样品中氢化钙的质量。(要求写出计算过程)
答案:
(1)1.8
(2)解:设样品中氢化钙的质量为x。CaH₂+2H₂O$\xlongequal{\;\;}$Ca(OH)₂+2H₂↑,42 4,x 1.8g,$\frac{42}{4}=\frac{x}{1.8\;g}$ x=18.9g,答:该样品中氢化钙的质量为18.9g。
(1)1.8
(2)解:设样品中氢化钙的质量为x。CaH₂+2H₂O$\xlongequal{\;\;}$Ca(OH)₂+2H₂↑,42 4,x 1.8g,$\frac{42}{4}=\frac{x}{1.8\;g}$ x=18.9g,答:该样品中氢化钙的质量为18.9g。
9 取一定量碱式碳酸铜[$Cu_2(OH)_2CO_3$]粉末放入烧杯中,加入稀硫酸至恰好完全反应(假设气体全部扩散),测得实验过程中烧杯及烧杯内物质的质量随时间变化关系如图所示。
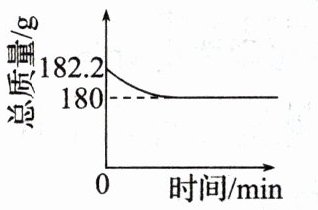
[反应原理:$Cu_2(OH)_2CO_3 + 2H_2SO_4 \xlongequal{} 2CuSO_4 + CO_2↑ + 3H_2O$]
请计算:(1)生成的二氧化碳质量为
(2)参加反应的硫酸质量是多少?(请严格按照解题步骤写出解题过程)

[反应原理:$Cu_2(OH)_2CO_3 + 2H_2SO_4 \xlongequal{} 2CuSO_4 + CO_2↑ + 3H_2O$]
请计算:(1)生成的二氧化碳质量为
2.2
g。(2)参加反应的硫酸质量是多少?(请严格按照解题步骤写出解题过程)
答案:
(1)2.2
(2)解:设参加反应的硫酸的质量为x。Cu₂(OH)₂CO₃+2H₂SO₄$\xlongequal{\;\;}$2CuSO₄+CO₂↑+3H₂O,196 44,x 2.2g,$\frac{196}{44}=\frac{x}{2.2\;g}$ x=9.8g,答:参加反应的硫酸的质量为9.8g。
(1)2.2
(2)解:设参加反应的硫酸的质量为x。Cu₂(OH)₂CO₃+2H₂SO₄$\xlongequal{\;\;}$2CuSO₄+CO₂↑+3H₂O,196 44,x 2.2g,$\frac{196}{44}=\frac{x}{2.2\;g}$ x=9.8g,答:参加反应的硫酸的质量为9.8g。
查看更多完整答案,请扫码查看


