第20页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
8(2024·三明期中)小明整理的“氧气”思维导图中错误的是(

A.①处:“物理性质”中可添加“密度大于空气”
B.②处:“用途”中可添加“作燃料”
C.③处:“气体产生”中可添加“过氧化氢$\xrightarrow{二氧化锰}$水+氧气”
D.④处:“气体收集”中可添加“向上排空气法”
B
)
A.①处:“物理性质”中可添加“密度大于空气”
B.②处:“用途”中可添加“作燃料”
C.③处:“气体产生”中可添加“过氧化氢$\xrightarrow{二氧化锰}$水+氧气”
D.④处:“气体收集”中可添加“向上排空气法”
答案:
B A、氧气的密度大于空气的密度,密度属于物理性质,正确;B、氧气具有助燃性,没有可燃性,不能作燃料,错误;C、实验室中过氧化氢溶液在二氧化锰的催化作用下分解为水和氧气,反应的文字表达式为过氧化氢$\xrightarrow{二氧化锰}$水+氧气,正确;D、氧气的密度大于空气,所以收集方法可以用向上排空气法,正确。
(1)仪器 a 的名称是
(2)实验室用 B 装置制取氧气时,长颈漏斗末端应伸入液面以下,原因是
(3)实验室用高锰酸钾制取一瓶较纯净的氧气,应选用装置 A 和
(4)将装置 F 装满水,用排水法收集氢气,气体应从
集气瓶
。(2)实验室用 B 装置制取氧气时,长颈漏斗末端应伸入液面以下,原因是
防止生成的氧气从长颈漏斗下端管口逸出
。(3)实验室用高锰酸钾制取一瓶较纯净的氧气,应选用装置 A 和
E
(从 C~E 中选填),反应的文字表达式为高锰酸钾$\xrightarrow{加热}$锰酸钾+二氧化锰+氧气
,装置 A 中试管口略向下倾斜的原因是防止冷凝水回流,使试管炸裂
。(4)将装置 F 装满水,用排水法收集氢气,气体应从
m
(填“m”或“n”)导管口进入。
答案:
(1)集气瓶
(2)防止生成的氧气从长颈漏斗下端管口逸出
(3)E 高锰酸钾$\xrightarrow{加热}$锰酸钾+二氧化锰+氧气 防止冷凝水回流,使试管炸裂
(4)m
(1)集气瓶
(2)防止生成的氧气从长颈漏斗下端管口逸出
(3)E 高锰酸钾$\xrightarrow{加热}$锰酸钾+二氧化锰+氧气 防止冷凝水回流,使试管炸裂
(4)m
10 化学兴趣小组对实验室制取氧气进行了如下探究。
探究二氧化锰在过氧化氢分解反应中的作用
实验1:在试管中加入5 mL 5%过氧化氢溶液,把带火星的木条伸入试管,观察现象。(如图)
实验2:向上述试管中加入二氧化锰粉末,把带火星的木条伸入试管,有大量气泡冒出,带火星的木条复燃。
实验3:待上述试管中没有现象发生时,重新加入过氧化氢溶液,把带火星的木条伸入试管,观察现象。

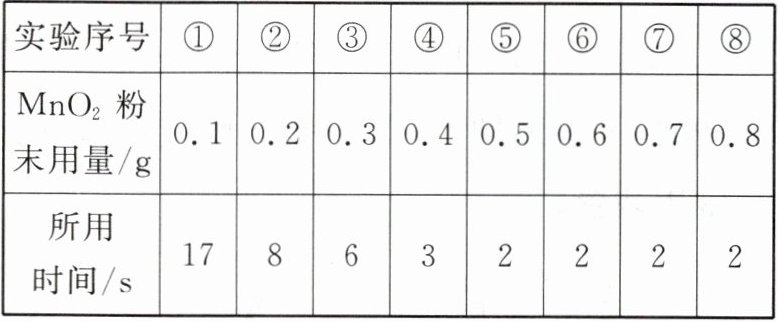
实验4:探究催化剂的用量对过氧化氢分解速率的影响。每次实验均用30 mL 10%的${H2O2}$溶液,采用不同质量${MnO2}$粉末做催化剂,测定收集到500 mL氧气所用的时间,结果如下:
|实验序号|①|②|③|④|⑤|⑥|⑦|⑧|
|${MnO2}$粉末用量/g|0.1|0.2|0.3|0.4|0.5|0.6|0.7|0.8|
|所用时间/s|17|8|6|3|2|2|2|2|
(1)实验1中,观察到有气泡产生,带火星的木条未复燃。实验结论是
(2)写出实验2发生反应的文字表达式
(3)实验3的实验目的是
(4)由实验4的实验结果可得出的结论是
探究二氧化锰在过氧化氢分解反应中的作用
实验1:在试管中加入5 mL 5%过氧化氢溶液,把带火星的木条伸入试管,观察现象。(如图)
实验2:向上述试管中加入二氧化锰粉末,把带火星的木条伸入试管,有大量气泡冒出,带火星的木条复燃。
实验3:待上述试管中没有现象发生时,重新加入过氧化氢溶液,把带火星的木条伸入试管,观察现象。

实验4:探究催化剂的用量对过氧化氢分解速率的影响。每次实验均用30 mL 10%的${H2O2}$溶液,采用不同质量${MnO2}$粉末做催化剂,测定收集到500 mL氧气所用的时间,结果如下:
|实验序号|①|②|③|④|⑤|⑥|⑦|⑧|
|${MnO2}$粉末用量/g|0.1|0.2|0.3|0.4|0.5|0.6|0.7|0.8|
|所用时间/s|17|8|6|3|2|2|2|2|

(1)实验1中,观察到有气泡产生,带火星的木条未复燃。实验结论是
过氧化氢溶液分解产生氧气的速率很慢,氧气浓度很低,无法使带火星的木条复燃
。(2)写出实验2发生反应的文字表达式
过氧化氢$\xrightarrow{二氧化锰}$水+氧气
。(3)实验3的实验目的是
证明二氧化锰的化学性质没有改变
。(4)由实验4的实验结果可得出的结论是
催化剂的用量能影响反应的速率
。
答案:
(1)过氧化氢溶液分解产生氧气的速率很慢,氧气浓度很低,无法使带火星的木条复燃
(2)过氧化氢$\xrightarrow{二氧化锰}$水+氧气
(3)证明二氧化锰的化学性质没有改变
(4)催化剂的用量能影响反应的速率
(1)过氧化氢溶液分解产生氧气的速率很慢,氧气浓度很低,无法使带火星的木条复燃
(2)过氧化氢$\xrightarrow{二氧化锰}$水+氧气
(3)证明二氧化锰的化学性质没有改变
(4)催化剂的用量能影响反应的速率
查看更多完整答案,请扫码查看


