2025年快乐暑假八升九年级科学浙教版延边人民出版社
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年快乐暑假八升九年级科学浙教版延边人民出版社 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第56页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
7. 下列资源的利用过程中,一定发生了化学变化的是(
A.风力发电
B.石油蒸馏得到汽油等
C.海水晒盐
D.煤分解得到煤焦油等
D
)A.风力发电
B.石油蒸馏得到汽油等
C.海水晒盐
D.煤分解得到煤焦油等
答案:
【解析】:
本题考察的是物理变化与化学变化的判断。我们需要分析每个选项中的过程,看其是否产生了新物质,从而确定是否发生了化学变化。
A选项,风力发电是将风能转化为电能,这个过程中没有新物质的生成,只是能量的转换,因此属于物理变化。
B选项,石油蒸馏得到汽油等是通过加热石油使其不同成分汽化然后冷凝收集的过程,这个过程中也没有新物质的生成,只是物质的分离,因此也属于物理变化。
C选项,海水晒盐是利用阳光和风力使海水中的水分蒸发,从而析出盐分,这个过程中同样没有新物质的生成,只是物质的分离,因此也属于物理变化。
D选项,煤分解得到煤焦油等是煤在高温下经过复杂化学反应分解成煤焦油、焦炭和煤气等新物质的过程,这个过程中有新物质的生成,因此属于化学变化。
综上所述,只有D选项中的过程发生了化学变化。
【答案】:D
本题考察的是物理变化与化学变化的判断。我们需要分析每个选项中的过程,看其是否产生了新物质,从而确定是否发生了化学变化。
A选项,风力发电是将风能转化为电能,这个过程中没有新物质的生成,只是能量的转换,因此属于物理变化。
B选项,石油蒸馏得到汽油等是通过加热石油使其不同成分汽化然后冷凝收集的过程,这个过程中也没有新物质的生成,只是物质的分离,因此也属于物理变化。
C选项,海水晒盐是利用阳光和风力使海水中的水分蒸发,从而析出盐分,这个过程中同样没有新物质的生成,只是物质的分离,因此也属于物理变化。
D选项,煤分解得到煤焦油等是煤在高温下经过复杂化学反应分解成煤焦油、焦炭和煤气等新物质的过程,这个过程中有新物质的生成,因此属于化学变化。
综上所述,只有D选项中的过程发生了化学变化。
【答案】:D
8. 实验室有两瓶失去标签的溶液,一瓶是稀盐酸,另一瓶是氢氧化钠溶液,下列试剂不能将它们鉴别出来的是(
A.酚酞试液
B.镁条
C.氯化钾溶液
D.氯化铜溶液
C
)A.酚酞试液
B.镁条
C.氯化钾溶液
D.氯化铜溶液
答案:
【解析】:
本题主要考查了酸和碱的化学性质,以及常见物质的鉴别。
A选项,酚酞试液是一种酸碱指示剂,遇到碱性溶液会变红,遇到酸性溶液则不变色。因此,将酚酞试液分别滴入两种溶液中,能使酚酞变红的是氢氧化钠溶液,无现象的是稀盐酸,可以鉴别,故A选项不符合题意。
B选项,镁条是一种活泼金属,能与稀盐酸反应生成氢气,产生气泡,而与氢氧化钠溶液不反应。因此,将镁条分别放入两种溶液中,有气泡产生的是稀盐酸,无现象的是氢氧化钠溶液,可以鉴别,故B选项不符合题意。
C选项,氯化钾溶液与稀盐酸和氢氧化钠溶液都不反应,混合后均无明显现象,因此不能鉴别,故C选项符合题意。
D选项,氯化铜溶液与氢氧化钠溶液反应会生成氢氧化铜蓝色沉淀,而与稀盐酸不反应。因此,将氯化铜溶液分别滴入两种溶液中,有蓝色沉淀产生的是氢氧化钠溶液,无现象的是稀盐酸,可以鉴别,故D选项不符合题意。
【答案】:C
本题主要考查了酸和碱的化学性质,以及常见物质的鉴别。
A选项,酚酞试液是一种酸碱指示剂,遇到碱性溶液会变红,遇到酸性溶液则不变色。因此,将酚酞试液分别滴入两种溶液中,能使酚酞变红的是氢氧化钠溶液,无现象的是稀盐酸,可以鉴别,故A选项不符合题意。
B选项,镁条是一种活泼金属,能与稀盐酸反应生成氢气,产生气泡,而与氢氧化钠溶液不反应。因此,将镁条分别放入两种溶液中,有气泡产生的是稀盐酸,无现象的是氢氧化钠溶液,可以鉴别,故B选项不符合题意。
C选项,氯化钾溶液与稀盐酸和氢氧化钠溶液都不反应,混合后均无明显现象,因此不能鉴别,故C选项符合题意。
D选项,氯化铜溶液与氢氧化钠溶液反应会生成氢氧化铜蓝色沉淀,而与稀盐酸不反应。因此,将氯化铜溶液分别滴入两种溶液中,有蓝色沉淀产生的是氢氧化钠溶液,无现象的是稀盐酸,可以鉴别,故D选项不符合题意。
【答案】:C
9. 向一定量硫酸和硫酸铜的混合溶液中,逐滴加入一定质量分数的氢氧化钠溶液,直至过量。某同学依据实验事实绘制了如图所示的曲线,下列说法正确的是( )
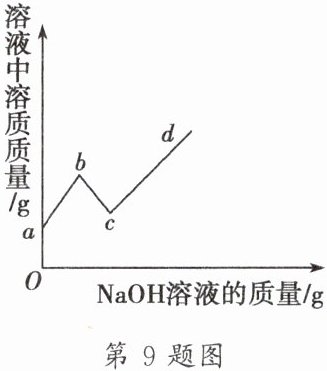
A.a至b段对应溶液的pH逐渐减小
B.b点对应溶液中的溶质为硫酸钠
C.c点对应溶液中的溶质种类最少
D.a至d段硫酸钠的质量逐渐增大
C

A.a至b段对应溶液的pH逐渐减小
B.b点对应溶液中的溶质为硫酸钠
C.c点对应溶液中的溶质种类最少
D.a至d段硫酸钠的质量逐渐增大
答案:
【解析】:
本题可根据氢氧化钠与硫酸、硫酸铜的反应原理,结合图像分析各阶段溶液中溶质的成分及pH的变化情况。
向一定量硫酸和硫酸铜的混合溶液中,逐滴加入一定质量分数的氢氧化钠溶液,氢氧化钠先与硫酸反应生成硫酸钠和水,此过程没有沉淀生成;当硫酸完全反应后,氢氧化钠再与硫酸铜反应生成氢氧化铜蓝色沉淀和硫酸钠。
A选项:a至b段是氢氧化钠与硫酸反应的过程,随着氢氧化钠溶液的加入,硫酸逐渐被消耗,溶液的酸性逐渐减弱,对应溶液的pH逐渐增大,而不是减小,故A选项错误。
B选项:b点时硫酸恰好完全反应,此时溶液中的溶质有反应生成的硫酸钠以及还未反应的硫酸铜,而不是只有硫酸钠,故B选项错误。
C选项:a至c段发生氢氧化钠与硫酸、硫酸铜的反应,c点时硫酸铜恰好完全反应,此时溶液中的溶质只有硫酸钠,溶质种类最少,故C选项正确。
D选项:a至c段,氢氧化钠与硫酸、硫酸铜反应生成硫酸钠,硫酸钠的质量逐渐增大;c至d段,氢氧化钠过量,不再生成硫酸钠,硫酸钠的质量不变,故D选项错误。
【答案】:C
本题可根据氢氧化钠与硫酸、硫酸铜的反应原理,结合图像分析各阶段溶液中溶质的成分及pH的变化情况。
向一定量硫酸和硫酸铜的混合溶液中,逐滴加入一定质量分数的氢氧化钠溶液,氢氧化钠先与硫酸反应生成硫酸钠和水,此过程没有沉淀生成;当硫酸完全反应后,氢氧化钠再与硫酸铜反应生成氢氧化铜蓝色沉淀和硫酸钠。
A选项:a至b段是氢氧化钠与硫酸反应的过程,随着氢氧化钠溶液的加入,硫酸逐渐被消耗,溶液的酸性逐渐减弱,对应溶液的pH逐渐增大,而不是减小,故A选项错误。
B选项:b点时硫酸恰好完全反应,此时溶液中的溶质有反应生成的硫酸钠以及还未反应的硫酸铜,而不是只有硫酸钠,故B选项错误。
C选项:a至c段发生氢氧化钠与硫酸、硫酸铜的反应,c点时硫酸铜恰好完全反应,此时溶液中的溶质只有硫酸钠,溶质种类最少,故C选项正确。
D选项:a至c段,氢氧化钠与硫酸、硫酸铜反应生成硫酸钠,硫酸钠的质量逐渐增大;c至d段,氢氧化钠过量,不再生成硫酸钠,硫酸钠的质量不变,故D选项错误。
【答案】:C
10. 小金完成了图示实验①②③,下列判断正确的是(
A.实验①中石灰水有剩余
B.实验②中有气泡产生
C.实验③中没有明显现象
D.实验③所得溶液中一定含$CaCl_{2}$和NaCl
D
)A.实验①中石灰水有剩余
B.实验②中有气泡产生
C.实验③中没有明显现象
D.实验③所得溶液中一定含$CaCl_{2}$和NaCl
答案:
解:实验①:Ca(OH)₂ + 2HCl = CaCl₂ + 2H₂O,因加入“一定量”稀盐酸,可能恰好反应或盐酸过量,石灰水不一定剩余,A错误。
实验②:Ca(OH)₂ + Na₂CO₃ = CaCO₃↓ + 2NaOH,现象为产生白色沉淀,无气泡,B错误。
实验③:混合后得无色澄清溶液,说明CaCO₃沉淀完全溶解,涉及反应:CaCO₃ + 2HCl = CaCl₂ + H₂O + CO₂↑,NaOH + HCl = NaCl + H₂O,溶液由浑浊变澄清,有明显现象,C错误。
反应后溶液中溶质一定有CaCl₂(来自①和③中CaCO₃与HCl反应)和NaCl(来自②中生成的NaOH与过量HCl反应),D正确。
答案:D
实验②:Ca(OH)₂ + Na₂CO₃ = CaCO₃↓ + 2NaOH,现象为产生白色沉淀,无气泡,B错误。
实验③:混合后得无色澄清溶液,说明CaCO₃沉淀完全溶解,涉及反应:CaCO₃ + 2HCl = CaCl₂ + H₂O + CO₂↑,NaOH + HCl = NaCl + H₂O,溶液由浑浊变澄清,有明显现象,C错误。
反应后溶液中溶质一定有CaCl₂(来自①和③中CaCO₃与HCl反应)和NaCl(来自②中生成的NaOH与过量HCl反应),D正确。
答案:D
11. 下列物质的用途不正确的是(
A
)
答案:
【解析】:
A. 纯碱是碳酸钠的俗称,其水溶液呈碱性,但纯碱不能用于改良酸性土壤,因为纯碱的价格相对较高,且其碱性较强,可能对土壤和植物造成不良影响,通常使用熟石灰来改良酸性土壤,故A选项错误;
B. 一氧化碳具有可燃性,燃烧时放出大量的热,因此一氧化碳可以作燃料,故B选项正确;
C. 氧气具有助燃性,在炼钢过程中,氧气可以与生铁中的杂质反应,提高钢的质量,故C选项正确;
D. 石墨具有良好的导电性,因此石墨可以作电极,故D选项正确。
【答案】:A
A. 纯碱是碳酸钠的俗称,其水溶液呈碱性,但纯碱不能用于改良酸性土壤,因为纯碱的价格相对较高,且其碱性较强,可能对土壤和植物造成不良影响,通常使用熟石灰来改良酸性土壤,故A选项错误;
B. 一氧化碳具有可燃性,燃烧时放出大量的热,因此一氧化碳可以作燃料,故B选项正确;
C. 氧气具有助燃性,在炼钢过程中,氧气可以与生铁中的杂质反应,提高钢的质量,故C选项正确;
D. 石墨具有良好的导电性,因此石墨可以作电极,故D选项正确。
【答案】:A
12. 某锥形瓶内盛有盐酸和氯化铜的混合溶液100g,向其中加入溶质质量分数为10%的氢氧化钠溶液,锥形瓶内溶液质量$m_{1}与加入的氢氧化钠溶液质量m_{2}$的变化关系如图所示。下列说法错误的是(
A.反应至A点时,所加NaOH溶液的质量为40g
B.反应至A点时,溶液中的溶质有$CuCl_{2}$和NaCl
C.反应至B点时,锥形瓶内溶液的质量为280.4g
D.反应至B点时,锥形瓶内溶液中NaCl的质量为23.4g
D
)A.反应至A点时,所加NaOH溶液的质量为40g
B.反应至A点时,溶液中的溶质有$CuCl_{2}$和NaCl
C.反应至B点时,锥形瓶内溶液的质量为280.4g
D.反应至B点时,锥形瓶内溶液中NaCl的质量为23.4g
答案:
【解析】:
本题可根据氢氧化钠与盐酸、氯化铜的反应原理,结合图像信息来分析各选项。
向盐酸和氯化铜的混合溶液中加入氢氧化钠溶液时,氢氧化钠先与盐酸反应生成氯化钠和水,当盐酸完全反应后,氢氧化钠再与氯化铜反应生成氢氧化铜沉淀和氯化钠。
选项A:
从图像可知,开始加入氢氧化钠溶液时,溶液质量增加,当加入到一定质量时,溶液质量增加幅度变小,说明此时开始发生氢氧化钠与氯化铜的反应,即A点时盐酸恰好完全反应。
设与盐酸反应的氢氧化钠溶液质量为$x$。
$HCl + NaOH = NaCl + H_{2}O$
$40$ $58.5$
$10\%x$ $y$
由图像可知,与盐酸反应后溶液质量增加了$140g - 100g = 40g$,根据质量守恒定律,参加反应的氢氧化钠溶液质量就是$40g$,故A选项正确。
选项B:
A点时盐酸恰好完全反应,此时氢氧化钠与盐酸反应生成了氯化钠,而氯化铜还未开始反应,所以溶液中的溶质有$CuCl_{2}$和$NaCl$,故B选项正确。
选项C:
B点时氯化铜恰好完全反应,加入氢氧化钠溶液的质量为$200g$,生成氢氧化铜沉淀的质量为$200g + 100g - m_{B}$。
设与氯化铜反应的氢氧化钠溶液质量为$z$,生成氢氧化铜沉淀的质量为$m$。
$CuCl_{2} + 2NaOH = Cu(OH)_{2}\downarrow + 2NaCl$
$80$ $98$
$10\%z$ $m$
与氯化铜反应的氢氧化钠溶液质量为$200g - 40g = 160g$,则生成氢氧化铜沉淀的质量$m = \frac{98}{80}×160g×10\% = 19.6g$。
所以B点时锥形瓶内溶液的质量为$100g + 200g - 19.6g = 280.4g$,故C选项正确。
选项D:
根据钠元素守恒,氢氧化钠中的钠元素全部转化到氯化钠中。
加入氢氧化钠的质量为$200g×10\% = 20g$,设生成氯化钠的质量为$w$。
$NaOH$~$NaCl$
$40$ $58.5$
$20g$ $w$
$\frac{40}{58.5}=\frac{20g}{w}$,解得$w = 29.25g$,故D选项错误。
【答案】:D
本题可根据氢氧化钠与盐酸、氯化铜的反应原理,结合图像信息来分析各选项。
向盐酸和氯化铜的混合溶液中加入氢氧化钠溶液时,氢氧化钠先与盐酸反应生成氯化钠和水,当盐酸完全反应后,氢氧化钠再与氯化铜反应生成氢氧化铜沉淀和氯化钠。
选项A:
从图像可知,开始加入氢氧化钠溶液时,溶液质量增加,当加入到一定质量时,溶液质量增加幅度变小,说明此时开始发生氢氧化钠与氯化铜的反应,即A点时盐酸恰好完全反应。
设与盐酸反应的氢氧化钠溶液质量为$x$。
$HCl + NaOH = NaCl + H_{2}O$
$40$ $58.5$
$10\%x$ $y$
由图像可知,与盐酸反应后溶液质量增加了$140g - 100g = 40g$,根据质量守恒定律,参加反应的氢氧化钠溶液质量就是$40g$,故A选项正确。
选项B:
A点时盐酸恰好完全反应,此时氢氧化钠与盐酸反应生成了氯化钠,而氯化铜还未开始反应,所以溶液中的溶质有$CuCl_{2}$和$NaCl$,故B选项正确。
选项C:
B点时氯化铜恰好完全反应,加入氢氧化钠溶液的质量为$200g$,生成氢氧化铜沉淀的质量为$200g + 100g - m_{B}$。
设与氯化铜反应的氢氧化钠溶液质量为$z$,生成氢氧化铜沉淀的质量为$m$。
$CuCl_{2} + 2NaOH = Cu(OH)_{2}\downarrow + 2NaCl$
$80$ $98$
$10\%z$ $m$
与氯化铜反应的氢氧化钠溶液质量为$200g - 40g = 160g$,则生成氢氧化铜沉淀的质量$m = \frac{98}{80}×160g×10\% = 19.6g$。
所以B点时锥形瓶内溶液的质量为$100g + 200g - 19.6g = 280.4g$,故C选项正确。
选项D:
根据钠元素守恒,氢氧化钠中的钠元素全部转化到氯化钠中。
加入氢氧化钠的质量为$200g×10\% = 20g$,设生成氯化钠的质量为$w$。
$NaOH$~$NaCl$
$40$ $58.5$
$20g$ $w$
$\frac{40}{58.5}=\frac{20g}{w}$,解得$w = 29.25g$,故D选项错误。
【答案】:D
13. 化学改变世界的途径是使物质发生化学变化。下列属于化学变化的是(
A.冰块制成冰雕
B.利用半透膜法从海水中获得淡水
C.泥土烧成瓷器
D.工业上从空气中分离出氧气
C
)A.冰块制成冰雕
B.利用半透膜法从海水中获得淡水
C.泥土烧成瓷器
D.工业上从空气中分离出氧气
答案:
【解析】:本题考察的是化学变化和物理变化的判断。化学变化是指有新物质生成的变化,物理变化则是指没有新物质生成的变化。
A选项,冰块制成冰雕,只是冰的形状发生了改变,并无新物质生成,因此是物理变化,故A选项错误。
B选项,利用半透膜法从海水中获得淡水,是利用半透膜的选择透过性将海水中的盐分和水分子分离,此过程中并无新物质生成,因此是物理变化,故B选项错误。
C选项,泥土烧成瓷器,泥土在高温下经过一系列复杂的化学反应,生成了新的物质——瓷器,因此是化学变化,故C选项正确。
D选项,工业上从空气中分离出氧气,是利用空气中各组分的沸点不同进行分离,此过程中并无新物质生成,因此是物理变化,故D选项错误。
【答案】:C
A选项,冰块制成冰雕,只是冰的形状发生了改变,并无新物质生成,因此是物理变化,故A选项错误。
B选项,利用半透膜法从海水中获得淡水,是利用半透膜的选择透过性将海水中的盐分和水分子分离,此过程中并无新物质生成,因此是物理变化,故B选项错误。
C选项,泥土烧成瓷器,泥土在高温下经过一系列复杂的化学反应,生成了新的物质——瓷器,因此是化学变化,故C选项正确。
D选项,工业上从空气中分离出氧气,是利用空气中各组分的沸点不同进行分离,此过程中并无新物质生成,因此是物理变化,故D选项错误。
【答案】:C
14. 下列说法正确的是(
A.粗盐提纯中蒸发时用玻璃棒搅拌是为了加快水分的蒸发
B.稀释浓硫酸需将水沿器壁缓慢倒入浓硫酸中,并不断搅拌
C.酸雨形成的原因是$CO_{2}和H_{2}O反应生成了H_{2}CO_{3}$
D.中和反应生成盐和水,生成盐和水的不一定是中和反应
D
)A.粗盐提纯中蒸发时用玻璃棒搅拌是为了加快水分的蒸发
B.稀释浓硫酸需将水沿器壁缓慢倒入浓硫酸中,并不断搅拌
C.酸雨形成的原因是$CO_{2}和H_{2}O反应生成了H_{2}CO_{3}$
D.中和反应生成盐和水,生成盐和水的不一定是中和反应
答案:
【解析】:
A选项:考察的是粗盐提纯的实验操作。在粗盐提纯的过程中,蒸发时用玻璃棒搅拌主要是为了防止液体局部过热而飞溅,并非为了加快水分的蒸发。因此,A选项错误。
B选项:考察的是浓硫酸的稀释操作。稀释浓硫酸时,应该将浓硫酸沿器壁缓慢倒入水中,并不断搅拌,以防止酸液飞溅。B选项描述的操作顺序错误,因此B选项错误。
C选项:考察的是酸雨形成的原因。酸雨的形成主要是由于化石燃料燃烧产生的二氧化硫、氮氧化物等酸性气体,经过复杂的大气化学反应,被雨水吸收溶解而成。二氧化碳和水反应生成碳酸,但碳酸的酸性较弱,不是酸雨形成的主要原因。因此,C选项错误。
D选项:考察的是中和反应的定义及判断。中和反应是酸和碱反应生成盐和水的反应。但是,生成盐和水的反应不一定是中和反应,例如二氧化碳和氢氧化钠反应生成碳酸钠和水,这不是中和反应。因此,D选项正确。
【答案】:D
A选项:考察的是粗盐提纯的实验操作。在粗盐提纯的过程中,蒸发时用玻璃棒搅拌主要是为了防止液体局部过热而飞溅,并非为了加快水分的蒸发。因此,A选项错误。
B选项:考察的是浓硫酸的稀释操作。稀释浓硫酸时,应该将浓硫酸沿器壁缓慢倒入水中,并不断搅拌,以防止酸液飞溅。B选项描述的操作顺序错误,因此B选项错误。
C选项:考察的是酸雨形成的原因。酸雨的形成主要是由于化石燃料燃烧产生的二氧化硫、氮氧化物等酸性气体,经过复杂的大气化学反应,被雨水吸收溶解而成。二氧化碳和水反应生成碳酸,但碳酸的酸性较弱,不是酸雨形成的主要原因。因此,C选项错误。
D选项:考察的是中和反应的定义及判断。中和反应是酸和碱反应生成盐和水的反应。但是,生成盐和水的反应不一定是中和反应,例如二氧化碳和氢氧化钠反应生成碳酸钠和水,这不是中和反应。因此,D选项正确。
【答案】:D
查看更多完整答案,请扫码查看


