2025年快乐暑假八升九年级科学浙教版延边人民出版社
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年快乐暑假八升九年级科学浙教版延边人民出版社 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第43页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
例2 为了测定一变质的NaOH样品(杂质只含$Na_2CO_3)$中NaOH的质量分数,小红同学采用沉淀法进行如下操作:取14.6g样品于烧杯中,加足量水配成溶液;在样品溶液中加入足量的$BaCl_2$溶液;待反应完全后,过滤。有关数据记录如下表:
|反应前烧杯和样品溶液总质量/g|加入的氯化钡溶液质量/g|过滤后烧杯和溶液总质量/g(溶液的损失忽略不计)|
|95|65|140.3|
(1)根据质量守恒定律,反应共生成沉淀____g。
(2)此样品中NaOH的质量分数是多少? (写出计算过程,计算结果保留至0.1%)
(3)测定此变质的NaOH样品中NaOH的质量分数,还可采用气体法。实验过程:取14.6g样品加入过量的10%稀盐酸,通过测定生成二氧化碳的质量计算NaOH的质量分数。请画出在14.6g样品中加入稀盐酸的质量与生成二氧化碳质量的曲线图。
|反应前烧杯和样品溶液总质量/g|加入的氯化钡溶液质量/g|过滤后烧杯和溶液总质量/g(溶液的损失忽略不计)|
|95|65|140.3|

(1)根据质量守恒定律,反应共生成沉淀____g。
(2)此样品中NaOH的质量分数是多少? (写出计算过程,计算结果保留至0.1%)
(3)测定此变质的NaOH样品中NaOH的质量分数,还可采用气体法。实验过程:取14.6g样品加入过量的10%稀盐酸,通过测定生成二氧化碳的质量计算NaOH的质量分数。请画出在14.6g样品中加入稀盐酸的质量与生成二氧化碳质量的曲线图。
答案:
(2)设参加反应的碳酸钠的质量为x
(3)设与氢氧化钠反应的盐酸溶液的质量为y,与碳酸钠反应的盐酸溶液的质量为z,生成二氧化碳的质量为a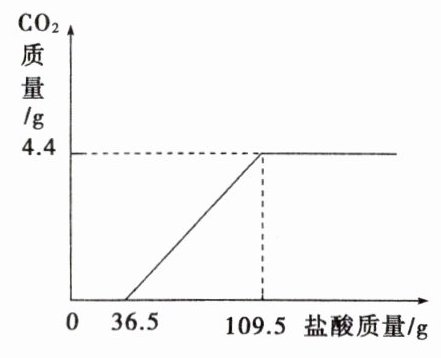
氢氧化钠的变质问题是学习的难点,但只要我们掌握基本的检验方法,可以举一反三。
【分析】
(1)根据质量守恒定律,反应共生成沉淀为:95g+65g-140.3g= 19.7g;
(1)根据质量守恒定律,反应共生成沉淀为:95g+65g-140.3g= 19.7g;
(2)设参加反应的碳酸钠的质量为x
BaCl_2+Na_2CO_3= BaCO_3↓+2NaCl
106 197
x 19.7g
$\frac{106}{x}= \frac{197}{19.7g}$
x= 10.6g
样品中氢氧化钠的质量分数为:$\frac{14.6g-10.6g}{14.6g}×100\%= 27.4\%$;
(3)设与氢氧化钠反应的盐酸溶液的质量为y,与碳酸钠反应的盐酸溶液的质量为z,生成二氧化碳的质量为a
NaOH+HCl= NaCl+H_2O
40 36.5
4g 10%×y
$\frac{40}{4g}= \frac{36.5}{10\%× y}$
y= 36.5g
Na_2CO_3+2HCl= 2NaCl+H_2O+CO_2↑
106 73 44
10.6g z×10% a
$\frac{106}{10.6g}= \frac{73}{z×10\%}= \frac{44}{a}$
z= 73g,a= 4.4g
加入稀盐酸的质量与生成二氧化碳质量的曲线图,如图:

【答案】
(1)19.7
(2)27.4%
(3)见分析图
(1)19.7
(2)27.4%
(3)见分析图
查看更多完整答案,请扫码查看


