第79页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
8. 化学与生产、生活、环保等密切相关。下列有关说法错误的是 ( )
A. 电池可将化学能转化为电能
B. 随意丢弃聚乙烯塑料不产生污染
C. 强热使煤焦化属于化学变化
D. 维生素D有助于骨骼的生长发育
A. 电池可将化学能转化为电能
B. 随意丢弃聚乙烯塑料不产生污染
C. 强热使煤焦化属于化学变化
D. 维生素D有助于骨骼的生长发育
答案:
B
9.(2024·淮安·一模)奥司他韦(化学式为C₁₆H₂₈N₂O₄)是目前治疗流感的药物之一,下列关于奥司他韦说法正确的是 ( )
A. 奥司他韦属于有机高分子化合物
B. 奥司他韦的相对分子质量为312 g
C. 奥司他韦中碳元素的质量分数最大
D. 流感时,吃药越多,康复越快
A. 奥司他韦属于有机高分子化合物
B. 奥司他韦的相对分子质量为312 g
C. 奥司他韦中碳元素的质量分数最大
D. 流感时,吃药越多,康复越快
答案:
C
10.(2022·广州)如图为我国不同年份的能源结构图。下列说法不正确的是 ( )
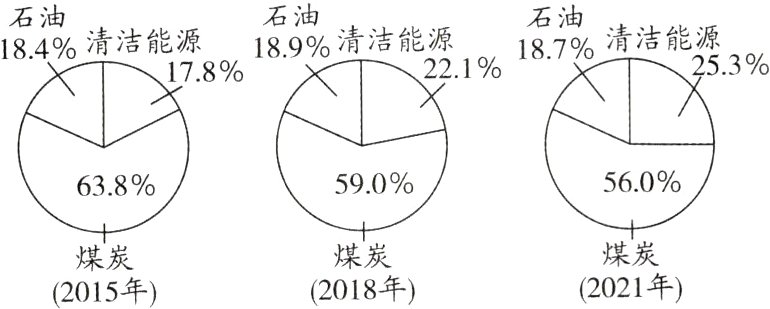
A. 我国能源结构中清洁能源占比呈增加趋势
B. 加大水电、风电的开发利用有利于减少环境污染
C. 天然气是比煤炭和石油更清洁的燃料
D. 液氢用作火箭燃料是因为氢气易于贮存和加注

A. 我国能源结构中清洁能源占比呈增加趋势
B. 加大水电、风电的开发利用有利于减少环境污染
C. 天然气是比煤炭和石油更清洁的燃料
D. 液氢用作火箭燃料是因为氢气易于贮存和加注
答案:
D解析:液氢用作火箭燃料是因为氢气的热值高,并不是氢气易于贮存和加注。
11.(2024·青岛中考)如图是某品牌维生素C泡腾片说明书的部分信息,已知柠檬酸具有酸的通性。下列说法不正确的是 ( )

A. 该泡腾片可以预防坏血病
B. 该泡腾片溶于水产生二氧化碳气体
C. 该泡腾片中维生素C的质量分数为25%
D. 用热水溶解该泡腾片可能导致效用降低

A. 该泡腾片可以预防坏血病
B. 该泡腾片溶于水产生二氧化碳气体
C. 该泡腾片中维生素C的质量分数为25%
D. 用热水溶解该泡腾片可能导致效用降低
答案:
C
12.(2024·盐城模拟)科学家研究开发氢能源的脚步从未停止。如图为利用MnFe₂O₄热化学循环制氢的反应流程,反应前后Mn 的化合价均为+2价。下列说法中错误的是 ( )
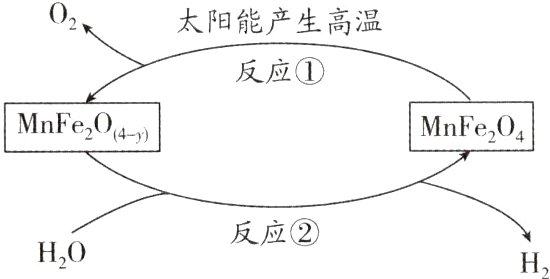
A. 若MnFe₂O(₄ - y)中y = 0.5,则MnFe₂O(₄ - y)中Fe³⁺与Fe²⁺ 的个数比为1:2
B. 与传统电解法制取氢气相比,该流程的优点是能够节约能源
C. 利用该流程每生成48 kg氧气,理论上能得到氢气的质量是6 kg
D. 氢气燃烧热值高,产物无污染,是最清洁的能源

A. 若MnFe₂O(₄ - y)中y = 0.5,则MnFe₂O(₄ - y)中Fe³⁺与Fe²⁺ 的个数比为1:2
B. 与传统电解法制取氢气相比,该流程的优点是能够节约能源
C. 利用该流程每生成48 kg氧气,理论上能得到氢气的质量是6 kg
D. 氢气燃烧热值高,产物无污染,是最清洁的能源
答案:
A 解析:$MnFe_{2}O_{(4 - y)}$中$y = 0.5$,反应前后 Mn 的化合价均为 +2 价,氧元素的化合价为 -2 价,根据在化合物中各元素的正、负化合价代数和为 0,设铁元素化合价为$x$,$( + 2)+2x+( - 2)\times(4 - 0.5)=0$,$x = +\frac{5}{2}$,则铁元素化合价之和是 +5,$Fe^{3 + }$与$Fe^{2 + }$的化合价分别是 +3、+2,因此$Fe^{3 + }$与$Fe^{2 + }$的个数比为 1 : 1,A错误;由图可知,该反应过程中的能量来源于太阳能产生的高温,与传统电解法制取氢气相比,该流程的优点是能够节约能源,B正确;由水的化学式$H_{2}O$可知,其中氢元素与氧元素的质量比为 2 : 16 = 1 : 8,根据反应前后元素质量不变,所以该反应中每生成 48 kg $O_{2}$,理论上能得到$48\ kg\times\frac{1}{8}=6\ kg$氢气,C正确;氢气燃烧热值高,氢气燃烧产物只有水,无污染,是最清洁的能源,D正确。
二、填空与简答题(本大题包括3小题,共32分)
13.(8分)富含淀粉的谷物、甘薯等可以酿酒。在酿酒过程中淀粉在酶的作用下转化为葡萄糖,葡萄糖发酵为酒精,香甜的酒酿就是利用该原理,用酒曲酶(俗称酒药)制作的。家庭一般制作酒酿的简单流程图如图(注:有机反应化学方程式可用箭头表示):
1kg糯米$\xrightarrow[8 - 10小时]{冷水浸泡}$$\xrightarrow{蒸煮}$熟米饭$\xrightarrow[维持33℃左右]{冷水冲淋解粘}$$\xrightarrow{拌入约10g酒药}$装入陶罐密封$\xrightarrow[保温36小时]{}$酒酿

(1)配平化学方程式:(C₆H₁₀O₅)ₙ(淀粉)+______H₂O$\xrightarrow{淀粉酶}$nC₆H₁₂O₆(葡萄糖)。
(2)如温度、水分等因素控制不当,易导致乳酸量过多而味偏酸,请完成该反应的化学方程式:C₆H₁₂O₆$\xrightarrow{乳化酶}$2______(乳酸)。
(3)成熟的酒酿放置时间越长酒味越浓,因为更多的葡萄糖在酒化酶作用下发酵分解为酒精(C₂H₅OH)和二氧化碳,写出该反应的化学方程式:_____________________。
(4)若用1 kg大米酿米酒,假设其中有0.81 kg 的淀粉全部转化为酒精,则理论上可酿制含酒精质量分数为10% 的米酒______kg[提示:由淀粉转化为酒精 的关系式为(C₆H₁₀O₅)ₙ~2nC₂H₅OH]。
13.(8分)富含淀粉的谷物、甘薯等可以酿酒。在酿酒过程中淀粉在酶的作用下转化为葡萄糖,葡萄糖发酵为酒精,香甜的酒酿就是利用该原理,用酒曲酶(俗称酒药)制作的。家庭一般制作酒酿的简单流程图如图(注:有机反应化学方程式可用箭头表示):
1kg糯米$\xrightarrow[8 - 10小时]{冷水浸泡}$$\xrightarrow{蒸煮}$熟米饭$\xrightarrow[维持33℃左右]{冷水冲淋解粘}$$\xrightarrow{拌入约10g酒药}$装入陶罐密封$\xrightarrow[保温36小时]{}$酒酿

(1)配平化学方程式:(C₆H₁₀O₅)ₙ(淀粉)+______H₂O$\xrightarrow{淀粉酶}$nC₆H₁₂O₆(葡萄糖)。
(2)如温度、水分等因素控制不当,易导致乳酸量过多而味偏酸,请完成该反应的化学方程式:C₆H₁₂O₆$\xrightarrow{乳化酶}$2______(乳酸)。
(3)成熟的酒酿放置时间越长酒味越浓,因为更多的葡萄糖在酒化酶作用下发酵分解为酒精(C₂H₅OH)和二氧化碳,写出该反应的化学方程式:_____________________。
(4)若用1 kg大米酿米酒,假设其中有0.81 kg 的淀粉全部转化为酒精,则理论上可酿制含酒精质量分数为10% 的米酒______kg[提示:由淀粉转化为酒精 的关系式为(C₆H₁₀O₅)ₙ~2nC₂H₅OH]。
答案:
(1)$n$
(2)$C_{3}H_{6}O_{3}$
(3)$C_{6}H_{12}O_{6}\xlongequal{酒化酶}2C_{2}H_{5}OH + 2CO_{2}\uparrow$
(4)4.6
(1)$n$
(2)$C_{3}H_{6}O_{3}$
(3)$C_{6}H_{12}O_{6}\xlongequal{酒化酶}2C_{2}H_{5}OH + 2CO_{2}\uparrow$
(4)4.6
查看更多完整答案,请扫码查看


