第17页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
7.(2024·盐城期末)两个烧杯中分别盛装X、Y的饱和溶液,两支试管中分别装有NaOH和NH₄NO₃固体,向两支试管中分别滴加适量水,现象如图1所示,结合图2判断下列说法正确的是 ( )

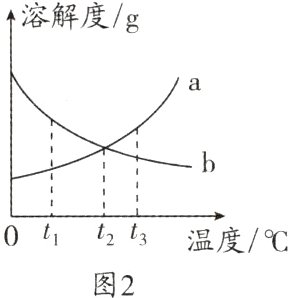
A. Y的溶解度曲线为b曲线
B. X的饱和溶液从t₂℃降温到t₁℃,仍为饱和溶液
C. 降温可使X的饱和溶液变浑浊
D. t₃℃时,X、Y的饱和溶液质量相等,则溶剂质量:X > Y


A. Y的溶解度曲线为b曲线
B. X的饱和溶液从t₂℃降温到t₁℃,仍为饱和溶液
C. 降温可使X的饱和溶液变浑浊
D. t₃℃时,X、Y的饱和溶液质量相等,则溶剂质量:X > Y
答案:
D 解析:氢氧化钠固体溶于水时剧烈放热,而硝酸铵固体溶于水时吸热,故X的饱和溶液在升温时析出溶质,而Y的饱和溶液在降温时析出溶质,则X的溶解度随温度的升高而降低,而Y的溶解度随温度的降低而降低,故Y的溶解度曲线为a,X的溶解度曲线为b,A错误;X的溶解度随温度的降低而升高,故X的饱和溶液从t₂℃降温到t₁℃,变成不饱和溶液,B错误;氢氧化钠固体溶解时剧烈放热,这时X 的饱和溶液变浑浊,故升温可使X的饱和溶液变浑浊,C错误;Y的溶解度曲线为a,X的溶解度曲线为b,故t₃℃时X的溶解度小于Y的溶解度,即此温度下X饱和溶液的溶质质量分数小于Y饱和溶液的溶质质量分数,则当X、Y的饱和溶液质量相等,其溶剂质量:X>Y,D正确。
8. 某温度下,称取不同质量的无水固体M、N溶解在一定质量的水中,分别形成饱和溶液(固体均不与水反应)。其中水的质量x与所溶解固体质量y的关系如图中直线lₘ、lₙ所示。下列说法错误的是 ( )
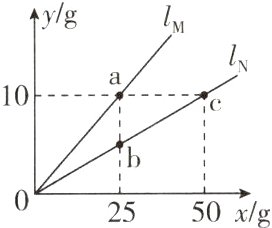
A. 该温度下,两种物质的溶解度大小:M > N
B. 该温度下,物质N饱和溶液的溶质质量分数为20%
C. 加入固体M可实现M溶液由b点向a点转化
D. a、b、c三点对应的溶液中,溶质质量分数:a > b = c

A. 该温度下,两种物质的溶解度大小:M > N
B. 该温度下,物质N饱和溶液的溶质质量分数为20%
C. 加入固体M可实现M溶液由b点向a点转化
D. a、b、c三点对应的溶液中,溶质质量分数:a > b = c
答案:
B 解析:由题图知等量的水中溶解的M质量多,故该温度下,两种物质的溶解度大小:M>N,A说法正确;该温度下,50g水中最多溶解10g物质N,其饱和溶液的溶质质量分数为$\frac{10g}{50g+10g}$×100%≈16.7%<20%,B说法错误;该温度下,b点是M的不饱和溶液,a点是M的饱和溶液,加入固体M可实现M溶液由b点向a点转化,C说法正确;a、b两点对应溶液中,溶剂质量都为25g,a点溶液中的溶质质量大于b点溶液中的溶质质量,故a点溶液的溶质质量分数大于b点溶液的溶质质量分数,b、c两点对应溶液都为该温度下N的饱和溶液,溶质质量分数相等,故a、b、c三点对应的溶液中,溶质质量分数:a>b=c,D说法正确。
9. 新题型(2023·大庆)已知硝酸钾的溶解度(S)、饱和NaCl溶液中溶质的质量分数(w%)与温度的关系如图所示。下列说法正确的是 ( )
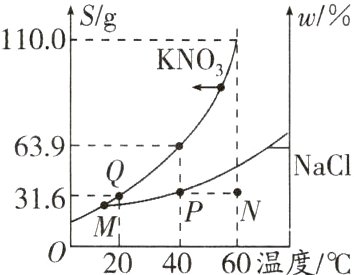
A. M点表示硝酸钾和氯化钠的溶解度相同
B. 20℃时,饱和KNO₃溶液中溶质的质量分数为31.6%
C. 20℃时,100 g 15.8%的KNO₃溶液蒸发掉30 g水变为饱和溶液
D. 将N点的NaCl溶液降温至40℃,N点转化为P点

A. M点表示硝酸钾和氯化钠的溶解度相同
B. 20℃时,饱和KNO₃溶液中溶质的质量分数为31.6%
C. 20℃时,100 g 15.8%的KNO₃溶液蒸发掉30 g水变为饱和溶液
D. 将N点的NaCl溶液降温至40℃,N点转化为P点
答案:
D 解析:M点是硝酸钾的溶解度曲线和饱和NaCl溶液中溶质的质量分数曲线的交点,M点时硝酸钾的溶解度和饱和NaCl溶液中溶质的质量分数的数值相等,饱和溶液中溶质质量分数=$\frac{溶解度}{溶解度 + 100g}$×100%,M点时硝酸钾的溶解度小于氯化钠的溶解度,A错误;20℃时,硝酸钾的溶解度为31.6g,则20℃时,饱和KNO₃溶液中溶质的质量分数为$\frac{31.6g}{31.6g+100g}$×100%<31.6%,B错误;20℃时,100g15.8%的KNO₃溶液中含硝酸钾的质量为100g×15.8%=15.8g,含水的质量为100g−15.8g=84.2g;蒸发掉30g水,溶液中含水的质量为84.2g−30g=54.2g,而20℃时,完全溶解15.8g 硝酸钾形成饱和溶液需要50g水,则溶液仍是不饱和溶液,C错误;N点的NaCl 溶液中含有31.6g溶质,将N点的NaCl 溶液降温至40℃,N点转化为P点,D正确。
10. 化学兴趣小组探究碳酸氢钠、氯化钾、氯化钠和氯化铵的溶解性时,查阅资料如下:
表1 物质在不同温度时的溶解度

表2 溶解度的相对大小(20℃)

请回答下列问题:
(1)10℃时,NaCl的溶解度为______。
(2)根据20℃时上述四种物质的溶解度,判断其中属于“可溶”的物质是______。
(3)将30℃时上述四种物质的饱和溶液各a g分别降温到0℃,析出固体质量最大的物质是______。
(4)20℃时,将氯化钠和氯化铵各m g分别放入两只烧杯中,再分别加入n g水,充分搅拌。下列说法正确的是______(填字母)。
A. 若两只烧杯中均无固体剩余,则所得氯化铵溶液一定是不饱和溶液
B. 若所得溶液中只有一种是饱和溶液,则0.36n≤m≤0.372n
表1 物质在不同温度时的溶解度

表2 溶解度的相对大小(20℃)

请回答下列问题:
(1)10℃时,NaCl的溶解度为______。
(2)根据20℃时上述四种物质的溶解度,判断其中属于“可溶”的物质是______。
(3)将30℃时上述四种物质的饱和溶液各a g分别降温到0℃,析出固体质量最大的物质是______。
(4)20℃时,将氯化钠和氯化铵各m g分别放入两只烧杯中,再分别加入n g水,充分搅拌。下列说法正确的是______(填字母)。
A. 若两只烧杯中均无固体剩余,则所得氯化铵溶液一定是不饱和溶液
B. 若所得溶液中只有一种是饱和溶液,则0.36n≤m≤0.372n
答案:
(1)35.8g
(2)碳酸氢钠(或NaHCO₃)
(3)氯化铵(或NH₄Cl)
(4)A
解析:
(1)由表1知,10℃时,NaCl的溶解度为35.8g。
(2)20℃时,固体物质的溶解度为1~10g为可溶,由表1 可知,20℃时,NaHCO₃的溶解度为9.6g,为可溶。
(3)由表1可知,0~30℃氯化铵的溶解度受温度影响最大,所以将30℃时题述四种物质的饱和溶液各ag分别降温到0℃,析出固体质量最大的物质是NH₄Cl。
(4)20℃时,氯化铵的溶解度比氯化钠的溶解度大,若两只烧杯中均无固体剩余,则所得氯化铵溶液一定是不饱和溶液,A正确;20℃时,氯化铵的溶解度为37.2g,氯化钠的溶解度为36.0g,若所得溶液中只有一种是饱和溶液,则饱和溶液一定是氯化钠,氯化铵不饱和,则0.36n≤m<0.372n,B错误;故选A。
(1)35.8g
(2)碳酸氢钠(或NaHCO₃)
(3)氯化铵(或NH₄Cl)
(4)A
解析:
(1)由表1知,10℃时,NaCl的溶解度为35.8g。
(2)20℃时,固体物质的溶解度为1~10g为可溶,由表1 可知,20℃时,NaHCO₃的溶解度为9.6g,为可溶。
(3)由表1可知,0~30℃氯化铵的溶解度受温度影响最大,所以将30℃时题述四种物质的饱和溶液各ag分别降温到0℃,析出固体质量最大的物质是NH₄Cl。
(4)20℃时,氯化铵的溶解度比氯化钠的溶解度大,若两只烧杯中均无固体剩余,则所得氯化铵溶液一定是不饱和溶液,A正确;20℃时,氯化铵的溶解度为37.2g,氯化钠的溶解度为36.0g,若所得溶液中只有一种是饱和溶液,则饱和溶液一定是氯化钠,氯化铵不饱和,则0.36n≤m<0.372n,B错误;故选A。
查看更多完整答案,请扫码查看


