2026年高考一线课时练习高中化学必修第一册通用版江苏专版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年高考一线课时练习高中化学必修第一册通用版江苏专版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第50页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
3. 下列氧化还原反应方程式表示的变化过程正确的是 (
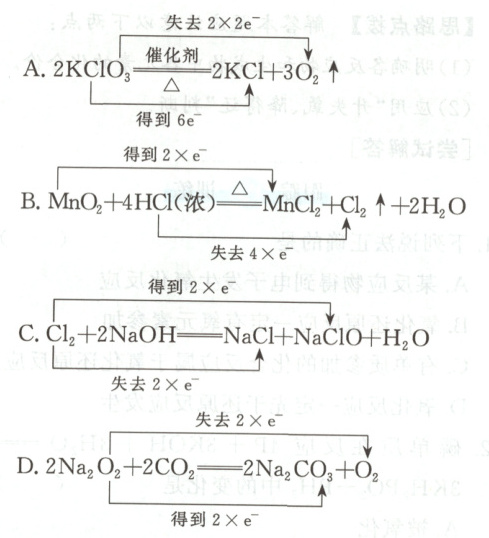
D
)
答案:
3.D A中得失电子数目不相等,不正确;B中得失电子总数也不相等,不正确;C中Cl₂失去电子生成NaClO,Cl₂得到电子生成NaCl,且得失数目也错误,不正确。
1. 下列物质的用途,利用氧化还原反应的是 (
A.用氯气消毒浴池
B.用稀盐酸除去热水瓶胆壁上的水垢(主要成分是$\mathrm{CaCO}_3$)
C.用食盐腌制食物
D.用小苏打治疗胃酸过多
A
)A.用氯气消毒浴池
B.用稀盐酸除去热水瓶胆壁上的水垢(主要成分是$\mathrm{CaCO}_3$)
C.用食盐腌制食物
D.用小苏打治疗胃酸过多
答案:
1.A 用氯气消毒浴池,主要是由于氯气与水反应生成的次氯酸的强氧化性具有杀菌消毒的作用,所以主要发生的是氧化还原反应,A符合题意。
2. 下列变化过程中,属于还原反应的是 (
A.$\mathrm{HCl} \xrightarrow{} \mathrm{Cl}_2$
B.$\mathrm{Na} \xrightarrow{} \mathrm{Na}^+$
C.$\mathrm{CO} \xrightarrow{} \mathrm{CO}_2$
D.$\mathrm{Fe}^{3+} \xrightarrow{} \mathrm{Fe}$
D
)A.$\mathrm{HCl} \xrightarrow{} \mathrm{Cl}_2$
B.$\mathrm{Na} \xrightarrow{} \mathrm{Na}^+$
C.$\mathrm{CO} \xrightarrow{} \mathrm{CO}_2$
D.$\mathrm{Fe}^{3+} \xrightarrow{} \mathrm{Fe}$
答案:
2.D 还原反应就是物质得电子、元素化合价降低的反应。
3. (1) 分析下列反应的化学方程式,是氧化还原反应的用双线桥法标出电子转移的方向和数目,指出被氧化和被还原的元素。
①$2\mathrm{Na} + \mathrm{Cl}_2 \xlongequal{} 2\mathrm{NaCl}$;
②$\mathrm{NaOH} + \mathrm{HCl} \xlongequal{} \mathrm{NaCl} +$
(2) 分析下列反应的化学方程式,是氧化还原反应的用单线桥法标出电子转移的方向和数目。
①$\mathrm{BaCl}_2 + \mathrm{Na}_2\mathrm{SO}_4 \xlongequal{} \mathrm{BaSO}_4 \downarrow + 2\mathrm{NaCl}$;
②$\mathrm{Fe} + 2\mathrm{HCl} \xlongequal{} \mathrm{FeCl}_2 +$$\mathrm{H}_2 \uparrow$。
①$2\mathrm{Na} + \mathrm{Cl}_2 \xlongequal{} 2\mathrm{NaCl}$;
②$\mathrm{NaOH} + \mathrm{HCl} \xlongequal{} \mathrm{NaCl} +$
非氧化还原反应
$\mathrm{H}_2\mathrm{O}$。(2) 分析下列反应的化学方程式,是氧化还原反应的用单线桥法标出电子转移的方向和数目。
①$\mathrm{BaCl}_2 + \mathrm{Na}_2\mathrm{SO}_4 \xlongequal{} \mathrm{BaSO}_4 \downarrow + 2\mathrm{NaCl}$;
非氧化还原反应
②$\mathrm{Fe} + 2\mathrm{HCl} \xlongequal{} \mathrm{FeCl}_2 +$$\mathrm{H}_2 \uparrow$。
答案:
3.解析:首先分析各个反应中元素的化合价的变化,根据化合价升高的元素,失去电子,被氧化;化合价降低的元素,得到电子,被还原;用箭头标出电子转移的情况时,要注意单、双线桥的表示方法的特点及各自的注意事项。
答案:
(1)①2Na+Cl₂=2NaCl
②非氧化还原反应
(2)①非氧化还原反应
②Fe+2HCl=FeCl₂+H₂↑
答案:
(1)①2Na+Cl₂=2NaCl
②非氧化还原反应
(2)①非氧化还原反应
②Fe+2HCl=FeCl₂+H₂↑
4. 已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下:$3\mathrm{Cu} + 8\mathrm{HNO}_3(稀) \xlongequal{} 3\mathrm{Cu(NO}_3\mathrm{)}_2 + 2\mathrm{NO} \uparrow + 4\mathrm{H}_2\mathrm{O}$
(1)被氧化的元素是$\underline{\underline{\mathrm{Cu}}}$,被还原的元素是$\underline{\underline{\mathrm{N}}}$,氧化剂是$\underline{\underline{\mathrm{HNO}_3}}$,还原剂是$\underline{\underline{\mathrm{Cu}}}$,氧化产物为$\underline{\underline{\mathrm{Cu(NO}_3\mathrm{)}_2}}$,还原产物为$\underline{\underline{\mathrm{NO}}}$。
(2) 用双线桥法表示反应电子得失的方向和数目:$\underline{\underline{略}}$。
(3) 用单线桥法表示反应电子得失的方向和数目:$\underline{\underline{略}}$。
(1)被氧化的元素是$\underline{\underline{\mathrm{Cu}}}$,被还原的元素是$\underline{\underline{\mathrm{N}}}$,氧化剂是$\underline{\underline{\mathrm{HNO}_3}}$,还原剂是$\underline{\underline{\mathrm{Cu}}}$,氧化产物为$\underline{\underline{\mathrm{Cu(NO}_3\mathrm{)}_2}}$,还原产物为$\underline{\underline{\mathrm{NO}}}$。
(2) 用双线桥法表示反应电子得失的方向和数目:$\underline{\underline{略}}$。
(3) 用单线桥法表示反应电子得失的方向和数目:$\underline{\underline{略}}$。
答案:
4.解析:由化学方程式可知铜元素化合价升高,从0价变为+2价,被氧化;氮元素化合价降低,从+5价变为+2 价,被还原;故Cu发生氧化反应,HNO₃发生还原反应。
参考答案答案:
(1)Cu N HNO₃ Cu Cu(NO₃)₂ NO

失去3×2e⁻
(2)3Cu+8HNO₃(稀)=3Cu(NO₃)₂+2NO↑+4H₂O
得到2×3e⁻
(3)3Cu+8HNO₃(稀)=3Cu(NO₃)₂+2NO↑+4H₂O
4.解析:由化学方程式可知铜元素化合价升高,从0价变为+2价,被氧化;氮元素化合价降低,从+5价变为+2 价,被还原;故Cu发生氧化反应,HNO₃发生还原反应。
参考答案答案:
(1)Cu N HNO₃ Cu Cu(NO₃)₂ NO

失去3×2e⁻
(2)3Cu+8HNO₃(稀)=3Cu(NO₃)₂+2NO↑+4H₂O
得到2×3e⁻
(3)3Cu+8HNO₃(稀)=3Cu(NO₃)₂+2NO↑+4H₂O
5. 关于下列转化过程分析不正确的是 (
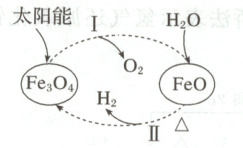
A.$\mathrm{Fe}_3\mathrm{O}_4$ 中 $\mathrm{Fe}$ 元素的化合价为 +2、+3 价
B.过程Ⅰ中每消耗 $58\mathrm{g}$ $\mathrm{Fe}_3\mathrm{O}_4$ 转移 $1\mathrm{mol}$ 电子
C.过程Ⅱ的化学方程式为 $3\mathrm{FeO} + \mathrm{H}_2\mathrm{O} \xlongequal{\triangle} \mathrm{Fe}_3\mathrm{O}_4 + \mathrm{H}_2 \uparrow$
D.该过程总反应为 $2\mathrm{H}_2\mathrm{O} \xlongequal{} \mathrm{O}_2 \uparrow + 2\mathrm{H}_2 \uparrow$
提醒:请完成训练(十五)
B
)
A.$\mathrm{Fe}_3\mathrm{O}_4$ 中 $\mathrm{Fe}$ 元素的化合价为 +2、+3 价
B.过程Ⅰ中每消耗 $58\mathrm{g}$ $\mathrm{Fe}_3\mathrm{O}_4$ 转移 $1\mathrm{mol}$ 电子
C.过程Ⅱ的化学方程式为 $3\mathrm{FeO} + \mathrm{H}_2\mathrm{O} \xlongequal{\triangle} \mathrm{Fe}_3\mathrm{O}_4 + \mathrm{H}_2 \uparrow$
D.该过程总反应为 $2\mathrm{H}_2\mathrm{O} \xlongequal{} \mathrm{O}_2 \uparrow + 2\mathrm{H}_2 \uparrow$
提醒:请完成训练(十五)
答案:
5.B
查看更多完整答案,请扫码查看


