2026年高考一线课时练习高中化学必修第一册通用版江苏专版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年高考一线课时练习高中化学必修第一册通用版江苏专版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第5页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
下列物质的转化中,不能通过一步化学反应实现的是 (
A.${Fe \to Fe3O4}$
B.${C \to CO2}$
C.${CaO \to Ca(OH)2}$
D.${S \to SO3}$
D
)A.${Fe \to Fe3O4}$
B.${C \to CO2}$
C.${CaO \to Ca(OH)2}$
D.${S \to SO3}$
答案:
D
1. 化合价变化的分析
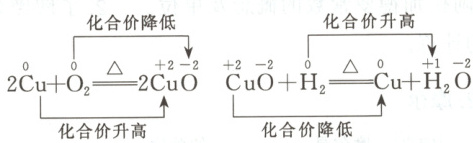
$\begin{array}{c} 化合价降低\\ 2{Cu} + {O2} \xlongequal{\triangle} 2{CuO}\\ 化合价升高\\ \end{array}$ $\begin{array}{c} 化合价升高\\ {CuO} + {H2} \xlongequal{\triangle} {Cu} + {H2O}\\ 化合价降低\\ \end{array}$

$\begin{array}{c} 化合价降低\\ 2{Cu} + {O2} \xlongequal{\triangle} 2{CuO}\\ 化合价升高\\ \end{array}$ $\begin{array}{c} 化合价升高\\ {CuO} + {H2} \xlongequal{\triangle} {Cu} + {H2O}\\ 化合价降低\\ \end{array}$
答案:
在反应 $2Cu + O_2 \xlongequal{\triangle} 2CuO$ 中:
铜($Cu$)的化合价从 0 升高到 +2,氧($O$)的化合价从 0 降低到 -2。
在反应 $CuO + H_2 \xlongequal{\triangle} Cu + H_2O$ 中:
氢($H$)的化合价从 0 升高到 +1,铜($Cu$)的化合价从 +2 降低到 0。
铜($Cu$)的化合价从 0 升高到 +2,氧($O$)的化合价从 0 降低到 -2。
在反应 $CuO + H_2 \xlongequal{\triangle} Cu + H_2O$ 中:
氢($H$)的化合价从 0 升高到 +1,铜($Cu$)的化合价从 +2 降低到 0。
2. 从化合价变化的角度认识氧化反应和还原反应
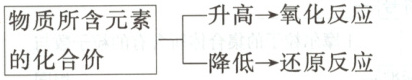
$物质所含元素的化合价$ $\begin{cases} 升高 \to 氧化反应\\降低 \to 还原反应 \end{cases}$

$物质所含元素的化合价$ $\begin{cases} 升高 \to 氧化反应\\降低 \to 还原反应 \end{cases}$
答案:
在化学反应中,从化合价变化的角度可以这样认识氧化反应和还原反应:
当物质所含元素的化合价升高时,该物质发生氧化反应;
当物质所含元素的化合价降低时,该物质发生还原反应。
当物质所含元素的化合价升高时,该物质发生氧化反应;
当物质所含元素的化合价降低时,该物质发生还原反应。
3. 概念
有元素化合价发生变化的反应称为氧化还原反应。
有元素化合价发生变化的反应称为氧化还原反应。
答案:
①氧化还原反应的特征是有元素化合价发生变化。
②判断一个反应是否为氧化还原反应,关键看反应前后是否有元素的化合价改变。若有,则为氧化还原反应;若没有,则不是氧化还原反应。
②判断一个反应是否为氧化还原反应,关键看反应前后是否有元素的化合价改变。若有,则为氧化还原反应;若没有,则不是氧化还原反应。
4. 氧化还原反应与四种基本反应类型之间的关系
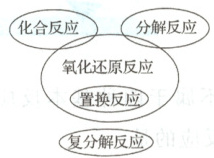
(1)置换反应一定是氧化还原反应。
(2)复分解反应一定不是氧化还原反应。
(3)有单质参加的化合反应是氧化还原反应。
(4)有单质生成的分解反应是氧化还原反应。
[想想] 有单质参加的反应一定是氧化还原反应吗?
[我的感悟]
_
[名师点睛]
(1)在氧化还原反应中,并不是所有元素的化合价都发生改变。
(2)并非只有得氧、失氧的反应才是氧化还原反应。凡是有元素化合价升降的化学反应都是氧化还原反应。
(3)化合价变化是氧化还原反应的外在特征,是判断氧化还原反应的依据。

(1)置换反应一定是氧化还原反应。
(2)复分解反应一定不是氧化还原反应。
(3)有单质参加的化合反应是氧化还原反应。
(4)有单质生成的分解反应是氧化还原反应。
[想想] 有单质参加的反应一定是氧化还原反应吗?
[我的感悟]
_
[名师点睛]
(1)在氧化还原反应中,并不是所有元素的化合价都发生改变。
(2)并非只有得氧、失氧的反应才是氧化还原反应。凡是有元素化合价升降的化学反应都是氧化还原反应。
(3)化合价变化是氧化还原反应的外在特征,是判断氧化还原反应的依据。
答案:
提示:不一定,有单质参加或生成的反应不一定是氧化还原反应。如同素异形体之间的相互转化(如$3O₂\stackrel{放电}{⇌}2O₃)$不属于氧化还原反应。
判断下列反应是否属于氧化还原反应。(填“是”或“否”)
(1)${2Na + Cl2 \xlongequal{点燃} 2NaCl}$ ()
(2)${Fe + CuSO4 = FeSO4 + Cu}$ ()
(3)${2HgO \xlongequal{\triangle} 2Hg + O2 ^}$ ()
(4)${NH4NO3 \xlongequal{\triangle} N2O ^ + 2H2O}$ ()
(5)${CaO + H2O = Ca(OH)2}$ ()
(6)${3Fe + 2O2 \xlongequal{点燃} Fe3O4}$ ()
(7)${BaCl2 + H2SO4 = BaSO4 v + 2HCl}$ ()
(8)${CaCO3 \xlongequal{高温} CaO + CO2 ^}$ ()
[尝试解答]
(1)${2Na + Cl2 \xlongequal{点燃} 2NaCl}$ ()
(2)${Fe + CuSO4 = FeSO4 + Cu}$ ()
(3)${2HgO \xlongequal{\triangle} 2Hg + O2 ^}$ ()
(4)${NH4NO3 \xlongequal{\triangle} N2O ^ + 2H2O}$ ()
(5)${CaO + H2O = Ca(OH)2}$ ()
(6)${3Fe + 2O2 \xlongequal{点燃} Fe3O4}$ ()
(7)${BaCl2 + H2SO4 = BaSO4 v + 2HCl}$ ()
(8)${CaCO3 \xlongequal{高温} CaO + CO2 ^}$ ()
[尝试解答]
答案:
答案:
(1)是
(2)是
(3)是
(4)是
(5)否
(6)是
(7)否
(8)否
(1)是
(2)是
(3)是
(4)是
(5)否
(6)是
(7)否
(8)否
查看更多完整答案,请扫码查看


