2025年世纪金榜新视野暑假作业高一化学
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年世纪金榜新视野暑假作业高一化学 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
8.如图所示,利用培养皿探究$NH_3$的性质。实验时向NaOH固体上滴几滴浓氨水能产生氨气,立即将另一表面皿扣在上面。下列对实验现象所进行的解释正确的是 (
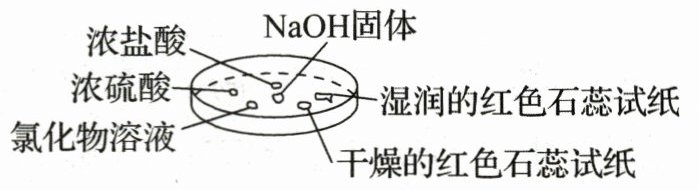
A.浓盐酸附近产生白烟,是因为$NH_3$与HCl反应生成$NH_4Cl$固体
B.浓硫酸附近无现象,说明$NH_3$与浓硫酸不反应
C.氯化物溶液变浑浊,则该溶液一定是$AlCl_3$溶液
D.干燥的红色石蕊试纸不变色,湿润的红色石蕊试纸变蓝,说明$NH_3$是可溶性碱
A
)
A.浓盐酸附近产生白烟,是因为$NH_3$与HCl反应生成$NH_4Cl$固体
B.浓硫酸附近无现象,说明$NH_3$与浓硫酸不反应
C.氯化物溶液变浑浊,则该溶液一定是$AlCl_3$溶液
D.干燥的红色石蕊试纸不变色,湿润的红色石蕊试纸变蓝,说明$NH_3$是可溶性碱
答案:
A
9.在实验室采用如图装置制备气体,合理的是 (
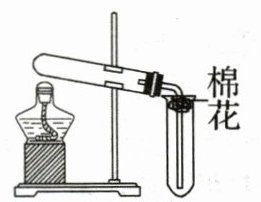
|选项|化学试剂|制备的气体|
|A|$Ca(OH)_2+NH_4Cl$|$NH_3$|
|B|$MnO_2+HCl($浓)|$Cl_2$|
|C|$MnO_2+KClO_3$|$O_2$|
|D|$NaCl+H_2SO_4($浓)|HCl|
C
)
|选项|化学试剂|制备的气体|
|A|$Ca(OH)_2+NH_4Cl$|$NH_3$|
|B|$MnO_2+HCl($浓)|$Cl_2$|
|C|$MnO_2+KClO_3$|$O_2$|
|D|$NaCl+H_2SO_4($浓)|HCl|
答案:
C
10.为验证铜与稀硝酸反应的还原产物是NO而不是$NO_2。$某同学设计了如图所示的装置,下列叙述错误的是 (
A.应先打开活塞,再从U形管右侧加入稀硝酸
B.加入的稀硝酸应充满U形管左侧
C.关闭活塞后铜丝会全部溶解
D.反应停止后打开活塞,气体变成红棕色
C
)A.应先打开活塞,再从U形管右侧加入稀硝酸
B.加入的稀硝酸应充满U形管左侧
C.关闭活塞后铜丝会全部溶解
D.反应停止后打开活塞,气体变成红棕色
答案:
C
11.喷泉实验装置如图所示。应用下列各组气体—溶液,能出现喷泉现象的是 (
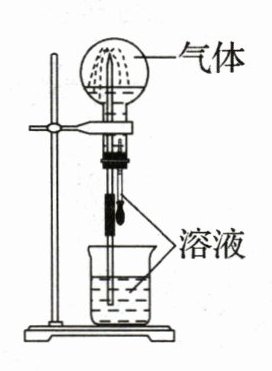
|选项|气体|溶液|
|A|$H_2S$|稀盐酸|
|B|HCl|稀氨水|
|C|NO|稀$H_2SO_4$|
|D|$CO_2$|饱和$NaHCO_3$溶液|
B
)
|选项|气体|溶液|
|A|$H_2S$|稀盐酸|
|B|HCl|稀氨水|
|C|NO|稀$H_2SO_4$|
|D|$CO_2$|饱和$NaHCO_3$溶液|
答案:
B
12.某氮的氧化物和一氧化碳在催化剂的作用下充分反应,生成氮气和二氧化碳。若测得氮气和二氧化碳的物质的量之比为1∶2,则该氮的氧化物是 (
A.$N_2O $
B.$NO $
C.$NO_2 $
D.$N_2O_5$
B
)A.$N_2O $
B.$NO $
C.$NO_2 $
D.$N_2O_5$
答案:
B 设氮的氧化物化学式为 $ N_xO_y $,则 $ N_xO_y + 2CO \rightarrow N_2 + 2CO_2 $,则 $ x : y = 1 : 1 $,即为 $ NO $。
13.对$3NO_2+H_2O= 2HNO_3+NO$反应的下列说法正确的是 (
A.氧化剂与还原剂的质量比为1∶2
B.氧化产物与还原产物的物质的量之比为1∶2
$C.NO_2$是氧化剂$,H_2O$是还原剂
D.在反应中若有$6 mol NO_2$参与反应时,有3 mol电子发生转移
A
)A.氧化剂与还原剂的质量比为1∶2
B.氧化产物与还原产物的物质的量之比为1∶2
$C.NO_2$是氧化剂$,H_2O$是还原剂
D.在反应中若有$6 mol NO_2$参与反应时,有3 mol电子发生转移
答案:
A
14.如图所示,向一定量的铁粉中加入一定体积$12 mol·L⁻^1$的$HNO_3,$加热充分反应后,下列微粒在体系中一定大量存在的是 (
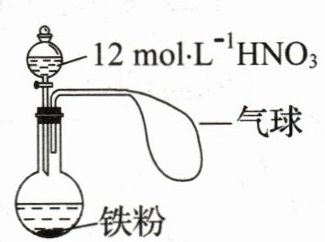
$①NO_3⁻ ②Fe^3⁺ ③H⁺ ④NO ⑤NO_2$
A.①
B.①⑤
C.②④⑤
D.①②③⑤
B
)
$①NO_3⁻ ②Fe^3⁺ ③H⁺ ④NO ⑤NO_2$
A.①
B.①⑤
C.②④⑤
D.①②③⑤
答案:
B
15.把0.5 L含硫酸铵和硝酸铵的混合液分成两等份,一份用3 mol氢氧化钠刚好把氨全部赶出,另一份与1 mol氯化钡恰好完全反应,由此可知原溶液中$NO_3⁻$的物质的量浓度为 (
$A.1 mol·L⁻^1$
$B.2 mol·L⁻^1 $
$C.4 mol·L⁻^1 $
$D.0.5 mol·L⁻^1$
C
)$A.1 mol·L⁻^1$
$B.2 mol·L⁻^1 $
$C.4 mol·L⁻^1 $
$D.0.5 mol·L⁻^1$
答案:
C
查看更多完整答案,请扫码查看


