2025年世纪金榜新视野暑假作业高一化学
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年世纪金榜新视野暑假作业高一化学 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
16. (14 分)(1)$ \text{NaBH}_4(\text{s}) $与水(l)反应生成 $ \text{NaBO}_2(\text{s}) $和氢气(g),在 $ 25 ^\circ \text{C} $,101 kPa 下,已知每消耗 $ 3.8 \text{ g} \text{NaBH}_4(\text{s}) $放热 $ 21.6 \text{ kJ} $,该反应的热化学方程式是______。
(2)碳是地球上含量丰富的元素,其氧化物的研究有着重要意义。
①如图是 $ 1 \text{ mol} \text{NO}_2 $和 $ 1 \text{ mol} \text{CO} $反应生成 $ \text{CO}_2 $和 $ \text{NO} $过程中能量变化示意图,写出 $ \text{NO}_2 $和 $ \text{CO} $反应的热化学方程式______。
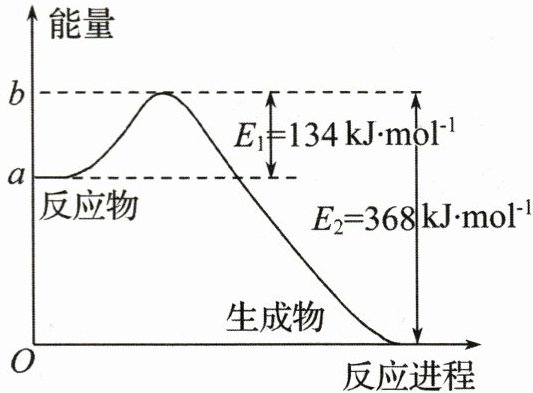
②试在原图基础上画出加入正催化剂后该反应在反应过程中的能量变化示意图(进行必要的标注)。
(2)碳是地球上含量丰富的元素,其氧化物的研究有着重要意义。
①如图是 $ 1 \text{ mol} \text{NO}_2 $和 $ 1 \text{ mol} \text{CO} $反应生成 $ \text{CO}_2 $和 $ \text{NO} $过程中能量变化示意图,写出 $ \text{NO}_2 $和 $ \text{CO} $反应的热化学方程式______。

②试在原图基础上画出加入正催化剂后该反应在反应过程中的能量变化示意图(进行必要的标注)。
答案:
(1)$\mathrm{NaBH}_{4}(\mathrm{~s})+2 \mathrm{H}_{2} \mathrm{O}(\mathrm{l})=\mathrm{NaBO}_{2}(\mathrm{~s})+4 \mathrm{H}_{2}(\mathrm{~g})$$\Delta H=-216 \mathrm{~kJ} \cdot \mathrm{mol}^{-1}$
(2)①$\mathrm{NO}_{2}(\mathrm{~g})+\mathrm{CO}(\mathrm{g})=\mathrm{NO}(\mathrm{g})+\mathrm{CO}_{2}(\mathrm{~g})$$\Delta H=-234 \mathrm{~kJ} \cdot \mathrm{mol}^{-1}$
②
(1)$\mathrm{NaBH}_{4}(\mathrm{~s})+2 \mathrm{H}_{2} \mathrm{O}(\mathrm{l})=\mathrm{NaBO}_{2}(\mathrm{~s})+4 \mathrm{H}_{2}(\mathrm{~g})$$\Delta H=-216 \mathrm{~kJ} \cdot \mathrm{mol}^{-1}$
(2)①$\mathrm{NO}_{2}(\mathrm{~g})+\mathrm{CO}(\mathrm{g})=\mathrm{NO}(\mathrm{g})+\mathrm{CO}_{2}(\mathrm{~g})$$\Delta H=-234 \mathrm{~kJ} \cdot \mathrm{mol}^{-1}$
②

17. (16 分)白磷、红磷是磷的两种同素异形体,在空气中燃烧得到磷的氧化物,空气不足时生成 $ \text{P}_4\text{O}_6 $,空气充足时生成 $ \text{P}_4\text{O}_{10} $。
(1)已知 298 K 时白磷、红磷完全燃烧的热化学方程式分别为
$ \text{P}_4(\text{s},\text{白磷}) + 5\text{O}_2(\text{g}) = \text{P}_4\text{O}_{10}(\text{s}) $ $ \Delta H_1 = -2983.2 \text{ kJ} \cdot \text{mol}^{-1} $
$ \text{P(s},\text{红磷}) + \frac{5}{4}\text{O}_2(\text{g}) = \frac{1}{4}\text{P}_4\text{O}_{10}(\text{s}) $ $ \Delta H_2 = -738.5 \text{ kJ} \cdot \text{mol}^{-1} $
则该温度下白磷转化为红磷的热化学方程式为______
(2)已知 298 K 时白磷不完全燃烧的热化学方程式为 $ \text{P}_4(\text{s},\text{白磷}) + 3\text{O}_2(\text{g}) = \text{P}_4\text{O}_6(\text{s}) $ $ \Delta H = -1638 \text{ kJ} \cdot \text{mol}^{-1} $。在某密闭容器中加入 62 g 白磷和 50.4 L 氧气(标准状况),控制条件使之恰好完全反应。则所得到的 $ \text{P}_4\text{O}_{10} $与 $ \text{P}_4\text{O}_6 $的物质的量之比为______
(3)已知白磷和 $ \text{PCl}_3 $的分子结构如图所示,现提供以下化学键的键能($ \text{kJ} \cdot \text{mol}^{-1} $):
$ \text{P} - \text{P} $ 198,$ \text{Cl} - \text{Cl} $ 243,$ \text{P} - \text{Cl} $ 331。
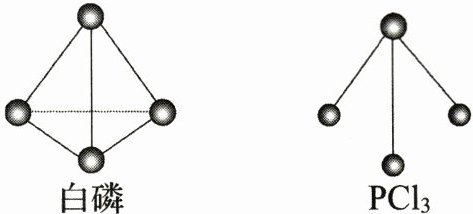
则反应 $ \text{P}_4(\text{s},\text{白磷}) + 6\text{Cl}_2(\text{g}) = 4\text{PCl}_3(\text{s}) $的反应热 $ \Delta H = $______
(1)已知 298 K 时白磷、红磷完全燃烧的热化学方程式分别为
$ \text{P}_4(\text{s},\text{白磷}) + 5\text{O}_2(\text{g}) = \text{P}_4\text{O}_{10}(\text{s}) $ $ \Delta H_1 = -2983.2 \text{ kJ} \cdot \text{mol}^{-1} $
$ \text{P(s},\text{红磷}) + \frac{5}{4}\text{O}_2(\text{g}) = \frac{1}{4}\text{P}_4\text{O}_{10}(\text{s}) $ $ \Delta H_2 = -738.5 \text{ kJ} \cdot \text{mol}^{-1} $
则该温度下白磷转化为红磷的热化学方程式为______
$\mathrm{P}_{4}(\mathrm{~s}$, 白磷$)=4 \mathrm{P}(\mathrm{s}$, 红磷$) \quad \Delta H=-29.2 \mathrm{~kJ} \cdot \mathrm{mol}^{-1}$
。(2)已知 298 K 时白磷不完全燃烧的热化学方程式为 $ \text{P}_4(\text{s},\text{白磷}) + 3\text{O}_2(\text{g}) = \text{P}_4\text{O}_6(\text{s}) $ $ \Delta H = -1638 \text{ kJ} \cdot \text{mol}^{-1} $。在某密闭容器中加入 62 g 白磷和 50.4 L 氧气(标准状况),控制条件使之恰好完全反应。则所得到的 $ \text{P}_4\text{O}_{10} $与 $ \text{P}_4\text{O}_6 $的物质的量之比为______
$3: 1$
,反应过程中放出的热量为______$1323.45 \mathrm{~kJ}$
。(3)已知白磷和 $ \text{PCl}_3 $的分子结构如图所示,现提供以下化学键的键能($ \text{kJ} \cdot \text{mol}^{-1} $):
$ \text{P} - \text{P} $ 198,$ \text{Cl} - \text{Cl} $ 243,$ \text{P} - \text{Cl} $ 331。

则反应 $ \text{P}_4(\text{s},\text{白磷}) + 6\text{Cl}_2(\text{g}) = 4\text{PCl}_3(\text{s}) $的反应热 $ \Delta H = $______
$-1326 \mathrm{~kJ} \cdot \mathrm{mol}^{-1}$
。
答案:
(1)$\mathrm{P}_{4}(\mathrm{~s}$, 白磷$)=4 \mathrm{P}(\mathrm{s}$, 红磷$) \quad \Delta H=-29.2 \mathrm{~kJ} \cdot \mathrm{mol}^{-1}$
(2)$3: 1 \quad 1323.45 \mathrm{~kJ}$
(3)$-1326 \mathrm{~kJ} \cdot \mathrm{mol}^{-1}$
(1)$\mathrm{P}_{4}(\mathrm{~s}$, 白磷$)=4 \mathrm{P}(\mathrm{s}$, 红磷$) \quad \Delta H=-29.2 \mathrm{~kJ} \cdot \mathrm{mol}^{-1}$
(2)$3: 1 \quad 1323.45 \mathrm{~kJ}$
(3)$-1326 \mathrm{~kJ} \cdot \mathrm{mol}^{-1}$
查看更多完整答案,请扫码查看


