2025年世纪金榜新视野暑假作业高一化学
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年世纪金榜新视野暑假作业高一化学 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
6. 实验室进行中和反应反应热测定的实验时除需要大烧杯(500 mL)、小烧杯(100 mL)外,其他所用的仪器和试剂均正确的一组是(
A.$ 0.50 \text{ mol} \cdot \text{L}^{-1} $盐酸,$ 0.50 \text{ mol} \cdot \text{L}^{-1} \text{NaOH} $溶液,100 mL 量筒 1 个
B.$ 0.50 \text{ mol} \cdot \text{L}^{-1} $盐酸,$ 0.50 \text{ mol} \cdot \text{L}^{-1} \text{NaOH} $溶液,100 mL 量筒 2 个
C.$ 0.50 \text{ mol} \cdot \text{L}^{-1} $盐酸,$ 0.50 \text{ mol} \cdot \text{L}^{-1} \text{NaOH} $溶液,50 mL 量筒 1 个
D.$ 0.50 \text{ mol} \cdot \text{L}^{-1} $盐酸,$ 0.55 \text{ mol} \cdot \text{L}^{-1} \text{NaOH} $溶液,50 mL 量筒 2 个
D
)A.$ 0.50 \text{ mol} \cdot \text{L}^{-1} $盐酸,$ 0.50 \text{ mol} \cdot \text{L}^{-1} \text{NaOH} $溶液,100 mL 量筒 1 个
B.$ 0.50 \text{ mol} \cdot \text{L}^{-1} $盐酸,$ 0.50 \text{ mol} \cdot \text{L}^{-1} \text{NaOH} $溶液,100 mL 量筒 2 个
C.$ 0.50 \text{ mol} \cdot \text{L}^{-1} $盐酸,$ 0.50 \text{ mol} \cdot \text{L}^{-1} \text{NaOH} $溶液,50 mL 量筒 1 个
D.$ 0.50 \text{ mol} \cdot \text{L}^{-1} $盐酸,$ 0.55 \text{ mol} \cdot \text{L}^{-1} \text{NaOH} $溶液,50 mL 量筒 2 个
答案:
D
7. 关于化学反应与能量的说法正确的是(
A.任何化学反应都伴随有能量变化
B.$ \Delta H > 0 $表示放热反应,$ \Delta H < 0 $表示吸热反应
C.化学键的断裂会放出能量
D.反应物总能量比生成物总能量高的反应是吸热反应
A
)A.任何化学反应都伴随有能量变化
B.$ \Delta H > 0 $表示放热反应,$ \Delta H < 0 $表示吸热反应
C.化学键的断裂会放出能量
D.反应物总能量比生成物总能量高的反应是吸热反应
答案:
A
8. 依据图判断,下列说法不正确的是(
A.$ 1 \text{ mol} \text{H}_2(\text{g}) $与 $ \frac{1}{2} \text{ mol} \text{O}_2(\text{g}) $所具有的总能量比 $ 1 \text{ mol} \text{H}_2\text{O(g)} $所具有的总能量高
B.$ \text{H}_2\text{O(g)} $生成 $ \text{H}_2\text{O(l)} $时,断键吸收的能量小于成键放出的能量
C.$ 2 \text{ mol} \text{ H(g)} $与 $ 1 \text{ mol} \text{ O(g)} $生成 $ 1 \text{ mol} \text{H}_2\text{O(g)} $所放出的热量是 $ b \text{ kJ} $
D.液态水分解的热化学方程式为 $ 2\text{H}_2\text{O(l)} = 2\text{H}_2(\text{g}) + \text{O}_2(\text{g}) $ $ \Delta H = 2(b + c - a) \text{ kJ} \cdot \text{mol}^{-1} $
B
)A.$ 1 \text{ mol} \text{H}_2(\text{g}) $与 $ \frac{1}{2} \text{ mol} \text{O}_2(\text{g}) $所具有的总能量比 $ 1 \text{ mol} \text{H}_2\text{O(g)} $所具有的总能量高
B.$ \text{H}_2\text{O(g)} $生成 $ \text{H}_2\text{O(l)} $时,断键吸收的能量小于成键放出的能量
C.$ 2 \text{ mol} \text{ H(g)} $与 $ 1 \text{ mol} \text{ O(g)} $生成 $ 1 \text{ mol} \text{H}_2\text{O(g)} $所放出的热量是 $ b \text{ kJ} $
D.液态水分解的热化学方程式为 $ 2\text{H}_2\text{O(l)} = 2\text{H}_2(\text{g}) + \text{O}_2(\text{g}) $ $ \Delta H = 2(b + c - a) \text{ kJ} \cdot \text{mol}^{-1} $
答案:
B
9. 如图所示,某化学变化过程存在三种途径,下列有关说法正确的是(
A.$ \Delta H_1 $一定小于 $ \Delta H $
B.$ \Delta H $一定大于 $ \Delta H_4 + \Delta H_5 $
C.$ \Delta H_1 + \Delta H_2 $可能大于 $ \Delta H_3 + \Delta H_4 + \Delta H_5 $
D.终态→c 的反应热可表示为 $ \Delta H_3 + \Delta H_4 - \Delta H $
D
)A.$ \Delta H_1 $一定小于 $ \Delta H $
B.$ \Delta H $一定大于 $ \Delta H_4 + \Delta H_5 $
C.$ \Delta H_1 + \Delta H_2 $可能大于 $ \Delta H_3 + \Delta H_4 + \Delta H_5 $
D.终态→c 的反应热可表示为 $ \Delta H_3 + \Delta H_4 - \Delta H $
答案:
D
10. 已知:
$ \text{C(s)} + \text{H}_2\text{O(g)} = \text{CO(g)} + \text{H}_2(\text{g}) $ $ \Delta H = a \text{ kJ} \cdot \text{mol}^{-1} $
$ 2\text{C(s)} + \text{O}_2(\text{g}) = 2\text{CO(g)} $ $ \Delta H = -220 \text{ kJ} \cdot \text{mol}^{-1} $
$ \text{H} - \text{H} $、$ \text{O} = \text{O} $和 $ \text{O} - \text{H} $键的键能分别为 $ 436 \text{ kJ} \cdot \text{mol}^{-1} $,$ 496 \text{ kJ} \cdot \text{mol}^{-1} $和 $ 462 \text{ kJ} \cdot \text{mol}^{-1} $。则 $ a $为(
A.-332
B.-118
C.+350
D.+130
$ \text{C(s)} + \text{H}_2\text{O(g)} = \text{CO(g)} + \text{H}_2(\text{g}) $ $ \Delta H = a \text{ kJ} \cdot \text{mol}^{-1} $
$ 2\text{C(s)} + \text{O}_2(\text{g}) = 2\text{CO(g)} $ $ \Delta H = -220 \text{ kJ} \cdot \text{mol}^{-1} $
$ \text{H} - \text{H} $、$ \text{O} = \text{O} $和 $ \text{O} - \text{H} $键的键能分别为 $ 436 \text{ kJ} \cdot \text{mol}^{-1} $,$ 496 \text{ kJ} \cdot \text{mol}^{-1} $和 $ 462 \text{ kJ} \cdot \text{mol}^{-1} $。则 $ a $为(
D
)A.-332
B.-118
C.+350
D.+130
答案:
D
11. 甲醇质子交换膜在燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①$ \text{CH}_3\text{OH(g)} + \text{H}_2\text{O(g)} = \text{CO}_2(\text{g}) + 3\text{H}_2(\text{g}) $ $ \Delta H_1 = +49.0 \text{ kJ} \cdot \text{mol}^{-1} $
②$ \text{CH}_3\text{OH(g)} + \frac{1}{2}\text{O}_2(\text{g}) = \text{CO}_2(\text{g}) + 2\text{H}_2(\text{g}) $ $ \Delta H_2 = -192.9 \text{ kJ} \cdot \text{mol}^{-1} $
根据上述反应,下列说法正确的是(
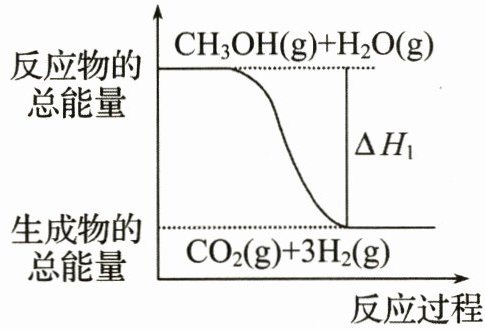
A.反应①中的能量变化如图所示
B.$ \text{CH}_3\text{OH} $转变成 $ \text{H}_2 $的过程一定要吸收能量
C.$ 1 \text{ mol} \text{CH}_3\text{OH} $充分燃烧放出的热量为 $ 192.9 \text{ kJ} $
D.可推知 $ 2\text{H}_2(\text{g}) + \text{O}_2(\text{g}) = 2\text{H}_2\text{O(g)} $ $ \Delta H = -483.8 \text{ kJ} \cdot \text{mol}^{-1} $
①$ \text{CH}_3\text{OH(g)} + \text{H}_2\text{O(g)} = \text{CO}_2(\text{g}) + 3\text{H}_2(\text{g}) $ $ \Delta H_1 = +49.0 \text{ kJ} \cdot \text{mol}^{-1} $
②$ \text{CH}_3\text{OH(g)} + \frac{1}{2}\text{O}_2(\text{g}) = \text{CO}_2(\text{g}) + 2\text{H}_2(\text{g}) $ $ \Delta H_2 = -192.9 \text{ kJ} \cdot \text{mol}^{-1} $
根据上述反应,下列说法正确的是(
D
)
A.反应①中的能量变化如图所示
B.$ \text{CH}_3\text{OH} $转变成 $ \text{H}_2 $的过程一定要吸收能量
C.$ 1 \text{ mol} \text{CH}_3\text{OH} $充分燃烧放出的热量为 $ 192.9 \text{ kJ} $
D.可推知 $ 2\text{H}_2(\text{g}) + \text{O}_2(\text{g}) = 2\text{H}_2\text{O(g)} $ $ \Delta H = -483.8 \text{ kJ} \cdot \text{mol}^{-1} $
答案:
D
查看更多完整答案,请扫码查看


