第12页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
11. 铜是重要的金属资源,它对于改善人类生活、促进人类文明起着重要作用。
(1)铜的认识:生活中常用铜做导线,体现了铜的延展性和
(2)铜的加工:青铜是金属冶铸史上最早的合金,其主要成分是铜和锡。表中的A和B分别表示铜和青铜中的一种。《吕氏春秋》记载:“金(铜)柔锡柔,合两柔则刚。”据此判断A是
|物质|A|B|
|--|--|--|
|硬度|2.5~3|5~6.6|
注:硬度以金刚石的硬度为10作标准,1表示很软,10表示很硬。
(3)铜的回收:某工厂的废水经预处理后得到含$ FeSO_4 $和$ CuSO_4 $的溶液。为了减少污染并促进废物利用,工厂设计以下流程回收Cu和$ FeSO_4 $。
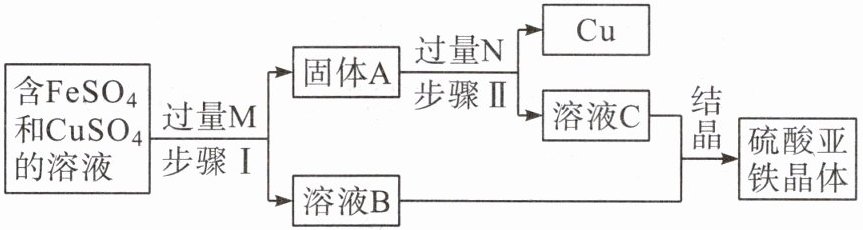
①步骤Ⅰ中发生反应的化学方程式为
②溶液C中溶解的物质是
(1)铜的认识:生活中常用铜做导线,体现了铜的延展性和
导电
性。(2)铜的加工:青铜是金属冶铸史上最早的合金,其主要成分是铜和锡。表中的A和B分别表示铜和青铜中的一种。《吕氏春秋》记载:“金(铜)柔锡柔,合两柔则刚。”据此判断A是
铜
。|物质|A|B|
|--|--|--|
|硬度|2.5~3|5~6.6|
注:硬度以金刚石的硬度为10作标准,1表示很软,10表示很硬。
(3)铜的回收:某工厂的废水经预处理后得到含$ FeSO_4 $和$ CuSO_4 $的溶液。为了减少污染并促进废物利用,工厂设计以下流程回收Cu和$ FeSO_4 $。

①步骤Ⅰ中发生反应的化学方程式为
$Fe + CuSO_{4} = FeSO_{4} + Cu$
。②溶液C中溶解的物质是
$FeSO_{4}$和$H_{2}SO_{4}$(硫酸亚铁和硫酸)
。
答案:
(1) 导电
(2) 铜
(3) ①$\boldsymbol{Fe + CuSO_{4} = FeSO_{4} + Cu}$ ②$\boldsymbol{FeSO_{4}}$和$\boldsymbol{H_{2}SO_{4}}$(硫酸亚铁和硫酸)
(1) 导电
(2) 铜
(3) ①$\boldsymbol{Fe + CuSO_{4} = FeSO_{4} + Cu}$ ②$\boldsymbol{FeSO_{4}}$和$\boldsymbol{H_{2}SO_{4}}$(硫酸亚铁和硫酸)
12. 金属活动性顺序是金属化学性质的核心内容,为了更好地掌握该知识,提升科学探究能力,某实验小组同学以铝、铁、铜三种常见金属为例,对金属活动性强弱的验证展开了项目化学习。
任务一:依据金属与氧气的反应进行验证
【查阅交流】(1)铝在常温下能与空气中的氧气反应,在表面形成致密的氧化铝薄膜,使铝更耐腐蚀。
(2)铁在空气中不能燃烧,在纯氧中点燃铁丝,能剧烈燃烧。
(3)铁、铜在常温下几乎不与氧气反应,在潮湿空气中,铜比铁耐腐蚀。
【得出结论】
小组同学依据
任务二:利用金属与稀酸的反应进行验证
【进行实验】分别取形状、大小完全相同的三种金属片放在三支试管中,进行如图1操作并记录了实验现象。
|金属片|实验现象|
|--|--|
|铝片|铝片表面产生大量气泡|
|铁片|
|铜片|铜片表面无明显现象|
【得出结论】金属活动性:$ Al>Fe>Cu $。
【反思评价】
小组同学仔细分析实验后,提出了质疑,认为实验不严密,理由是
任务三:根据金属与金属盐溶液的反应进行验证
【进行实验】如图2,分别取两片形状、大小完全相同的铁片放在试管中,滴加等量的氯化铝溶液和氯化铜溶液。
【实验分析】实验①无明显现象;实验②的现象是
任务一:依据金属与氧气的反应进行验证
【查阅交流】(1)铝在常温下能与空气中的氧气反应,在表面形成致密的氧化铝薄膜,使铝更耐腐蚀。
(2)铁在空气中不能燃烧,在纯氧中点燃铁丝,能剧烈燃烧。
(3)铁、铜在常温下几乎不与氧气反应,在潮湿空气中,铜比铁耐腐蚀。
【得出结论】
小组同学依据
金属与氧气反应的难易程度和剧烈程度
,得出结论:$ Al>Fe>Cu $(金属活泼性)。任务二:利用金属与稀酸的反应进行验证
【进行实验】分别取形状、大小完全相同的三种金属片放在三支试管中,进行如图1操作并记录了实验现象。
|金属片|实验现象|
|--|--|
|铝片|铝片表面产生大量气泡|
|铁片|
铁片表面产生少量气泡
||铜片|铜片表面无明显现象|
【得出结论】金属活动性:$ Al>Fe>Cu $。
【反思评价】
小组同学仔细分析实验后,提出了质疑,认为实验不严密,理由是
实验中酸的种类不同
。任务三:根据金属与金属盐溶液的反应进行验证
【进行实验】如图2,分别取两片形状、大小完全相同的铁片放在试管中,滴加等量的氯化铝溶液和氯化铜溶液。
【实验分析】实验①无明显现象;实验②的现象是
铁片表面有红色物质析出,溶液由蓝色变为浅绿色
,反应的化学方程式是$Fe + CuCl_{2} = FeCl_{2} + Cu$
。
答案:
【解析】:
- 任务一:金属与氧气反应的难易程度和剧烈程度
- 任务二:铁片表面产生少量气泡;实验中酸的种类不同
- 任务三:铁片表面有红色物质析出,溶液由蓝色变为浅绿色;$Fe + CuCl_{2} = FeCl_{2} + Cu$
【答案】:
- 金属与氧气反应的难易程度和剧烈程度
- 铁片表面产生少量气泡;实验中酸的种类不同
- 铁片表面有红色物质析出,溶液由蓝色变为浅绿色;$Fe + CuCl_{2} = FeCl_{2} + Cu$
- 任务一:金属与氧气反应的难易程度和剧烈程度
- 任务二:铁片表面产生少量气泡;实验中酸的种类不同
- 任务三:铁片表面有红色物质析出,溶液由蓝色变为浅绿色;$Fe + CuCl_{2} = FeCl_{2} + Cu$
【答案】:
- 金属与氧气反应的难易程度和剧烈程度
- 铁片表面产生少量气泡;实验中酸的种类不同
- 铁片表面有红色物质析出,溶液由蓝色变为浅绿色;$Fe + CuCl_{2} = FeCl_{2} + Cu$
查看更多完整答案,请扫码查看


