1. 下列可以作为溶质的是 ( )
A. 只有固体
B. 只有液体
C. 只有气体
D. 固体、液体或气体
A. 只有固体
B. 只有液体
C. 只有气体
D. 固体、液体或气体
答案:
D
2. [2024南京二模]下列溶液中的溶质,在通常状态下为气体的是 ( )
A. 食盐水
B. 稀盐酸
C. 澄清石灰水
D. 硫酸铜溶液
A. 食盐水
B. 稀盐酸
C. 澄清石灰水
D. 硫酸铜溶液
答案:
B
3. [2024苏州]下列有关溶液的说法正确的是 ( )
A. 溶液由溶质和溶剂组成
B. 碘酒中,碘是溶剂,酒精是溶质
C. 溶液中的溶质只能是一种
D. 所有溶液均是无色、澄清的液体
A. 溶液由溶质和溶剂组成
B. 碘酒中,碘是溶剂,酒精是溶质
C. 溶液中的溶质只能是一种
D. 所有溶液均是无色、澄清的液体
答案:
A 点拨:碘酒是碘的酒精溶液,碘是溶质,酒精是溶剂,B错误;一种或几种物质分散到另一种物质中,形成的均一、稳定的混合物叫做溶液,所以溶液中的溶质不一定只能是一种,可以有多种,C错误;不是所有溶液均是无色、澄清的液体,如硫酸铜溶液是蓝色的,D错误。
4. 对“溶质质量分数为10%的氯化钠溶液”的理解错误的是 ( )
A. 100 g水中溶解了10 g氯化钠
B. 将10 g氯化钠溶于90 g水中所得到的溶液
C. 100 g氯化钠溶液中含有10 g氯化钠
D. 氯化钠与溶液的质量比为1∶10
A. 100 g水中溶解了10 g氯化钠
B. 将10 g氯化钠溶于90 g水中所得到的溶液
C. 100 g氯化钠溶液中含有10 g氯化钠
D. 氯化钠与溶液的质量比为1∶10
答案:
A 点拨:100 g水中溶解10 g氯化钠,所得溶液的溶质质量分数为$\frac{10\ g}{10\ g + 100\ g}×100\% \approx 9.1\%$。
5. 把5 g食盐溶解在120 g水中,所得溶液中溶质的质量分数为 ( )
A. 4%
B. 4.2%
C. 4.4%
D. 5%
A. 4%
B. 4.2%
C. 4.4%
D. 5%
答案:
A
6. [2023宿迁期中]溶质质量分数为20%的某溶液,其中溶质与溶剂的质量比为 ( )
A. 1∶4
B. 1∶5
C. 4∶1
D. 5∶1
A. 1∶4
B. 1∶5
C. 4∶1
D. 5∶1
答案:
A 点拨:溶质质量分数为20%的某溶液的含义是每100份质量的该溶液中含有20份质量的溶质,其中溶质与溶剂的质量比为20:(100 - 20)=1:4。
7. [2024扬州]实验室用NaCl固体和蒸馏水配制50 g 15%的NaCl溶液时,不需要使用的仪器是 ( )
A. 烧杯
B. 玻璃棒
C. 量筒
D. 坩埚钳
A. 烧杯
B. 玻璃棒
C. 量筒
D. 坩埚钳
答案:
D
8. [2024连云港改编]配制100 g溶质质量分数为10%的NaOH溶液,主要操作流程如图所示:
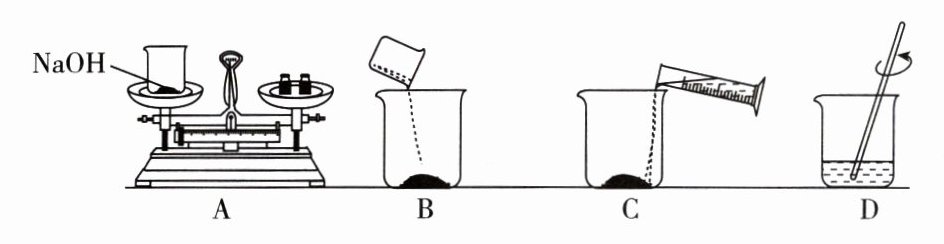
(1)A中应称量_______g NaOH固体,C中应用_______(填“50 mL”或“100 mL”)的量筒量取水。
(2)D中玻璃棒搅拌的目的是__________________________。
(3)用已配好的溶质质量分数为10%的NaOH溶液配制20 g溶质质量分数为5%或1%的NaOH溶液时,需计算所需溶质质量分数为10%的NaOH溶液的质量。计算依据是:溶液稀释前后,_________不变。

(1)A中应称量_______g NaOH固体,C中应用_______(填“50 mL”或“100 mL”)的量筒量取水。
(2)D中玻璃棒搅拌的目的是__________________________。
(3)用已配好的溶质质量分数为10%的NaOH溶液配制20 g溶质质量分数为5%或1%的NaOH溶液时,需计算所需溶质质量分数为10%的NaOH溶液的质量。计算依据是:溶液稀释前后,_________不变。
答案:
10@@100 mL@@加速NaOH溶解@@溶质质量
查看更多完整答案,请扫码查看


