1. [2023兴化月考]溶液与人们的生活息息相关。下列有关溶液的说法中,正确的是 ( )
A. 溶液一定是无色的,且溶剂一定是水
B. 5%的氯化钠溶液洒出一部分,剩余溶液的溶质质量分数仍为5%
C. 蔗糖溶液和食盐溶液都能导电
D. 利用洗洁精可以去除衣物或餐具上的油污,其原理和汽油除油污相同
A. 溶液一定是无色的,且溶剂一定是水
B. 5%的氯化钠溶液洒出一部分,剩余溶液的溶质质量分数仍为5%
C. 蔗糖溶液和食盐溶液都能导电
D. 利用洗洁精可以去除衣物或餐具上的油污,其原理和汽油除油污相同
答案:
B@@点拨:溶液是均一、稳定的混合物,但不一定为无色,如硫酸铜溶液为蓝色,其中溶剂可以是水,也可以是汽油、酒精等,A错误;溶液具有均一性,所以5%的氯化钠溶液洒出一部分,剩余溶液的溶质质量分数仍为5%,B正确;蔗糖溶液中存在蔗糖分子和水分子,没有能自由移动的离子,不能导电,而食盐溶液中存在能自由移动的钠离子和氯离子,能导电,C错误;利用洗洁精的乳化作用可以去除衣物或餐具上的油污,汽油除油污利用的是将油污溶解的原理,两者原理不同,D错误。
2. [2023西安曲江一中模拟]下列有关溶液的说法正确的是 ( )
A. 澄清石灰水中的溶质为石灰
B. 碘酒中的溶剂是水
C. Fe和过量CuSO₄溶液充分反应,所得溶液中的溶质为FeSO₄
D. 将过量的Zn加入稀H₂SO₄中,充分反应后所得溶液中的溶质为ZnSO₄
A. 澄清石灰水中的溶质为石灰
B. 碘酒中的溶剂是水
C. Fe和过量CuSO₄溶液充分反应,所得溶液中的溶质为FeSO₄
D. 将过量的Zn加入稀H₂SO₄中,充分反应后所得溶液中的溶质为ZnSO₄
答案:
D@@点拨:澄清石灰水中的溶质为氢氧化钙,氢氧化钙俗称熟石灰,A错误;碘酒是碘溶于酒精形成的溶液,其溶剂为酒精,B错误;铁能与硫酸铜反应生成硫酸亚铁和铜,则铁和过量硫酸铜溶液充分反应,所得溶液中的溶质为硫酸亚铁和硫酸铜,C错误;锌能与稀硫酸反应生成硫酸锌和氢气,锌为不溶物,则过量的锌与稀硫酸充分反应后所得溶液中的溶质为硫酸锌,D正确。【点方法】反应后溶液中的溶质一定要根据生成物进行判断,且要注意是否有可溶性的反应物过量。
3. 下列关于溶液的叙述正确的是 ( )
A. 溶液是均一、稳定的化合物
B. 浓溶液不一定是饱和溶液
C. 稀溶液一定是不饱和溶液
D. 饱和溶液就是不能再继续溶解任何溶质的溶液
A. 溶液是均一、稳定的化合物
B. 浓溶液不一定是饱和溶液
C. 稀溶液一定是不饱和溶液
D. 饱和溶液就是不能再继续溶解任何溶质的溶液
答案:
B@@点拨:溶液是均一、稳定的混合物,而不是化合物,A错误;浓溶液不一定是饱和溶液,也可能是不饱和溶液,如80℃时接近饱和的硝酸钾溶液是浓溶液,但不是饱和溶液,B正确;稀溶液不一定是不饱和溶液,也可能是饱和溶液,如饱和石灰水是稀溶液,C错误;某溶质的饱和溶液是指在一定温度下、一定量的溶剂里,不能再继续溶解这种溶质的溶液,但还能溶解其他溶质,D错误。【点易错】解答此题要注意:溶液是否饱和与溶液的浓稀没有必然联系,饱和溶液不一定是浓溶液,不饱和溶液不一定是稀溶液。
4. [2022扬州]KNO₃和KCl的溶解度曲线如图所示。下列说法正确的是 ( )
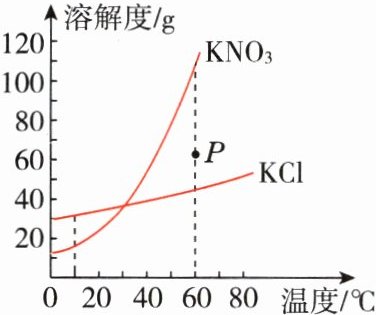
A. 10 ℃时,KNO₃的溶解度比KCl大
B. KCl的溶解度受温度变化的影响比KNO₃大
C. 60 ℃时,P点表示的KNO₃溶液还能继续溶解KNO₃固体
D. 将60 ℃的KCl饱和溶液降温至10 ℃,溶液中溶质质量分数不变

A. 10 ℃时,KNO₃的溶解度比KCl大
B. KCl的溶解度受温度变化的影响比KNO₃大
C. 60 ℃时,P点表示的KNO₃溶液还能继续溶解KNO₃固体
D. 将60 ℃的KCl饱和溶液降温至10 ℃,溶液中溶质质量分数不变
答案:
C@@点拨:由题图可知,10℃时KCl的溶解度比KNO₃大,A错误;KNO₃的溶解度受温度变化的影响比KCl大,B错误;60℃时,P点在KNO₃溶解度曲线的下方,表示的是KNO₃的不饱和溶液,因此还能继续溶解KNO₃固体,C正确;将60℃的KCl饱和溶液降温至10℃,KCl的溶解度变小,析出KCl晶体,溶液的溶质质量分数变小,D错误。【点易错】此题易因对溶解度曲线中点、交点的含义及曲线的变化趋势理解不清而错选。
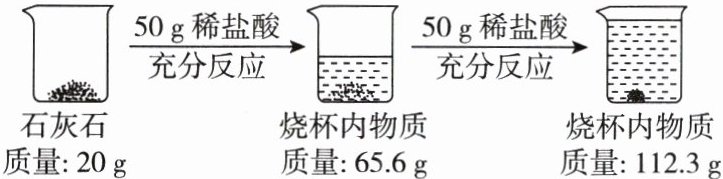
5. 化学小组在实验室用石灰石和稀盐酸进行实验(石灰石中的杂质不参加反应),实验过程和相关数据如图所示。请计算:
(1)生成二氧化碳的总质量为________g。
(2)该稀盐酸中溶质的质量分数。
(1)生成二氧化碳的总质量为________g。
(2)该稀盐酸中溶质的质量分数。

答案:
7.7@@解:50 g稀盐酸完全反应生成二氧化碳的质量为20 g+50 g-65.6 g=4.4 g。
设50 g稀盐酸中溶质的质量为x。
\[CaCO_{3}+2HCl = CaCl_{2}+H_{2}O + CO_{2}\uparrow\]
|73|44|
|----|----|
|x|4.4 g|
$\frac{73}{44}=\frac{x}{4.4 g}$ $x = 7.3 g$
该稀盐酸中溶质的质量分数为$\frac{7.3 g}{50 g}\times100\% = 14.6\%$。
答:该稀盐酸中溶质的质量分数为14.6%。
【点易错】本题易错将反应生成的二氧化碳的总质量代入化学方程式计算出100 g稀盐酸中溶质的质量,忽略了稀盐酸是否完全反应,从而算错稀盐酸中溶质的质量及质量分数。
查看更多完整答案,请扫码查看


