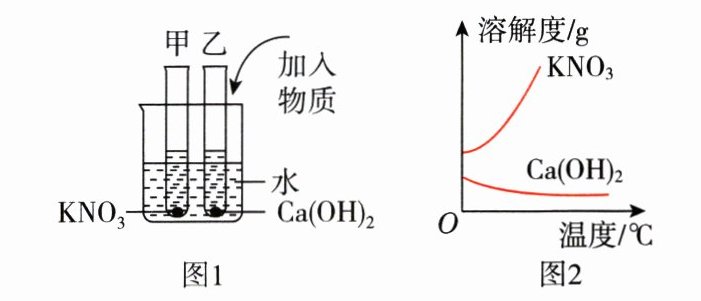
6. 如图1所示,甲、乙试管中分别盛有硝酸钾、氢氧化钙的饱和溶液,试管底部均有未溶解的固体。二者的溶解度曲线如图2所示。向烧杯中加入一定质量的氢氧化钠固体后,下列分析正确的是 ( )
A. 甲试管的溶液中溶质的质量减小
B. 甲试管中溶液的质量减小
C. 乙试管中固体的质量增大
D. 乙试管的溶液中溶质的质量增大

A. 甲试管的溶液中溶质的质量减小
B. 甲试管中溶液的质量减小
C. 乙试管中固体的质量增大
D. 乙试管的溶液中溶质的质量增大
答案:
C@@点拨:氢氧化钠溶于水放热,烧杯中溶液的温度升高。硝酸钾的溶解度随温度的升高而增大,甲试管中的固体会继续溶解,溶液中溶质的质量增大,溶液的质量也增大,A、B错误;氢氧化钙的溶解度随温度的升高而减小,乙试管中的溶液会析出氢氧化钙固体,故乙试管中固体的质量增大,溶液中溶质的质量减小,C正确,D错误。
7. t₁℃时,将等质量的硝酸钾和氯化钾分别加入盛有100g水的两个烧杯中,充分搅拌后现象如图1所示,硝酸钾和氯化钾的溶解度曲线如图2所示。下列说法错误的是 ( )

A. 烧杯①中溶解的溶质是氯化钾
B. 烧杯②中的上层清液属于饱和溶液
C. 将t₁℃时50g硝酸钾的饱和溶液稀释成5%的溶液,需加水150g
D. t₁℃时,将两个烧杯中的溶液混合,充分搅拌后,烧杯中一定还有剩余固体

A. 烧杯①中溶解的溶质是氯化钾
B. 烧杯②中的上层清液属于饱和溶液
C. 将t₁℃时50g硝酸钾的饱和溶液稀释成5%的溶液,需加水150g
D. t₁℃时,将两个烧杯中的溶液混合,充分搅拌后,烧杯中一定还有剩余固体
答案:
D@@点拨:$t_1℃$时,氯化钾的溶解度大于硝酸钾的溶解度,所以$t_1℃$时相同质量的水中溶解氯化钾的质量更大,结合图1可知,烧杯①中的固体完全溶解,烧杯②中有固体剩余,所以烧杯①中的溶质是氯化钾,烧杯②中的上层清液为饱和溶液,A、B正确;将$t_1℃$时50 g硝酸钾的饱和溶液(溶质质量为$50g×\frac{25g}{100g + 25g}=10g$)稀释成5%的溶液,需加水的质量为$10g÷5\% - 50g = 150g$,C正确;$t_1℃$时,将两个烧杯中的溶液混合,充分搅拌后,烧杯中不一定还有剩余固体,D错误。
8. [2024盐城节选]海水中含有KCl和MgSO₄等物质,其在不同温度时的溶解度如表所示,如图是对应溶解度曲线。

|温度/℃|20|30|40|60|80|100|
|----|----|----|----|----|----|----|
|溶解度/g|KCl|34.0|37.0|40.0|45.5|51.1|56.7|
||MgSO₄|33.7|38.9|44.5|54.6|52.9|50.4|
(1)图中曲线________(填“甲”或“乙”)代表KCl的溶解度曲线。
(2)40℃时,将50g KCl固体加入100g水中,________(填“能”或“不能”)得到150g KCl溶液。
(3)t₂℃时,将等质量的甲、乙两物质的饱和溶液降温到t₁℃,析出晶体的质量相等。判断:上述说法________(填“正确”或“错误”)。
(4)现有t₃℃时100g MgSO₄饱和溶液,逐渐降温经t₂℃直至t₁℃,其溶质质量分数的变化趋势为________________。

|温度/℃|20|30|40|60|80|100|
|----|----|----|----|----|----|----|
|溶解度/g|KCl|34.0|37.0|40.0|45.5|51.1|56.7|
||MgSO₄|33.7|38.9|44.5|54.6|52.9|50.4|
(1)图中曲线________(填“甲”或“乙”)代表KCl的溶解度曲线。
(2)40℃时,将50g KCl固体加入100g水中,________(填“能”或“不能”)得到150g KCl溶液。
(3)t₂℃时,将等质量的甲、乙两物质的饱和溶液降温到t₁℃,析出晶体的质量相等。判断:上述说法________(填“正确”或“错误”)。
(4)现有t₃℃时100g MgSO₄饱和溶液,逐渐降温经t₂℃直至t₁℃,其溶质质量分数的变化趋势为________________。
答案:
甲@@不能@@正确@@先不变后变小@@点拨:
- (1)由表格中数据可知,氯化钾的溶解度随温度升高而增大,硫酸镁的溶解度在一定温度范围内,随温度升高先增大后减小,图中曲线甲代表KCl的溶解度曲线。
- (2)40℃时氯化钾的溶解度是40 g,将50 g KCl固体加入100 g水中,只能溶解40 g KCl,不能得到150 g KCl溶液。
- (3)$t_2℃$时,将等质量的甲、乙两物质的饱和溶液降温到$t_1℃$,该温度范围内,两种物质的溶解度差相等,析出晶体的质量相等。
- (4)现有$t_3℃$时100 g $MgSO_4$饱和溶液,逐渐降温经$t_2℃$直至$t_1℃$,由于$MgSO_4$的溶解度先增大后减小,所以其溶质质量分数的变化趋势为先不变(温度降低变成不饱和溶液)后变小(温度降低后析出固体)。
查看更多完整答案,请扫码查看


