第9页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
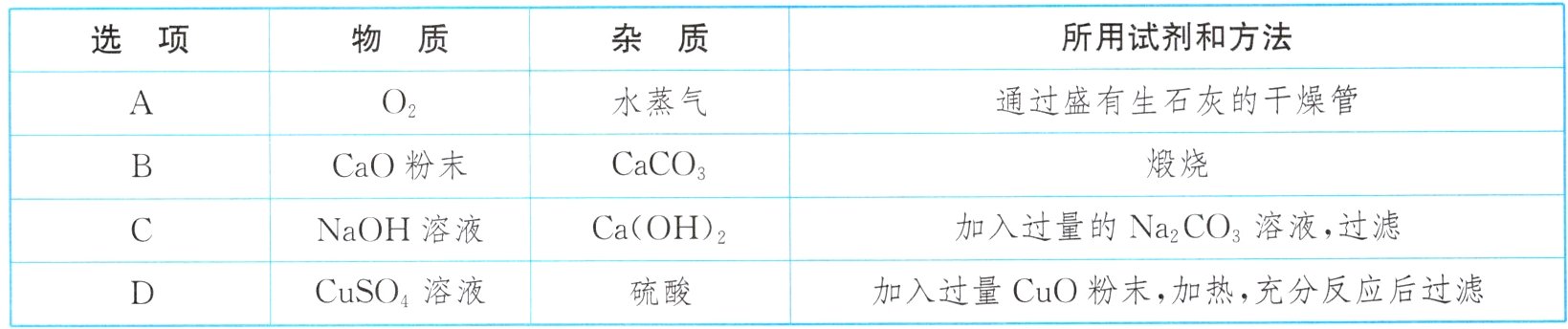
10. 除去下列各组物质中的杂质,所用试剂和方法不可行的是 ( )

答案:
10.C
11.(2023·海口模拟)用甲、乙两组实验证明二氧化碳能与氢氧化钠反应。已知:通常状况下,1体积水约能溶解1体积二氧化碳。
(1)甲实验:证明二氧化碳能与氢氧化钠反应的现象是______________________________。
(2)乙实验:测得瓶内压强变化如图丙所示。
① 首先注入瓶中的试剂是____________(填“$H_{2}O$”或“$NaOH$溶液”)。
② 对比坐标图中的______两段曲线,可证明二氧化碳能与氢氧化钠反应。

(1)甲实验:证明二氧化碳能与氢氧化钠反应的现象是______________________________。
(2)乙实验:测得瓶内压强变化如图丙所示。
① 首先注入瓶中的试剂是____________(填“$H_{2}O$”或“$NaOH$溶液”)。
② 对比坐标图中的______两段曲线,可证明二氧化碳能与氢氧化钠反应。

答案:
11.
(1)m试管内液面上升得比n试管高(合理答案均可)
(2)①$H_{2}O$ ②bc、de
(1)m试管内液面上升得比n试管高(合理答案均可)
(2)①$H_{2}O$ ②bc、de
12. 为测定某$CuSO_{4}$溶液中溶质的质量分数,取150 g该$CuSO_{4}$溶液,平均分为三份,每份样品均按如图所示进行实验,实验数据如表所示。请回答下列问题:
(1)50 g该$CuSO_{4}$溶液完全反应时,所得沉淀的质量为_______g。
(2)求该$CuSO_{4}$溶液中溶质的质量分数。(写出计算过程)

(1)50 g该$CuSO_{4}$溶液完全反应时,所得沉淀的质量为_______g。
(2)求该$CuSO_{4}$溶液中溶质的质量分数。(写出计算过程)

答案:
12.
(1)4.9
(2)解:设50g该$CuSO_{4}$溶液中溶质的质量为x。
$CuSO_{4} + 2NaOH = Cu(OH)_{2}\downarrow + Na_{2}SO_{4}$
160 98
x 4.9g
$\frac{160}{98} = \frac{x}{4.9g}$ $x = 8g$
该$CuSO_{4}$溶液中溶质的质量分数为$\frac{8g}{50g}×100\% = 16\%$。
答:该$CuSO_{4}$溶液中溶质的质量分数为16%。
(1)4.9
(2)解:设50g该$CuSO_{4}$溶液中溶质的质量为x。
$CuSO_{4} + 2NaOH = Cu(OH)_{2}\downarrow + Na_{2}SO_{4}$
160 98
x 4.9g
$\frac{160}{98} = \frac{x}{4.9g}$ $x = 8g$
该$CuSO_{4}$溶液中溶质的质量分数为$\frac{8g}{50g}×100\% = 16\%$。
答:该$CuSO_{4}$溶液中溶质的质量分数为16%。
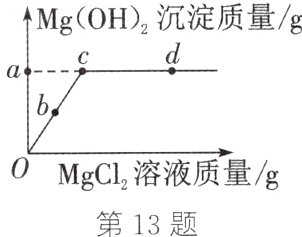
13.(2023·福州期中)向100 g溶质质量分数为4%的氢氧化钠溶液中逐滴加入氯化镁溶液,相关量的变化如图。下列说法错误的是 ( )
A. $a$点的值为2.9
B. $b$点对应的溶液能使无色酚酞试液变红
C. $c$点时两者恰好完全反应
D. $d$点对应的溶液含有三种溶质

A. $a$点的值为2.9
B. $b$点对应的溶液能使无色酚酞试液变红
C. $c$点时两者恰好完全反应
D. $d$点对应的溶液含有三种溶质
答案:
13.D解析:a点对应的值是恰好完全反应后生成的$Mg(OH)_{2}$的质量的数值,设恰好完全反应时生成的氢氧化镁的质量为x。
$2NaOH + MgCl_{2} = 2NaCl + Mg(OH)_{2}\downarrow$
80 58
$100g×4\%$ x
$\frac{80}{58} = \frac{100g×4\%}{x}$ $x = 2.9g$
即a = 2.9,A正确。b点时氢氧化钠还未反应完,故b点对应的溶液能使无色酚酞试液变红,B正确。c点时继续滴加氯化镁溶液,生成沉淀的质量不再增加,说明两者恰好完全反应,C正确。d点时氢氧化钠已完全反应,且滴加的氯化镁溶液已过量,此时溶液中含有氯化钠和氯化镁两种溶质,D不正确。故本题选D。
$2NaOH + MgCl_{2} = 2NaCl + Mg(OH)_{2}\downarrow$
80 58
$100g×4\%$ x
$\frac{80}{58} = \frac{100g×4\%}{x}$ $x = 2.9g$
即a = 2.9,A正确。b点时氢氧化钠还未反应完,故b点对应的溶液能使无色酚酞试液变红,B正确。c点时继续滴加氯化镁溶液,生成沉淀的质量不再增加,说明两者恰好完全反应,C正确。d点时氢氧化钠已完全反应,且滴加的氯化镁溶液已过量,此时溶液中含有氯化钠和氯化镁两种溶质,D不正确。故本题选D。
查看更多完整答案,请扫码查看


