第13页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
6. (2024·本溪段考)下列有关中和反应的说法正确的是 ( )
A. 反应物均须溶于水
B. 有沉淀生成
C. 有气体生成
D. 有盐生成
A. 反应物均须溶于水
B. 有沉淀生成
C. 有气体生成
D. 有盐生成
答案:
D
7. 中和反应在生活、生产中有广泛的应用,下列做法不是利用中和反应原理的是 ( )
A. 用熟石灰改良酸性土壤
B. 用稀盐酸除去铁制品表面的锈迹
C. 用含氢氧化镁的药物治疗胃酸过多
D. 用氨水(NH₃·H₂O)处理工厂的废酸
A. 用熟石灰改良酸性土壤
B. 用稀盐酸除去铁制品表面的锈迹
C. 用含氢氧化镁的药物治疗胃酸过多
D. 用氨水(NH₃·H₂O)处理工厂的废酸
答案:
B
8. (2023·南昌模拟)向滴有石蕊试液的稀盐酸中逐滴加入氢氧化钠溶液并振荡,一直加至氢氧化钠溶液过量,可观察到溶液的颜色变化过程为 ( )
A. 红→蓝→紫
B. 红→紫→蓝
C. 蓝→紫→红
D. 蓝→红→紫
A. 红→蓝→紫
B. 红→紫→蓝
C. 蓝→紫→红
D. 蓝→红→紫
答案:
B
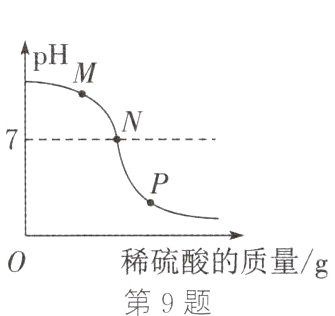
9. (2024·济南期末)向含有酚酞的氢氧化钠溶液中慢慢滴入稀硫酸,该过程中溶液pH的变化如图所示。下列分析正确的是 ( )
A. N点时的溶液一定呈红色 B. P点时溶液能与锌粒发生反应
C. M→N过程中溶液的碱性逐渐增强 D. M→P过程中生成的硫酸钠不断增加
A. N点时的溶液一定呈红色 B. P点时溶液能与锌粒发生反应
C. M→N过程中溶液的碱性逐渐增强 D. M→P过程中生成的硫酸钠不断增加

答案:
B 解析:$N$点时溶液的pH等于7,显中性,所以$N$点时的溶液一定呈无色,A错误。$P$点时溶液的pH小于7,显酸性,溶质为硫酸和硫酸钠,硫酸能与锌粒发生反应,B正确。$M→N$过程中溶液pH逐渐减小,碱性逐渐减弱,C错误。$M→P$过程中溶液pH不断减小,最终小于7,是因为硫酸先和氢氧化钠发生了中和反应,完全反应后,继续滴加稀硫酸,溶液呈酸性,且酸性越来越强,$M→P$过程中硫酸钠的质量先逐渐增加后保持不变,D错误。故本题选B。
10. (2024·榆林模拟)化学兴趣小组同学对氢氧化钾与硫酸能否发生反应进行了以下探究。
【实验步骤】取一定量氢氧化钾溶液于烧杯中,逐滴滴加稀硫酸,充分搅拌,无明显现象。
【提出问题】氢氧化钾与硫酸是否发生反应?
(1)猜想一:氢氧化钾与硫酸不发生反应。猜想二:______________________________。
【查阅资料】Na₂SO₄溶液呈中性,Ba²⁺与SO₄²⁻反应生成BaSO₄沉淀。
【实验验证】
(2)小响取10 mL氢氧化钾溶液于烧杯中,滴入2~3滴无色酚酞试液,再向烧杯中逐滴滴加稀硫酸,充分搅拌,观察到溶液由____________________。
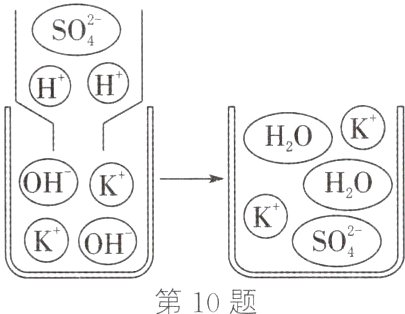
(3)小明上网查找到如图信息,可知氢氧化钾和硫酸反应的实质是____________________。
【得出结论】
(4)通过小组同学合作探究,证明猜想二是正确的,该反应的化学方程式为____________________。
【交流反思】
(5)对于无明显现象的化学反应,可通过检验有新物质生成或检验______________的方法来证明物质间发生了化学反应。
(6)小敏想进一步确定反应后无色溶液中的溶质成分,其中不能达到实验目的的是加入________(填序号)。
① 紫色石蕊试液 ② 氧化铁粉末 ③ 碳酸钠溶液 ④ 氯化钡溶液 ⑤ 铜片
【实验步骤】取一定量氢氧化钾溶液于烧杯中,逐滴滴加稀硫酸,充分搅拌,无明显现象。
【提出问题】氢氧化钾与硫酸是否发生反应?
(1)猜想一:氢氧化钾与硫酸不发生反应。猜想二:______________________________。
【查阅资料】Na₂SO₄溶液呈中性,Ba²⁺与SO₄²⁻反应生成BaSO₄沉淀。
【实验验证】
(2)小响取10 mL氢氧化钾溶液于烧杯中,滴入2~3滴无色酚酞试液,再向烧杯中逐滴滴加稀硫酸,充分搅拌,观察到溶液由____________________。
(3)小明上网查找到如图信息,可知氢氧化钾和硫酸反应的实质是____________________。
【得出结论】
(4)通过小组同学合作探究,证明猜想二是正确的,该反应的化学方程式为____________________。
【交流反思】
(5)对于无明显现象的化学反应,可通过检验有新物质生成或检验______________的方法来证明物质间发生了化学反应。
(6)小敏想进一步确定反应后无色溶液中的溶质成分,其中不能达到实验目的的是加入________(填序号)。
① 紫色石蕊试液 ② 氧化铁粉末 ③ 碳酸钠溶液 ④ 氯化钡溶液 ⑤ 铜片

答案:
(1)氢氧化钾与硫酸发生反应
(2)红色逐渐变为无色
(3)氢离子与氢氧根离子结合生成水分子
(4)$H_2SO_4 + 2KOH = K_2SO_4 + 2H_2O$
(5)反应物消失
(6)④⑤
(1)氢氧化钾与硫酸发生反应
(2)红色逐渐变为无色
(3)氢离子与氢氧根离子结合生成水分子
(4)$H_2SO_4 + 2KOH = K_2SO_4 + 2H_2O$
(5)反应物消失
(6)④⑤
查看更多完整答案,请扫码查看


