2026年金考卷特快专递高中化学
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年金考卷特快专递高中化学 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
17. (14分)在碳中和目标推动下,全球${CO_{2}}$加氢制甲醇技术加速发展。
Ⅰ. 间接法制甲醇
先将${CO_{2}}$与过量${H_{2}}$反应,获得含有$CO$和${H_{2}}$的混合气,再生产甲醇。相关反应如下:
反应ⅰ ${CO_{2}(g) + H_{2}(g)⇌ CO(g) + H_{2}O(g)}$ $\Delta H_{1} > 0$
反应ⅱ ${CO(g) + 2H_{2}(g)⇌ CH_{3}OH(g)}$ $\Delta H_{2}$
(1)相关键能如表所示,则$\Delta H_{2} = $

(2)恒压条件下,反应ⅰ结束后,先分离出混合气中的水蒸气,再进行甲醇合成,有利于提高$CO$和${H_{2}}$的平衡转化率,解释其原因为
Ⅱ. 直接法制甲醇
以${CO_{2}}$和${H_{2}}$为原料生产甲醇,发生反应ⅲ,同时发生副反应ⅰ。
反应ⅲ ${CO_{2}(g) + 3H_{2}(g)⇌ CH_{3}OH(g) + H_{2}O(g)}$ $\Delta H_{3} < 0$
(3)向$2\ L$恒容密闭容器中加入$1\ mol\ {CO_{2}}$和$3\ mol\ {H_{2}}$发生反应。平衡时,$CO$和${CH_{3}OH}$在含碳产物中的体积分数及${CO_{2}}$的转化率随温度的变化如图所示。
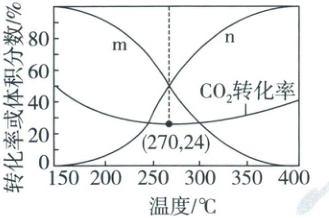
①表示甲醇体积分数随温度变化的曲线为
②$270\ ^{\circ} C$时,反应经$t\ min$达到平衡,则$0~t\ min$内${CH_{3}OH}$的生成速率$v{(CH_{3}OH)} = $
③$150\ ^{\circ} C~400\ ^{\circ} C$范围内,${CO_{2}}$的转化率先降低后升高的原因为
Ⅰ. 间接法制甲醇
先将${CO_{2}}$与过量${H_{2}}$反应,获得含有$CO$和${H_{2}}$的混合气,再生产甲醇。相关反应如下:
反应ⅰ ${CO_{2}(g) + H_{2}(g)⇌ CO(g) + H_{2}O(g)}$ $\Delta H_{1} > 0$
反应ⅱ ${CO(g) + 2H_{2}(g)⇌ CH_{3}OH(g)}$ $\Delta H_{2}$
(1)相关键能如表所示,则$\Delta H_{2} = $
$a + 2b - 3c - d - e$
$ kJ· mol^{-1}$(用含字母的代数式表示),反应ⅱ自发进行的条件为低温
(填“高温”“低温”或“任意温度”)。
(2)恒压条件下,反应ⅰ结束后,先分离出混合气中的水蒸气,再进行甲醇合成,有利于提高$CO$和${H_{2}}$的平衡转化率,解释其原因为
反应ⅱ是气体分子数减小的反应,脱水后,反应物的分压增大,有利于平衡正移
。Ⅱ. 直接法制甲醇
以${CO_{2}}$和${H_{2}}$为原料生产甲醇,发生反应ⅲ,同时发生副反应ⅰ。
反应ⅲ ${CO_{2}(g) + 3H_{2}(g)⇌ CH_{3}OH(g) + H_{2}O(g)}$ $\Delta H_{3} < 0$
(3)向$2\ L$恒容密闭容器中加入$1\ mol\ {CO_{2}}$和$3\ mol\ {H_{2}}$发生反应。平衡时,$CO$和${CH_{3}OH}$在含碳产物中的体积分数及${CO_{2}}$的转化率随温度的变化如图所示。

①表示甲醇体积分数随温度变化的曲线为
m
(填“m”或“n”)。②$270\ ^{\circ} C$时,反应经$t\ min$达到平衡,则$0~t\ min$内${CH_{3}OH}$的生成速率$v{(CH_{3}OH)} = $
$\frac{0.06}{t}$
$ mol· L^{-1}· min^{-1}$,生成${H_{2}O(g)}$的物质的量$n{(H_{2}O)} = $0.24
$ mol$,反应ⅲ的平衡常数$K_{ ⅲ} = $$\frac{0.06 × 0.12}{0.38 × 1.26^3}$
(列出计算式即可)。③$150\ ^{\circ} C~400\ ^{\circ} C$范围内,${CO_{2}}$的转化率先降低后升高的原因为
$\Delta H_1 > 0$;$\Delta H_3 < 0$ 150℃~270°C时反应ⅲ占主导,270℃~400℃反应ⅰ占主导
。
答案:
17
(1)$a + 2b - 3c - d - e$(2分) 低温(1分)
(2)反应ⅱ是气体分子数减小的反应,脱水后,反应物的分压增大,有利于平衡正移(2分,合理答案均可给分)
(3)①m(1分) ②$\frac{0.06}{t}$(2分) 0.24(2分) $\frac{0.06 × 0.12}{0.38 × 1.26^3}$(2 分,合理答案均可给分) ③$\Delta H_1 > 0$;$\Delta H_3 < 0$ 150℃~270°C时反应ⅲ占主导(给分点一),270℃~400℃反应ⅰ占主导(给分点二)(2分,两个给分点各1分)
(1)$a + 2b - 3c - d - e$(2分) 低温(1分)
(2)反应ⅱ是气体分子数减小的反应,脱水后,反应物的分压增大,有利于平衡正移(2分,合理答案均可给分)
(3)①m(1分) ②$\frac{0.06}{t}$(2分) 0.24(2分) $\frac{0.06 × 0.12}{0.38 × 1.26^3}$(2 分,合理答案均可给分) ③$\Delta H_1 > 0$;$\Delta H_3 < 0$ 150℃~270°C时反应ⅲ占主导(给分点一),270℃~400℃反应ⅰ占主导(给分点二)(2分,两个给分点各1分)
18. (15分)色瑞替尼(Ceritinib)是一种酪氨酸激酶抑制剂,其“微波促进”的合成方法如图所示(部分条件省略,副产物均未标出):
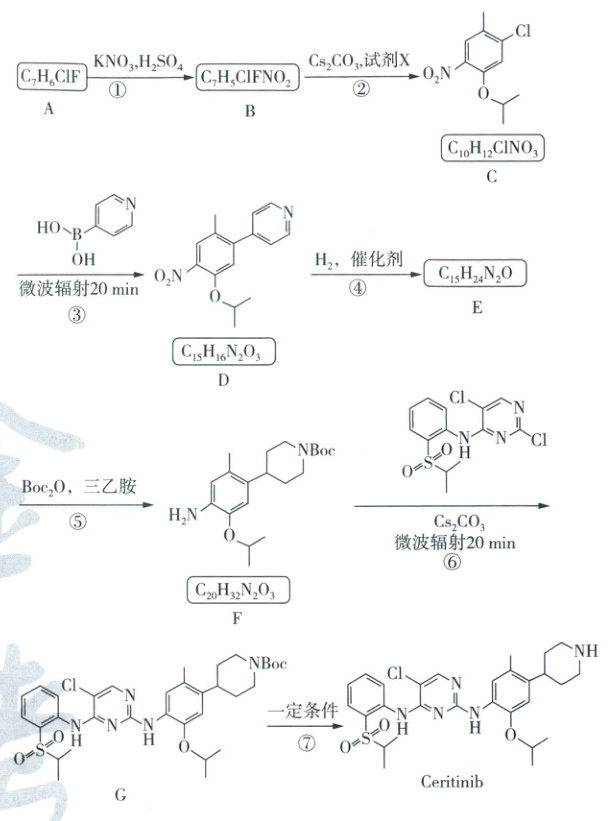
已知:ⅰ. Boc是叔丁氧羰基,$R - Boc$的结构为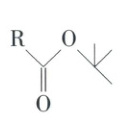
ⅱ. 反应③、⑥在传统合成方法中达到相同产率需要$20\ h$。
回答下列问题:
(1)$A\rightarrow B$的反应类型为
(2)试剂X的质谱图中最右侧的分子离子峰的质荷比数值为60,其核磁共振氢谱如图,则X的化学名称为
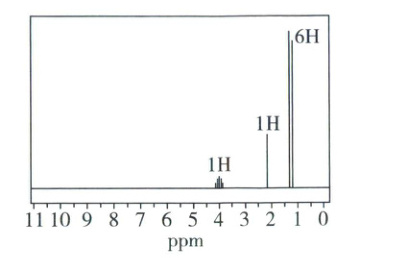
(3)$B\rightarrow C$加入${Cs_{2}CO_{3}}$的作用为
(4)微波辐射的目的为
(5)$D\rightarrow E$的化学方程式为 。
(6)与${Boc_{2}O}$在三乙胺条件下反应时, 的反应活性
的反应活性
(7)任写一种满足下列条件的C的同分异构体的结构简式: 或
或  (不考虑立体异构)。
(不考虑立体异构)。
ⅰ. X射线衍射实验发现分子含有苯环且苯环上有氨基(${-NH_{2}}$);
ⅱ. 能与${FeCl_{3}}$溶液发生显色反应;
ⅲ. 能发生银镜反应;
ⅳ. 核磁共振氢谱中峰面积之比为$1:1:2:2:6$。

已知:ⅰ. Boc是叔丁氧羰基,$R - Boc$的结构为

ⅱ. 反应③、⑥在传统合成方法中达到相同产率需要$20\ h$。
回答下列问题:
(1)$A\rightarrow B$的反应类型为
取代反应(或硝化反应)
,B中含氧官能团的名称为硝基
。(2)试剂X的质谱图中最右侧的分子离子峰的质荷比数值为60,其核磁共振氢谱如图,则X的化学名称为
2-丙醇(或异丙醇)
。
(3)$B\rightarrow C$加入${Cs_{2}CO_{3}}$的作用为
中和反应产生的HF,促进反应进行
。(4)微波辐射的目的为
加快反应速率
。(5)$D\rightarrow E$的化学方程式为
(6)与${Boc_{2}O}$在三乙胺条件下反应时,
 的反应活性
的反应活性低
(填“高”或“低”)。(7)任写一种满足下列条件的C的同分异构体的结构简式:
 或
或 
ⅰ. X射线衍射实验发现分子含有苯环且苯环上有氨基(${-NH_{2}}$);
ⅱ. 能与${FeCl_{3}}$溶液发生显色反应;
ⅲ. 能发生银镜反应;
ⅳ. 核磁共振氢谱中峰面积之比为$1:1:2:2:6$。
答案:
18
(1)取代反应(或硝化反应)(2分,多写或错写均不得分) 硝基(1分)
(2)2-丙醇(或异丙醇)(2分)
(3)中和反应产生的HF,促进反应进行(2分,合理答案均可给分)
(4)加快反应速率(2分)
(5) 2$\mathrm{H_2O}$(2分)
2$\mathrm{H_2O}$(2分)
(6)低(2分)
(7) 或
或  (2分)
(2分)
18
(1)取代反应(或硝化反应)(2分,多写或错写均不得分) 硝基(1分)
(2)2-丙醇(或异丙醇)(2分)
(3)中和反应产生的HF,促进反应进行(2分,合理答案均可给分)
(4)加快反应速率(2分)
(5)
 2$\mathrm{H_2O}$(2分)
2$\mathrm{H_2O}$(2分)(6)低(2分)
(7)
 或
或  (2分)
(2分) 查看更多完整答案,请扫码查看


