2026年金考卷特快专递高中化学
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年金考卷特快专递高中化学 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
9. 立方氮化硼晶体硬度仅次于金刚石,其晶胞结构如图所示。已知阿伏加德罗常数的值为$N_{ A}$,晶胞参数为$x\ pm$。下列说法正确的是
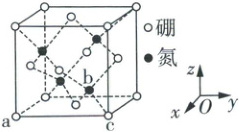
(图:立方晶胞,$B$在顶点和面心,$N$在体内)
A.$B$、$N$元素均位于元素周期表中的$ds$区
B.硼、氮原子间最短距离为$\boldsymbol{\frac{\sqrt{3}}{4}x\ pm}$
C.该晶体的密度为$\boldsymbol{\frac{4× 25}{N_{ A}· x^{3}}\ g· cm^{-3}}$($BN$的相对分子质量为25)
D.若$a$处原子分数坐标为$(1,0,0)$,则$b$处原子分数坐标为$\boldsymbol{(\frac{1}{4},\frac{3}{4},\frac{3}{4})}$

(图:立方晶胞,$B$在顶点和面心,$N$在体内)
A.$B$、$N$元素均位于元素周期表中的$ds$区
B.硼、氮原子间最短距离为$\boldsymbol{\frac{\sqrt{3}}{4}x\ pm}$
C.该晶体的密度为$\boldsymbol{\frac{4× 25}{N_{ A}· x^{3}}\ g· cm^{-3}}$($BN$的相对分子质量为25)
D.若$a$处原子分数坐标为$(1,0,0)$,则$b$处原子分数坐标为$\boldsymbol{(\frac{1}{4},\frac{3}{4},\frac{3}{4})}$
答案:
9.B 元素分区、晶胞分析与计算 硼、氮原子间的最短距离为晶胞体对角线长度的$\frac{1}{4}$,即x$\sqrt{3}$pm,B项正确
错误项分析 B的价电子排布式为2s²2p,N的价电子排布式为2s²2p;,均位于元素周期表的p区,A项错误;根据均摊法知,该晶胞中B的数目为8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,N的数目为4,则该晶体的密度为$\frac{(11+14)×4}{N.(x×10−10)3}$g.cm3=$\frac{25×4}{N.x²×10−30}$g.cm3
A
C项错误;若a处原子分数坐标为(1,0,0),则坐标原点位于晶胞底面左后方处,故b处原子的分数坐标为($\frac{3}{4}$'A$\frac{3}{4}$”$\frac{1}{4}$),D项错误
错误项分析 B的价电子排布式为2s²2p,N的价电子排布式为2s²2p;,均位于元素周期表的p区,A项错误;根据均摊法知,该晶胞中B的数目为8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,N的数目为4,则该晶体的密度为$\frac{(11+14)×4}{N.(x×10−10)3}$g.cm3=$\frac{25×4}{N.x²×10−30}$g.cm3
A
C项错误;若a处原子分数坐标为(1,0,0),则坐标原点位于晶胞底面左后方处,故b处原子的分数坐标为($\frac{3}{4}$'A$\frac{3}{4}$”$\frac{1}{4}$),D项错误
10. 化合物$Q$是合成一种抗癌药物的原料,可由如下反应合成。下列说法正确的是
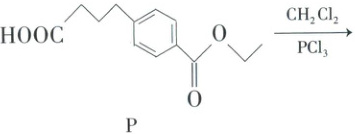
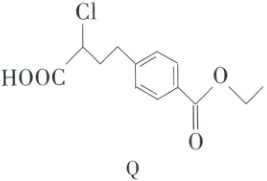
A.$P$与苯乙酸甲酯互为同系物
B.化合物$P$和$Q$中都含有2个手性碳原子
C.$1\ mol\ P$与${H_{2}}$加成,最多消耗$5\ mol\ {H_{2}}$
D.$1\ mol\ Q$最多消耗$NaOH$、${NaHCO_{3}}$的物质的量之比为$3:1$


A.$P$与苯乙酸甲酯互为同系物
B.化合物$P$和$Q$中都含有2个手性碳原子
C.$1\ mol\ P$与${H_{2}}$加成,最多消耗$5\ mol\ {H_{2}}$
D.$1\ mol\ Q$最多消耗$NaOH$、${NaHCO_{3}}$的物质的量之比为$3:1$
答案:
10.D 有机物的结构和性质

Q中氯原子、羧基、酯基都能与NaOH反应,1molQ最多消耗3molNaOH,只有羧基能与NaHCO3反应,1molQ最多消耗1molNaHCO,故1molQ最多消耗NaOH、NaHCO3的物质的量之比为3:1,D项正确。
错误项分析 P中含有酯基、羧基,而苯乙酸甲酯中只含酯基,故二者不互为同系物,A项错误;化合物P中不含手性碳原子,化合物Q中只有连接一COOH的碳原子为手性碳原子,B项错误;P中只有苯环能与H2加成,1molP含有1mol苯环,与H2 加成时,最多消耗3molH2,C项错误。
知识拓展 常见的有机化学反应的定量关系
可以与NaOH溶液反应的官能团:一COOH、酚羟基、1 −1mXo( )lXNa=OFH、、C1lm、Borl、酚I)羟,定基量~关1m系o)l为Na1OmHo、l1−mColO−OHX~
1molNaOH
2 可为以1m与o金l−属C钠O反OH应~的1官mo能lN团a:、1一mCOolO羟H基、羟~基1,m定ol量N关a系
可以与Na2CO溶液反应的官能团;−COOH、酚羟基,3 定量关系为1mol−C00H~0.5molNaC0~0.5mol
CO2、1mo)l酚羟基~1molNa2CO
4 可系以为与1mNoal1H−COCOO溶H液~反1m应o的lN官aH能CO团,:~-1CmOoOlHCO,2定2量关1
10.D 有机物的结构和性质

Q中氯原子、羧基、酯基都能与NaOH反应,1molQ最多消耗3molNaOH,只有羧基能与NaHCO3反应,1molQ最多消耗1molNaHCO,故1molQ最多消耗NaOH、NaHCO3的物质的量之比为3:1,D项正确。
错误项分析 P中含有酯基、羧基,而苯乙酸甲酯中只含酯基,故二者不互为同系物,A项错误;化合物P中不含手性碳原子,化合物Q中只有连接一COOH的碳原子为手性碳原子,B项错误;P中只有苯环能与H2加成,1molP含有1mol苯环,与H2 加成时,最多消耗3molH2,C项错误。
知识拓展 常见的有机化学反应的定量关系
可以与NaOH溶液反应的官能团:一COOH、酚羟基、1 −1mXo( )lXNa=OFH、、C1lm、Borl、酚I)羟,定基量~关1m系o)l为Na1OmHo、l1−mColO−OHX~
1molNaOH
2 可为以1m与o金l−属C钠O反OH应~的1官mo能lN团a:、1一mCOolO羟H基、羟~基1,m定ol量N关a系
可以与Na2CO溶液反应的官能团;−COOH、酚羟基,3 定量关系为1mol−C00H~0.5molNaC0~0.5mol
CO2、1mo)l酚羟基~1molNa2CO
4 可系以为与1mNoal1H−COCOO溶H液~反1m应o的lN官aH能CO团,:~-1CmOoOlHCO,2定2量关1
11. 一种离子液体结构如图,其中$Y$、$Z$、$M$、$N$位于同一短周期,$Y$的一种同位素可用于考古断代。下列说法错误的是
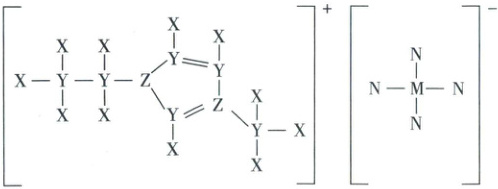
(阳离子:$Y$、$Z$、$X$组成;阴离子:$N - M - N$,$M$上下连$N$)
A.阴离子中所有原子最外层均满足8电子稳定结构
B.最高价氧化物对应水化物的酸性:$M > Z$
C.原子序数:$N > Z > Y > M$
D.最简单氢化物沸点:$N > Z$

(阳离子:$Y$、$Z$、$X$组成;阴离子:$N - M - N$,$M$上下连$N$)
A.阴离子中所有原子最外层均满足8电子稳定结构
B.最高价氧化物对应水化物的酸性:$M > Z$
C.原子序数:$N > Z > Y > M$
D.最简单氢化物沸点:$N > Z$
答案:
11.B 元素推断、元素周期律
审元素
Y的一种同位素可用于考古断代 Y为C
Y、Z、M、 Z带形一成个3单位个键正或电荷4个键,阳离子 Z为N
N同周期位一于短 M位形负电成荷4个键,阴离子带一个单 M为B
N形成1个键 N为F
X形成1个键 X可能为H 同周期主族元素从左到右非金属性逐渐增强,最高价氧化物对应水化物的酸性逐渐增强,故非金属性:B<N,最高价氧化物对应水化物的酸性:HBO<HNO,B项错误
阴离子中B得到一个电子,和F形成4个共价键,故阴离子中所有原子最外层均满足8电子稳定结构,A项正确;原子序数:F>N>C>B,C项正确;标准状况下HF为液体,NH为气体,故最简单氢化物沸点:HF>NH3,D项正确
审元素
Y的一种同位素可用于考古断代 Y为C
Y、Z、M、 Z带形一成个3单位个键正或电荷4个键,阳离子 Z为N
N同周期位一于短 M位形负电成荷4个键,阴离子带一个单 M为B
N形成1个键 N为F
X形成1个键 X可能为H 同周期主族元素从左到右非金属性逐渐增强,最高价氧化物对应水化物的酸性逐渐增强,故非金属性:B<N,最高价氧化物对应水化物的酸性:HBO<HNO,B项错误
阴离子中B得到一个电子,和F形成4个共价键,故阴离子中所有原子最外层均满足8电子稳定结构,A项正确;原子序数:F>N>C>B,C项正确;标准状况下HF为液体,NH为气体,故最简单氢化物沸点:HF>NH3,D项正确
12. 由下列实验操作及现象所得结论正确的是


答案:
12.C 化学实验分析和评价 分别向浓度均为0.1mol.L
的FeSO和CuSO溶液中通入H2S气体至饱和,前者无明显现象,后者生成沉淀,说明CuS的溶解度比FeS的小,故溶度积常数:K(FeS)>K(Cu応),C项正确。
错误项分析 二价铁离子和C1均可以被酸性KMnO溶液氧化而使溶液紫色褪去,因此题给实验操作及现象不能说明铁锈中含有二价铁离子,A项错误;溴乙烷水解在碱性条件下进行,直接加入AgNO3溶液,Br和OH均能与Ag反应产生不溶于水的沉淀,应先加入稀硝酸使溶液呈酸性,再加入AgNO3溶液,B项错误;等浓度的CHCOONa和HCOONa溶液,
CHCOONa溶液的pH大,说明CHCOO 的水解程度大于HCOO−的水解程度,根据“越弱越水解”,酸性:CHCOOH<HCOOH,故K。(CHCOOH)<K(HCOOH),D项错误。
的FeSO和CuSO溶液中通入H2S气体至饱和,前者无明显现象,后者生成沉淀,说明CuS的溶解度比FeS的小,故溶度积常数:K(FeS)>K(Cu応),C项正确。
错误项分析 二价铁离子和C1均可以被酸性KMnO溶液氧化而使溶液紫色褪去,因此题给实验操作及现象不能说明铁锈中含有二价铁离子,A项错误;溴乙烷水解在碱性条件下进行,直接加入AgNO3溶液,Br和OH均能与Ag反应产生不溶于水的沉淀,应先加入稀硝酸使溶液呈酸性,再加入AgNO3溶液,B项错误;等浓度的CHCOONa和HCOONa溶液,
CHCOONa溶液的pH大,说明CHCOO 的水解程度大于HCOO−的水解程度,根据“越弱越水解”,酸性:CHCOOH<HCOOH,故K。(CHCOOH)<K(HCOOH),D项错误。
13. 科学家基于${Cl_{2}}$易溶于${CCl_{4}}$的性质,发展了一种新型储能氯流电池(如图),其中电极$a$为${NaTi_{2}(PO_{4})_{3}/Na_{3}Ti_{2}(PO_{4})_{3}}$。通过风力发电进行充电时,电极$a$的反应为${NaTi_{2}(PO_{4})_{3} + 2Na^{+} + 2e^{-} = Na_{3}Ti_{2}(PO_{4})_{3}}$。下列说法错误的是

(图:电极$b$是${Cl_{2}/CCl_{4}}$,电极$a$是$NaCl$溶液,充电时风力发电连接)
A.放电时,电流的流向:电极$b -> 输电网 -> 电极a$
B.放电时,电极$a$为负极,发生氧化反应
C.放电时总反应:${NaTi_{2}(PO_{4})_{3} + 2NaCl\xlongequal{放电} Na_{3}Ti_{2}(PO_{4})_{3} + Cl_{2}\uparrow}$
D.充电时,每转移$0.4\ mol$电子,$NaCl$溶液质量减少$23.4\ g$

(图:电极$b$是${Cl_{2}/CCl_{4}}$,电极$a$是$NaCl$溶液,充电时风力发电连接)
A.放电时,电流的流向:电极$b -> 输电网 -> 电极a$
B.放电时,电极$a$为负极,发生氧化反应
C.放电时总反应:${NaTi_{2}(PO_{4})_{3} + 2NaCl\xlongequal{放电} Na_{3}Ti_{2}(PO_{4})_{3} + Cl_{2}\uparrow}$
D.充电时,每转移$0.4\ mol$电子,$NaCl$溶液质量减少$23.4\ g$
答案:
13.C 新型储能氯流电池的工作原理
电池分析

电极 电极反应式
放充电电负正阴阳极极极极$\frac{电极b}{电极}$电电极极abNNaa3TTii((PPOO4))323C+C−ll22N+e−a22+=ee+=2eN=a=2TCCil=l(NP↑Oa3T)i3+(P2ONa)3 总反应 NaTi(PO)3+Cl2放充电电NaTi2(PO)3+2NaCl 由上述分析可知,放电时负极上NasTi2(PO4)3失去电子,发生氧化反应生成NaTi2(POa)3,正极上Cl2得到电子,发生还原反应生成Cl,总反应为Na3Ti(PO)3+Cl2放电NaTi2(PO)3+2NaCl,C项错误。
放电时,电极a为负极,电极b为正极,外电路中电流的流向为正极→负极,即电极b→输电网→电极a,A项正确;放电时,电极a为负极,发生氧化反应,B项正确;充电时,NaCl溶液中的Na和Cl−分别向阴、阳极移动,根据转移电子守恒可知,2Na+~2Cl~2e”~2NaCl,故每转移0.4mol电子,NaCl溶液质量减少0.4mol×58.5g.mol=23.4g,D项正确。
13.C 新型储能氯流电池的工作原理
电池分析

电极 电极反应式
放充电电负正阴阳极极极极$\frac{电极b}{电极}$电电极极abNNaa3TTii((PPOO4))323C+C−ll22N+e−a22+=ee+=2eN=a=2TCCil=l(NP↑Oa3T)i3+(P2ONa)3 总反应 NaTi(PO)3+Cl2放充电电NaTi2(PO)3+2NaCl 由上述分析可知,放电时负极上NasTi2(PO4)3失去电子,发生氧化反应生成NaTi2(POa)3,正极上Cl2得到电子,发生还原反应生成Cl,总反应为Na3Ti(PO)3+Cl2放电NaTi2(PO)3+2NaCl,C项错误。
放电时,电极a为负极,电极b为正极,外电路中电流的流向为正极→负极,即电极b→输电网→电极a,A项正确;放电时,电极a为负极,发生氧化反应,B项正确;充电时,NaCl溶液中的Na和Cl−分别向阴、阳极移动,根据转移电子守恒可知,2Na+~2Cl~2e”~2NaCl,故每转移0.4mol电子,NaCl溶液质量减少0.4mol×58.5g.mol=23.4g,D项正确。
查看更多完整答案,请扫码查看


