2026年新高考5年真题高中化学全一册通用版湖南专版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年新高考5年真题高中化学全一册通用版湖南专版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第86页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
5. [2025·湖北卷,9T,3分] $\mathrm{SO_2}$ 晶胞是长方体,边长 $a \neq b \neq c$,如图所示。下列说法正确的是 (
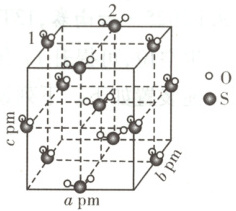
A.一个晶胞中含有 4 个 O 原子
B.晶胞中 $\mathrm{SO_2}$ 分子的取向相同
C.1 号和 2 号 S 原子间的核间距为 $\frac{\sqrt{2}}{2} \sqrt{a^2 + b^2}\ \mathrm{pm}$
D.每个 S 原子周围与其等距且紧邻的 S 原子有 4 个
D
)
A.一个晶胞中含有 4 个 O 原子
B.晶胞中 $\mathrm{SO_2}$ 分子的取向相同
C.1 号和 2 号 S 原子间的核间距为 $\frac{\sqrt{2}}{2} \sqrt{a^2 + b^2}\ \mathrm{pm}$
D.每个 S 原子周围与其等距且紧邻的 S 原子有 4 个
答案:
5. 参考答案D
命题意图本题通过晶胞参数分析,意在强化考生对晶体知识的应用,体现了“证据推理与模型认知”等化学学科核心素养。
解题思路由晶胞图可知,$ SO_2$分子位于晶胞的棱心和体心,一个晶胞中含有$12 × \frac{1}{4}+1=4$个$ SO_2$分子,则一个晶胞中含有8个O原子,A项错误。由图可知,晶胞中$ SO_2$分子有2种取向,B项错误。1号和2号S原子间的核间距为顶面面对角线长度的一半,则核间距为$\frac{1}{2} \sqrt{a^2+b^2} pm$,C项错误。以体心的S原子为例,由于$a \neq b \neq c$,每个S原子周围与其等距且紧邻的S原子有4个,D项正确。
命题意图本题通过晶胞参数分析,意在强化考生对晶体知识的应用,体现了“证据推理与模型认知”等化学学科核心素养。
解题思路由晶胞图可知,$ SO_2$分子位于晶胞的棱心和体心,一个晶胞中含有$12 × \frac{1}{4}+1=4$个$ SO_2$分子,则一个晶胞中含有8个O原子,A项错误。由图可知,晶胞中$ SO_2$分子有2种取向,B项错误。1号和2号S原子间的核间距为顶面面对角线长度的一半,则核间距为$\frac{1}{2} \sqrt{a^2+b^2} pm$,C项错误。以体心的S原子为例,由于$a \neq b \neq c$,每个S原子周围与其等距且紧邻的S原子有4个,D项正确。
6. [2025·浙江 1 月卷,13T,3分]某化合物 $\mathrm{Fe(NH_3)_2Cl_2}$ 的晶胞如图所示,下列说法不正确的是 (
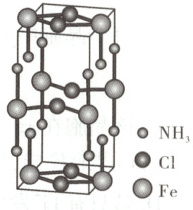
A.晶体类型为混合晶体
B.$\mathrm{NH_3}$ 与二价铁形成配位键
C.该化合物与水反应有难溶物生成
D.该化合物热稳定性比 $\mathrm{FeCl_2}$ 高
D
)
A.晶体类型为混合晶体
B.$\mathrm{NH_3}$ 与二价铁形成配位键
C.该化合物与水反应有难溶物生成
D.该化合物热稳定性比 $\mathrm{FeCl_2}$ 高
答案:
6. 参考答案D
命题意图本题考查晶体与配合物相关知识,意在考查考生的理解分析与判断能力,体现了“证据推理与模型认知”等化学学科核心素养。
解题思路该晶体中存在$ Fe^{2+}$、$ Cl^-$之间的离子键、$ Fe^{2+}$与$ NH_3$中N原子间的配位键和$ NH_3$分子间作用力,故晶体类型为混合晶体,A项正确。$ NH_3$与$ Fe^{2+}$通过配位键形成$[ Fe( NH_3)_2]^{2+}$,B项正确。$ Fe( NH_3)_2 Cl_2$溶于水可得到$ NH_3 · H_2 O$和$ Fe^{2+}$,二者反应可以生成$ Fe( OH)_2$沉淀,总反应方程式为$ Fe( NH_3)_2 Cl_2+2 H_2 O= Fe( OH)_2 \downarrow+2 NH_4 Cl$,C项正确。$ NH_3$与$ Fe^{2+}$形成的配位键不稳定,容易分解为$ FeCl_2$和$ NH_3$,故$ Fe( NH_3)_2 Cl_2$热稳定性小于$ FeCl_2$,D项错误。
命题意图本题考查晶体与配合物相关知识,意在考查考生的理解分析与判断能力,体现了“证据推理与模型认知”等化学学科核心素养。
解题思路该晶体中存在$ Fe^{2+}$、$ Cl^-$之间的离子键、$ Fe^{2+}$与$ NH_3$中N原子间的配位键和$ NH_3$分子间作用力,故晶体类型为混合晶体,A项正确。$ NH_3$与$ Fe^{2+}$通过配位键形成$[ Fe( NH_3)_2]^{2+}$,B项正确。$ Fe( NH_3)_2 Cl_2$溶于水可得到$ NH_3 · H_2 O$和$ Fe^{2+}$,二者反应可以生成$ Fe( OH)_2$沉淀,总反应方程式为$ Fe( NH_3)_2 Cl_2+2 H_2 O= Fe( OH)_2 \downarrow+2 NH_4 Cl$,C项正确。$ NH_3$与$ Fe^{2+}$形成的配位键不稳定,容易分解为$ FeCl_2$和$ NH_3$,故$ Fe( NH_3)_2 Cl_2$热稳定性小于$ FeCl_2$,D项错误。
7. [2025·河北卷,11T,3分] $\mathrm{SmCo_k}$ ($k>1$) 是一种具有优异磁性能的稀土永磁材料,在航空航天等领域中获得重要应用。$\mathrm{SmCo_k}$ 的六方晶胞示意图如下,晶胞参数 $a = 500\ \mathrm{pm}$、$c = 400\ \mathrm{pm}$,M、N 原子的分数坐标分别为 $(\frac{5}{6}, \frac{1}{6}, \frac{1}{2})$、$(\frac{1}{6}, \frac{5}{6}, \frac{1}{2})$。设 $N_\mathrm{A}$ 是阿伏加德罗常数的值。下列说法错误的是 (

A.该物质的化学式为 $\mathrm{SmCo_5}$
B.体心原子的分数坐标为 $(\frac{1}{2}, \frac{1}{2}, \frac{1}{2})$
C.晶体的密度为 $\frac{890\sqrt{3}}{3N_\mathrm{A} × 10^{-22}}\ \mathrm{g · cm^{-3}}$
D.原子 Q 到体心的距离为 $\frac{100}{41}\sqrt{ } 100\ \mathrm{pm}$
D
)
A.该物质的化学式为 $\mathrm{SmCo_5}$
B.体心原子的分数坐标为 $(\frac{1}{2}, \frac{1}{2}, \frac{1}{2})$
C.晶体的密度为 $\frac{890\sqrt{3}}{3N_\mathrm{A} × 10^{-22}}\ \mathrm{g · cm^{-3}}$
D.原子 Q 到体心的距离为 $\frac{100}{41}\sqrt{ } 100\ \mathrm{pm}$
答案:
7. 参考答案D
命题意图本题以$ SmCo_k$的六方晶胞为情境,涉及均摊法、分数坐标、晶体密度等知识,体现了“证据推理与模型认知”等化学学科核心素养。
解题思路根据均摊法,白球位于体心,晶胞中数目为1,黑球位于顶角、棱心和体内,晶胞中数目为$4 × \frac{1}{6}+4 × \frac{1}{12}+8 × \frac{1}{2}=5$,结合晶胞的化学式$ SmCo_k(k>1)$可知,白球为Sm、黑球为Co,该物质化学式为$ SmCo_5$,A项正确。体心原子位于晶胞的中心,其分数坐标为$(\frac{1}{2}, \frac{1}{2}, \frac{1}{2})$,B项正确。每个晶胞中含有1个$ SmCo_5$,晶胞底面为菱形,底面面积为$\frac{\sqrt{3}}{2} a^2$,六方晶胞的体积为$\frac{\sqrt{3}}{2} a^2 c$,则晶体密度为$\frac{150+59 × 5}{N_{ A} × \frac{\sqrt{3}}{2} a^2 c}=\frac{445}{N_{ A} × \frac{\sqrt{3}}{2} × (500 × 10^{-10})^2 × (400 × 10^{-10})}=\frac{890\sqrt{3}}{3N_{ A} × 10^{-22}} g · cm^{-3}$,C项正确。原子Q的分数坐标为(0, $\frac{1}{2}$, 1),由体心原子向上底面作垂线,垂足为上底面面心,连接该面心与原子Q、体心与原子Q可得直角三角形,如图 ,则原子Q到体心的距离为$\sqrt{250^2+200^2} pm=50\sqrt{41} pm$,D项错误。
,则原子Q到体心的距离为$\sqrt{250^2+200^2} pm=50\sqrt{41} pm$,D项错误。
7. 参考答案D
命题意图本题以$ SmCo_k$的六方晶胞为情境,涉及均摊法、分数坐标、晶体密度等知识,体现了“证据推理与模型认知”等化学学科核心素养。
解题思路根据均摊法,白球位于体心,晶胞中数目为1,黑球位于顶角、棱心和体内,晶胞中数目为$4 × \frac{1}{6}+4 × \frac{1}{12}+8 × \frac{1}{2}=5$,结合晶胞的化学式$ SmCo_k(k>1)$可知,白球为Sm、黑球为Co,该物质化学式为$ SmCo_5$,A项正确。体心原子位于晶胞的中心,其分数坐标为$(\frac{1}{2}, \frac{1}{2}, \frac{1}{2})$,B项正确。每个晶胞中含有1个$ SmCo_5$,晶胞底面为菱形,底面面积为$\frac{\sqrt{3}}{2} a^2$,六方晶胞的体积为$\frac{\sqrt{3}}{2} a^2 c$,则晶体密度为$\frac{150+59 × 5}{N_{ A} × \frac{\sqrt{3}}{2} a^2 c}=\frac{445}{N_{ A} × \frac{\sqrt{3}}{2} × (500 × 10^{-10})^2 × (400 × 10^{-10})}=\frac{890\sqrt{3}}{3N_{ A} × 10^{-22}} g · cm^{-3}$,C项正确。原子Q的分数坐标为(0, $\frac{1}{2}$, 1),由体心原子向上底面作垂线,垂足为上底面面心,连接该面心与原子Q、体心与原子Q可得直角三角形,如图
 ,则原子Q到体心的距离为$\sqrt{250^2+200^2} pm=50\sqrt{41} pm$,D项错误。
,则原子Q到体心的距离为$\sqrt{250^2+200^2} pm=50\sqrt{41} pm$,D项错误。 8. [2025·安徽卷,12T,3分]碘晶体为层状结构,层间作用为范德华力,层间距为 $d\ \mathrm{pm}$。下图给出了碘的单层结构,层内碘分子间存在“卤键”(强度与氢键相近)。$N_\mathrm{A}$ 为阿伏加德罗常数的值。下列说法错误的是 (
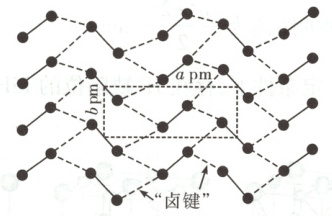
A.碘晶体是混合型晶体
B.液态碘单质中也存在“卤键”
C.127 g 碘晶体中有 $N_\mathrm{A}$ 个“卤键”
D.碘晶体的密度为 $\frac{2 × 254}{abd × N_\mathrm{A} × 10^{-30}}\ \mathrm{g · cm^{-3}}$
A
)
A.碘晶体是混合型晶体
B.液态碘单质中也存在“卤键”
C.127 g 碘晶体中有 $N_\mathrm{A}$ 个“卤键”
D.碘晶体的密度为 $\frac{2 × 254}{abd × N_\mathrm{A} × 10^{-30}}\ \mathrm{g · cm^{-3}}$
答案:
8. 参考答案A
命题意图本题通过碘晶体结构分析,考查晶体类型判断、卤键性质及晶胞密度计算,体现了“证据推理与模型认知”等化学学科核心素养。
解题思路由图示碘晶体的单层结构可知,层内分子间存在“卤键”(类似氢键)和范德华力,层间作用为范德华力,则碘晶体是分子晶体,而不是混合型晶体,A项错误。类比水,在固态水和液态水分子之间都存在氢键,则液态碘单质中也存在“卤键”,B项正确。由图可知,每个$ I_2$分子连有4个“卤键”,每个“卤键”被2个碘分子共用,由均摊法知,1个$ I_2$分子“占有”2个“卤键”,C项正确。从相邻两层碘分子中选取晶胞进行分析,图中虚线所给结构为晶胞底面,两层间距离为晶胞的高,则每个晶胞中碘原子的个数是$(4+4) × \frac{1}{2}=4$,每个晶胞中平均含有2个$ I_2$分子,晶胞的体积是$a b d × 10^{-30} cm^3$,碘晶体的密度是$\frac{2 × 254}{a b d × N_{ A} × 10^{-30}} g · cm^{-3}$,D项正确。
命题意图本题通过碘晶体结构分析,考查晶体类型判断、卤键性质及晶胞密度计算,体现了“证据推理与模型认知”等化学学科核心素养。
解题思路由图示碘晶体的单层结构可知,层内分子间存在“卤键”(类似氢键)和范德华力,层间作用为范德华力,则碘晶体是分子晶体,而不是混合型晶体,A项错误。类比水,在固态水和液态水分子之间都存在氢键,则液态碘单质中也存在“卤键”,B项正确。由图可知,每个$ I_2$分子连有4个“卤键”,每个“卤键”被2个碘分子共用,由均摊法知,1个$ I_2$分子“占有”2个“卤键”,C项正确。从相邻两层碘分子中选取晶胞进行分析,图中虚线所给结构为晶胞底面,两层间距离为晶胞的高,则每个晶胞中碘原子的个数是$(4+4) × \frac{1}{2}=4$,每个晶胞中平均含有2个$ I_2$分子,晶胞的体积是$a b d × 10^{-30} cm^3$,碘晶体的密度是$\frac{2 × 254}{a b d × N_{ A} × 10^{-30}} g · cm^{-3}$,D项正确。
查看更多完整答案,请扫码查看


