第69页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
19. (8分)生病住院时医生常采用输液治疗,即将药物溶解在生理盐水(溶质质量分数为0.9%的氯化钠溶液)中进行输液。现需500g生理盐水,请根据已学知识回答:
(1)需称取氯化钠固体
(2)下列配制溶液的操作顺序正确的是
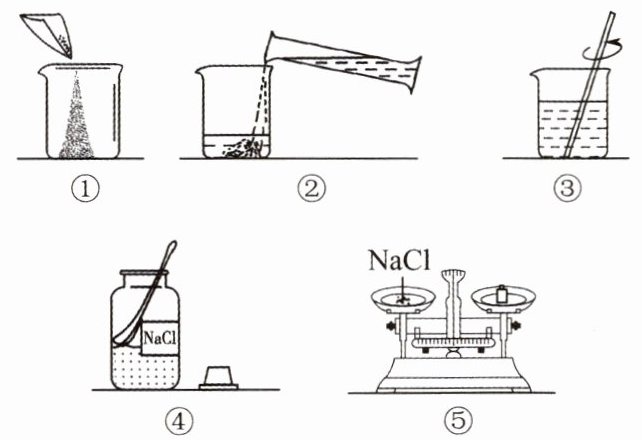
A. ④⑤①②③
B. ①②③④⑤
C. ⑤②①④③
D. ③④①②⑤
(3)上图中玻璃棒的作用是
(4)若上述生理盐水用10%的氯化钠溶液加水稀释而得到,则需10%的氯化钠溶液
(5)若所配500g 0.9%氯化钠溶液中溶质的质量分数偏小(1g以下用游码),则可能的原因有
A. 用托盘天平称取时,左边放砝码右边放氯化钠
B. 用量筒量取水时仰视读数
C. 转移已配好的溶液时,有少量液体溅出
D. 烧杯用蒸馏水润洗后再配制溶液
(1)需称取氯化钠固体
4.5
g,量取水的体积为495.5
mL。(2)下列配制溶液的操作顺序正确的是
A
(填字母)。
A. ④⑤①②③
B. ①②③④⑤
C. ⑤②①④③
D. ③④①②⑤
(3)上图中玻璃棒的作用是
搅拌,加快氯化钠的溶解
;若称取固体时,托盘天平的指针略微向右偏移,则需要进行的操作是加氯化钠固体直至天平平衡
。(4)若上述生理盐水用10%的氯化钠溶液加水稀释而得到,则需10%的氯化钠溶液
45
g;已知20℃时氯化钠的溶解度为36g,则生理盐水属于不饱和
(填“饱和”或“不饱和”)溶液。(5)若所配500g 0.9%氯化钠溶液中溶质的质量分数偏小(1g以下用游码),则可能的原因有
ABD
(填字母)。A. 用托盘天平称取时,左边放砝码右边放氯化钠
B. 用量筒量取水时仰视读数
C. 转移已配好的溶液时,有少量液体溅出
D. 烧杯用蒸馏水润洗后再配制溶液
答案:
(1)4.5 495.5
(2)A
(3)搅拌,加快氯化钠的溶解 加氯化钠固体直至天平平衡
(4)45 不饱和
(5)ABD
(1)4.5 495.5
(2)A
(3)搅拌,加快氯化钠的溶解 加氯化钠固体直至天平平衡
(4)45 不饱和
(5)ABD
20. (10分)二水合氯化钙是一种食品钙质强化剂,工业上可用大理石(含有氧化铁、氧化镁和二氧化硅等杂质)生产,其工艺流程如下:

查阅资料可知:二氧化硅不溶于水,也不与酸反应。
(1)滤渣a的化学式为
(2)请写出产生气体a的化学方程式:
(3)“②调节pH”时,溶液的pH
(4)“③结晶”过程的操作:蒸发浓缩、

查阅资料可知:二氧化硅不溶于水,也不与酸反应。
(1)滤渣a的化学式为
SiO₂
,固体b俗称干冰
。(2)请写出产生气体a的化学方程式:
CaCO₃+2HCl=CaCl₂+H₂O+CO₂↑
。(3)“②调节pH”时,溶液的pH
增大
(填“增大”“减小”或“不变”);其中发生中和反应的化学方程式是2HCl+Ca(OH)₂=CaCl₂+2H₂O
;滤渣b的成分是Mg(OH)₂和Fe(OH)₃
(写化学式)。(4)“③结晶”过程的操作:蒸发浓缩、
降温结晶
、过滤、洗涤、干燥。实验室进行蒸发时,玻璃棒搅拌的作用是防止局部温度过高造成液体飞溅
。
答案:
(1)SiO₂ 干冰
(2)CaCO₃+2HCl=CaCl₂+H₂O+CO₂↑
(3)增大 2HCl+Ca(OH)₂=CaCl₂+2H₂O Mg(OH)₂和Fe(OH)₃
(4)降温结晶 防止局部温度过高造成液体飞溅
(1)SiO₂ 干冰
(2)CaCO₃+2HCl=CaCl₂+H₂O+CO₂↑
(3)增大 2HCl+Ca(OH)₂=CaCl₂+2H₂O Mg(OH)₂和Fe(OH)₃
(4)降温结晶 防止局部温度过高造成液体飞溅
21. (10分)某校化学兴趣小组的同学们在实验室意外发现实验桌上有一瓶敞口放置的氢氧化钠固体,根据所学化学知识,他们认为此瓶氢氧化钠固体变质了,接着他们对这瓶氢氧化钠固体的变质情况进行了探究。
【提出问题】氢氧化钠固体的变质程度如何?
【猜想与假设】(1)甲同学猜想:氢氧化钠可能部分变质,固体为______(写化学式,下同)。乙同学猜想:氢氧化钠可能全部变质,固体为______。
【实验探究】(2)他们设计探究实验方案,探究过程如下,请完成下列表格。
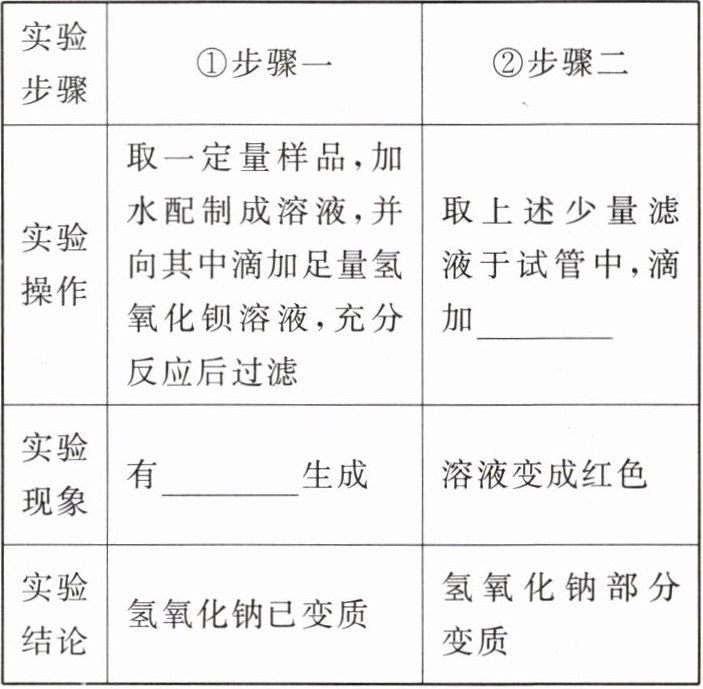
【得出结论】甲同学的猜想正确。
【表达交流】(3)丙同学认为通过上述实验不能得出甲同学的猜想正确,需要对上述实验操作作出一些修改,修改的内容为______。修改完成后,他们三人合作完成了实验,得出“该NaOH固体部分变质”的结论。
【拓展延伸】(4)为进一步确定该NaOH固体中$Na_2CO_3$的质量分数,三人再取一定量该样品,做了如图所示的补充实验。(已知:碱石灰是氢氧化钠和氧化钙组成的混合物)
①装置A的作用是______。

②待B中反应结束后还需要再通一次空气,其目的是______。
③若要得出$Na_2CO_3$的质量分数,除需要称量样品的质量外,还需称量______(填字母)装置反应前、后的质量。
【反思与评价】(5)导致氢氧化钠固体变质的原因是______(写化学方程式)。
【提出问题】氢氧化钠固体的变质程度如何?
【猜想与假设】(1)甲同学猜想:氢氧化钠可能部分变质,固体为______(写化学式,下同)。乙同学猜想:氢氧化钠可能全部变质,固体为______。
【实验探究】(2)他们设计探究实验方案,探究过程如下,请完成下列表格。

【得出结论】甲同学的猜想正确。
【表达交流】(3)丙同学认为通过上述实验不能得出甲同学的猜想正确,需要对上述实验操作作出一些修改,修改的内容为______。修改完成后,他们三人合作完成了实验,得出“该NaOH固体部分变质”的结论。
【拓展延伸】(4)为进一步确定该NaOH固体中$Na_2CO_3$的质量分数,三人再取一定量该样品,做了如图所示的补充实验。(已知:碱石灰是氢氧化钠和氧化钙组成的混合物)
①装置A的作用是______。

②待B中反应结束后还需要再通一次空气,其目的是______。
③若要得出$Na_2CO_3$的质量分数,除需要称量样品的质量外,还需称量______(填字母)装置反应前、后的质量。
【反思与评价】(5)导致氢氧化钠固体变质的原因是______(写化学方程式)。
答案:
(1)Na₂CO₃和NaOH Na₂CO₃
(2)①白色沉淀 ②无色酚酞试液
(3)把足量氢氧化钡溶液改为足量氯化钡溶液
(4)①除去空气中的二氧化碳,防止其对实验造成干扰 ②使生成的二氧化碳全部被D装置吸收 ③D
(5)CO₂+2NaOH=Na₂CO₃+H₂O
(1)Na₂CO₃和NaOH Na₂CO₃
(2)①白色沉淀 ②无色酚酞试液
(3)把足量氢氧化钡溶液改为足量氯化钡溶液
(4)①除去空气中的二氧化碳,防止其对实验造成干扰 ②使生成的二氧化碳全部被D装置吸收 ③D
(5)CO₂+2NaOH=Na₂CO₃+H₂O
查看更多完整答案,请扫码查看


