第60页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
6. 下列各组物质的溶液不用其他试剂,只用观察和组内物质相互混合的方法,就能将它们一一鉴别出来的是(
A.NaCl、H₂SO₄、CuSO₄、MgCl₂
B.CaCl₂、AgNO₃、MgCl₂、CuCl₂
C.Na₂SO₄、Na₂CO₃、NaCl、稀盐酸
D.Na₂CO₃、BaCl₂、Na₂SO₄、稀盐酸
D
)A.NaCl、H₂SO₄、CuSO₄、MgCl₂
B.CaCl₂、AgNO₃、MgCl₂、CuCl₂
C.Na₂SO₄、Na₂CO₃、NaCl、稀盐酸
D.Na₂CO₃、BaCl₂、Na₂SO₄、稀盐酸
答案:
D
7. 有A~E五种稀溶液,分别为氢氧化钙溶液、氢氧化钠溶液、氯化钠溶液、碳酸钠溶液、稀盐酸中的一种。各取少量溶液两两混合,可以观察到:A + E→无色气体,B + E→白色沉淀,其余无明显现象。回答下列问题。
(1)A为
(2)A与E反应的化学方程式为
(3)B与E反应的化学方程式为
(4)对还没有确定的两种溶液,下列鉴别方法可行的是
①分别滴加无色酚酞试液
②分别滴加氯化镁溶液
③分别加入铁粉
(1)A为
稀盐酸
。(2)A与E反应的化学方程式为
Na₂CO₃+2HCl=2NaCl+H₂O+CO₂↑
。(3)B与E反应的化学方程式为
Na₂CO₃+Ca(OH)₂=2NaOH+CaCO₃↓
。(4)对还没有确定的两种溶液,下列鉴别方法可行的是
①②
(填序号)。①分别滴加无色酚酞试液
②分别滴加氯化镁溶液
③分别加入铁粉
答案:
(1)稀盐酸
(2)Na₂CO₃+2HCl=2NaCl+H₂O+CO₂↑
(3)Na₂CO₃+Ca(OH)₂=2NaOH+CaCO₃↓
(4)①②
(1)稀盐酸
(2)Na₂CO₃+2HCl=2NaCl+H₂O+CO₂↑
(3)Na₂CO₃+Ca(OH)₂=2NaOH+CaCO₃↓
(4)①②
8. 某工业园区甲、乙两化工厂排放的废水中含有K⁺、Cu²⁺、Fe³⁺、Cl⁻、OH⁻、NO₃⁻六种离子,甲厂含有其中的三种,乙厂含有另外三种,两厂废水的直接排放对当地水质造成严重影响。某课外实践小组对两厂废水进行实地检测,发现甲厂废水呈碱性。
(1)甲厂废水中一定含有的离子是
(2)经课外实践小组多次实验,发现两厂废水按适当比例混合,可将废水中的某些离子转化为沉淀,这些离子分别是
(1)甲厂废水中一定含有的离子是
OH⁻
(填离子符号,下同),可能含有的离子是Cl⁻(或NO₃⁻)
。(2)经课外实践小组多次实验,发现两厂废水按适当比例混合,可将废水中的某些离子转化为沉淀,这些离子分别是
Cu²⁺、Fe³⁺、OH⁻
;过滤后的废水中主要含有KCl、KNO₃
(填化学式)两种物质,处理后的废水符合排放标准。
答案:
(1)OH⁻;Cl⁻(或NO₃⁻)
(2)Cu²⁺、Fe³⁺、OH⁻;KCl、KNO₃
(1)OH⁻;Cl⁻(或NO₃⁻)
(2)Cu²⁺、Fe³⁺、OH⁻;KCl、KNO₃
9. 兴趣小组的同学为探究在空气中久置的某氢氧化钠样品是否变质,设计了如图所示的A、B、C、D四组探究实验。
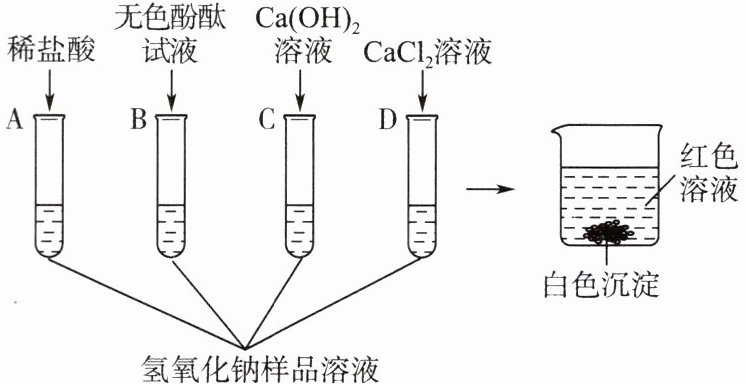
【查阅资料】氯化钙、氯化钡溶液都呈中性。
【实验探究】取适量该氢氧化钠样品,加足量的水溶解,将得到的溶液分别加入四支试管中。向四支试管中分别加入稀盐酸(足量)、无色酚酞试液、$Ca(OH)_2$溶液、$CaCl_2$溶液(如图所示)。
【分析与结论】(1)上述四组实验中,不能达到实验目的的是____(填字母)。
(2)实验A中,观察到____(填实验现象),说明该氢氧化钠样品已经变质。
(3)实验D中,证明该氢氧化钠样品已经变质的反应的化学方程式是____。
【继续探究】实验结束后,同学们将四支试管中反应后的混合物全部倒入一个洁净的大烧杯中(如图所示),充分搅拌、静置,观察到烧杯内上层清液呈红色,下层有白色沉淀。
【提出问题】上层清液呈红色,说明溶液呈碱性;上层清液中呈碱性的物质是什么?
【猜想与假设】上层清液中呈碱性的物质可能是碳酸钠、氢氧化钙和____三种物质中的一种或两种。
【设计实验】取少量烧杯中的上层清液于试管中,加入过量的氯化钡溶液,观察现象。
【现象与结论】

【实验反思】同学们认为上述预测现象②所得结论不严谨,原因是____。

【查阅资料】氯化钙、氯化钡溶液都呈中性。
【实验探究】取适量该氢氧化钠样品,加足量的水溶解,将得到的溶液分别加入四支试管中。向四支试管中分别加入稀盐酸(足量)、无色酚酞试液、$Ca(OH)_2$溶液、$CaCl_2$溶液(如图所示)。
【分析与结论】(1)上述四组实验中,不能达到实验目的的是____(填字母)。
(2)实验A中,观察到____(填实验现象),说明该氢氧化钠样品已经变质。
(3)实验D中,证明该氢氧化钠样品已经变质的反应的化学方程式是____。
【继续探究】实验结束后,同学们将四支试管中反应后的混合物全部倒入一个洁净的大烧杯中(如图所示),充分搅拌、静置,观察到烧杯内上层清液呈红色,下层有白色沉淀。
【提出问题】上层清液呈红色,说明溶液呈碱性;上层清液中呈碱性的物质是什么?
【猜想与假设】上层清液中呈碱性的物质可能是碳酸钠、氢氧化钙和____三种物质中的一种或两种。
【设计实验】取少量烧杯中的上层清液于试管中,加入过量的氯化钡溶液,观察现象。
【现象与结论】

【实验反思】同学们认为上述预测现象②所得结论不严谨,原因是____。
答案:
【分析与结论】
(1)B
(2)有气泡产生
(3)CaCl₂+Na₂CO₃=CaCO₃↓+2NaCl 【猜想与假设】氢氧化钠 【现象与结论】Na₂CO₃、NaOH
【实验反思】加入BaCl₂不产生沉淀,溶液显红色说明溶液呈碱性;除Ca(OH)₂外,NaOH溶于水也显碱性,使溶液呈红色
(1)B
(2)有气泡产生
(3)CaCl₂+Na₂CO₃=CaCO₃↓+2NaCl 【猜想与假设】氢氧化钠 【现象与结论】Na₂CO₃、NaOH
【实验反思】加入BaCl₂不产生沉淀,溶液显红色说明溶液呈碱性;除Ca(OH)₂外,NaOH溶于水也显碱性,使溶液呈红色
查看更多完整答案,请扫码查看


