2025年奔跑吧少年九年级科学全一册浙教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年奔跑吧少年九年级科学全一册浙教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
【例2】小舟归纳了金属及其化合物之间的部分转化关系,如图所示。
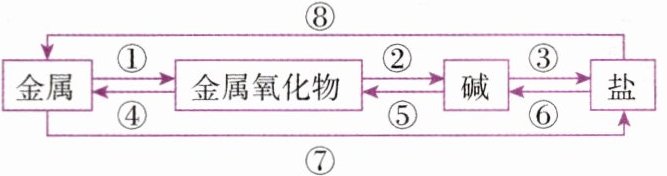
(1)请写出符合图中转化规律①的化学方程式:
(2)我国古代劳动人民最早发明使用湿法炼铜。湿法炼铜的步骤如下:第一步,用硫酸将铜矿中的铜转变为可溶性的硫酸铜;第二步,将铁放入硫酸铜溶液中把铜置换出来。其中利用了图中转化规律⑧的是第
注意点2 一般情况下,仅可溶性碱(如氢氧化钠、氢氧化钙、氢氧化钾、氢氧化钡)可由对应的金属氧化物和水化合生成;仅难溶性碱受热能分解成相应的金属氧化物和水。

(1)请写出符合图中转化规律①的化学方程式:
$2Mg+{O}_{2}\xlongequal{点燃\phantom{\rule[-.2em]{0ex}{0ex}}}2MgO$
(写出一个)。(2)我国古代劳动人民最早发明使用湿法炼铜。湿法炼铜的步骤如下:第一步,用硫酸将铜矿中的铜转变为可溶性的硫酸铜;第二步,将铁放入硫酸铜溶液中把铜置换出来。其中利用了图中转化规律⑧的是第
二
步,请写出此步的化学方程式:$Fe+CuS{O}_{4}\xlongequal{\;\;}FeS{O}_{4}+Cu$
。注意点2 一般情况下,仅可溶性碱(如氢氧化钠、氢氧化钙、氢氧化钾、氢氧化钡)可由对应的金属氧化物和水化合生成;仅难溶性碱受热能分解成相应的金属氧化物和水。
答案:
【例2】
(1)$2Mg+{O}_{2}\xlongequal{点燃\phantom{\rule[-.2em]{0ex}{0ex}}}2MgO$(合理均可)
(2)二 $Fe+CuS{O}_{4}\xlongequal{\;\;}FeS{O}_{4}+Cu$
(1)$2Mg+{O}_{2}\xlongequal{点燃\phantom{\rule[-.2em]{0ex}{0ex}}}2MgO$(合理均可)
(2)二 $Fe+CuS{O}_{4}\xlongequal{\;\;}FeS{O}_{4}+Cu$
1. 金属的冶炼。
含氧化合物里的氧被夺取的反应,叫作

含氧化合物里的氧被夺取的反应,叫作
还原
反应。碳、氢气和一氧化碳等能从氧化铜、氧化铁中夺取氧的能力叫还原性,具有还原性的物质可作还原剂。
答案:
还原 游离 化合 化合 游离 碳 氧
2. 碳还原氧化铜。
(1) 碳和金属氧化物在高温下反应,碳能夺取金属氧化物中的氧。
${C + 2CuO\xlongequal{高温}}$
(2) CO能夺取金属氧化物中的氧。
${CO + CuO\xlongequal{\triangle}Cu + }$
(1) 碳和金属氧化物在高温下反应,碳能夺取金属氧化物中的氧。
${C + 2CuO\xlongequal{高温}}$
$CO_{2}\uparrow$
${ + 2Cu}$(2) CO能夺取金属氧化物中的氧。
${CO + CuO\xlongequal{\triangle}Cu + }$
$CO_{2}$
答案:
(1)$CO_{2}\uparrow$
(2)$CO_{2}$
(1)$CO_{2}\uparrow$
(2)$CO_{2}$
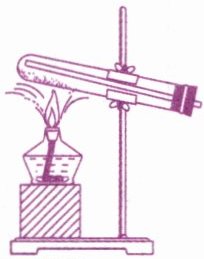
3. 氢气还原氧化铜。
(1) 化学方程式:
(2) 实验现象:黑色固体变为
(3) 实验装置及要点。
① 试管口向下倾斜的目的是避免
② 导管插到试管底部,一是为了让$${CuO}$与${H_{2}}$$
③ 实验前,先通氢气,后点燃酒精灯加热,防止氢气和空气混合加热时发生
(4) 巧记:氢气早出晚归,酒精灯迟到早退,前者颠倒会爆炸,后者颠倒要氧化。
(1) 化学方程式:
$CuO+H_{2}\xlongequal {△}Cu+H_{2}O$
。(2) 实验现象:黑色固体变为
红色
,试管口出现小水珠
。(3) 实验装置及要点。
① 试管口向下倾斜的目的是避免
反应生成的水倒流而使试管炸裂
。② 导管插到试管底部,一是为了让$${CuO}$与${H_{2}}$$
充分反应
,二是为了把试管底部的空气
排出,防止发生爆炸③ 实验前,先通氢气,后点燃酒精灯加热,防止氢气和空气混合加热时发生
爆炸
;实验后,先熄灭酒精灯,待试管冷却后,再停止通入氢气,防止生成的铜在温度较高时再次被氧气氧化
。(4) 巧记:氢气早出晚归,酒精灯迟到早退,前者颠倒会爆炸,后者颠倒要氧化。

答案:
(1)$CuO+H_{2}\xlongequal {△}Cu+H_{2}O$
(2)红色 小水珠
(3)①反应生成的水倒流而使试管炸裂 ②充分反应 空气 ③爆炸 氧化
(1)$CuO+H_{2}\xlongequal {△}Cu+H_{2}O$
(2)红色 小水珠
(3)①反应生成的水倒流而使试管炸裂 ②充分反应 空气 ③爆炸 氧化
4. 金属冶炼主要是指将金属氧化物转化为金属的过程。生铁的冶炼就是用CO还原氧化铁。
${3CO + Fe_{2}O_{3}\xlongequal{高温}2Fe + }$
${3CO + Fe_{2}O_{3}\xlongequal{高温}2Fe + }$
$3CO_{2}$
(铁矿石炼铁的主要反应原理)
答案:
$3CO_{2}$
5. 判断下列说法是否正确(正确的画“√”,错误的画“×”)。
(1) 金属冶炼就是要把金属从混合物中提取出来。 (
(2) 金属氧化物变成金属单质,发生了还原反应。 (
(3) 在氢气还原氧化铜的实验中,要先通一会儿氢气再点燃酒精灯。 (
(4) $${CO + CuO\xlongequal{\triangle}Cu + CO_{2}}$$利用了CO的还原性来冶炼铜,是置换反应。 (
(5) 氧化铁、氧化铜能用$${H_{2}}$$、CO等进行还原,所以只要是金属氧化物都能被$${H_{2}}$$、CO还原成金属单质。 (
(1) 金属冶炼就是要把金属从混合物中提取出来。 (
×
)(2) 金属氧化物变成金属单质,发生了还原反应。 (
√
)(3) 在氢气还原氧化铜的实验中,要先通一会儿氢气再点燃酒精灯。 (
√
)(4) $${CO + CuO\xlongequal{\triangle}Cu + CO_{2}}$$利用了CO的还原性来冶炼铜,是置换反应。 (
×
)(5) 氧化铁、氧化铜能用$${H_{2}}$$、CO等进行还原,所以只要是金属氧化物都能被$${H_{2}}$$、CO还原成金属单质。 (
×
)
答案:
(1)×
(2)√
(3)√
(4)×
(5)×
(1)×
(2)√
(3)√
(4)×
(5)×
查看更多完整答案,请扫码查看


