2025年课堂新坐标高中同步导学案高中化学选择性必修第一册苏教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年课堂新坐标高中同步导学案高中化学选择性必修第一册苏教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第76页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
四、压强变化对化学平衡的影响
1. 压强对平衡移动的影响的实例探讨

2. 结论
对于有气体参加的可逆反应:$ aA(g) ⇌ bB(g) $,其平衡常数$ K = $

[特别提醒] 对于只有固体或液体参加的反应,反应前后气体分子数不变的反应,改变压强,平衡不发生移动。
1. 压强对平衡移动的影响的实例探讨

2. 结论
对于有气体参加的可逆反应:$ aA(g) ⇌ bB(g) $,其平衡常数$ K = $
$\frac{c^{b}(B)}{c^{a}(A)}$
,改变体系压强时:
[特别提醒] 对于只有固体或液体参加的反应,反应前后气体分子数不变的反应,改变压强,平衡不发生移动。
答案:
1.正 逆 逆 正 不 不$ 2.\frac{c^{b}(B)}{c^{a}(A)} $正向 不 逆向
判一判 (正确的打“√”,错误的打“×”)
(1) 有气体参与的反应,改变压强,平衡一定发生移动。(
(2) 增大压强可使$ {2SO_{2}(g) + O_{2}(g) \xlongequal[\Delta]{ 催化剂} 2SO_{3}(g)} $平衡向正反应方向移动,原因是增大压强,$ v_{ 正} $增大,$ v_{ 逆} $减小。(
(3) 对$ {CO(g) + H_{2}O(g) ⇌ CO_{2}(g) + H_{2}(g)} $,在其他条件不变时,改变压强,平衡不移动。(
(4) 对$ {2HI(g) ⇌ H_{2}(g) + I_{2}(g)} $,其他条件不变时,增大压强,体系的颜色加深,平衡正向移动。(
(1) 有气体参与的反应,改变压强,平衡一定发生移动。(
×
)(2) 增大压强可使$ {2SO_{2}(g) + O_{2}(g) \xlongequal[\Delta]{ 催化剂} 2SO_{3}(g)} $平衡向正反应方向移动,原因是增大压强,$ v_{ 正} $增大,$ v_{ 逆} $减小。(
×
)(3) 对$ {CO(g) + H_{2}O(g) ⇌ CO_{2}(g) + H_{2}(g)} $,在其他条件不变时,改变压强,平衡不移动。(
√
)(4) 对$ {2HI(g) ⇌ H_{2}(g) + I_{2}(g)} $,其他条件不变时,增大压强,体系的颜色加深,平衡正向移动。(
×
)
答案:
(1)×
(2)×
(3)√
(4)×
(1)×
(2)×
(3)√
(4)×
五、温度变化对化学平衡的影响
1. 实验探究
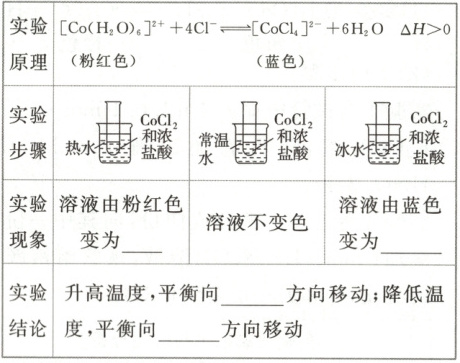
2. 结论(其他条件不变化时)
升高温度,化学平衡向
降低温度,化学平衡向
[特别提醒] 温度变化,化学平衡一定会发生移动。
1. 实验探究

2. 结论(其他条件不变化时)
升高温度,化学平衡向
吸热
反应方向移动;降低温度,化学平衡向
放热
反应方向移动。[特别提醒] 温度变化,化学平衡一定会发生移动。
答案:
1.蓝色 粉红色 正反应 逆反应 2.吸热 放热
判一判 (正确的打“√”,错误的打“×”)
(1) 温度可以影响任意可逆反应的化学平衡状态。(
(2) 升高温度,反应速率加快,化学平衡正向移动。(
(3) 升高温度,反应速率加快,但反应物的转化率可能降低。(
(4) 升高温度,化学平衡常数增大。(
(1) 温度可以影响任意可逆反应的化学平衡状态。(
√
)(2) 升高温度,反应速率加快,化学平衡正向移动。(
×
)(3) 升高温度,反应速率加快,但反应物的转化率可能降低。(
√
)(4) 升高温度,化学平衡常数增大。(
×
)
答案:
(1)√
(2)×
(3)√
(4)×
(1)√
(2)×
(3)√
(4)×
六、催化剂对化学平衡的影响
加入催化剂可以大大地加快反应速率,是因为它可以降低反应所需
[特别提醒] 催化剂不能改变达到化学平衡状态时反应混合物的组成,但是使用催化剂能同等程度地增大正、逆反应速率,缩短达到平衡所需要的时间。
加入催化剂可以大大地加快反应速率,是因为它可以降低反应所需
活化能
,从而提高活化分子百分含量
,从而增大反应速率,但是由于催化剂能够同等程度
地改变正、逆反应速率,因此它对化学平衡移动无
影响。[特别提醒] 催化剂不能改变达到化学平衡状态时反应混合物的组成,但是使用催化剂能同等程度地增大正、逆反应速率,缩短达到平衡所需要的时间。
答案:
活化能 百分含量 同等程度 无
查看更多完整答案,请扫码查看


