第4页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
1. 盐酸是HCl气体的水溶液,属于
混合物
(填“混合物”或“纯净物”)。由于浓盐酸具有挥发性
,挥发出的HCl气体与空气中的水蒸气形成盐酸的小液滴,所以会看到白雾
。浓盐酸敞口放置质量会变小
,溶质的质量分数会变小
,使用后要及时把试剂瓶盖好。
答案:
1.混合物 挥发性 白雾 变小 变小
2. 在稀盐酸中加入下列哪种物质,溶液pH几乎不变的是(
A.AgNO₃溶液
B.CaCO₃固体
C.KOH溶液
D.生石灰(CaO)
A
)A.AgNO₃溶液
B.CaCO₃固体
C.KOH溶液
D.生石灰(CaO)
答案:
2.A
3. 酸溶液中都含有大量H⁺,因此不同酸表现出一些共同的性质。下列关于盐酸性质的描述中,不属于酸的共性的是(
A.能与硝酸银溶液反应生成白色沉淀
B.能使紫色石蕊试液变为红色
C.能与氧化铜反应使溶液变蓝色
D.能与铁反应生成氢气
A
)A.能与硝酸银溶液反应生成白色沉淀
B.能使紫色石蕊试液变为红色
C.能与氧化铜反应使溶液变蓝色
D.能与铁反应生成氢气
答案:
3.A
4. 学习了盐酸的化学性质后,小凯构建了下面的知识网络图。请回答:
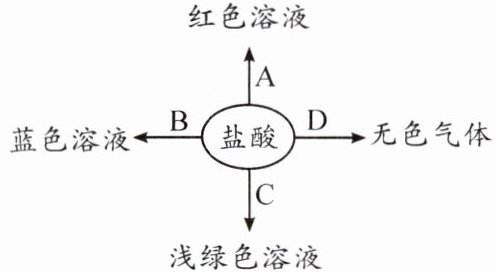
(1) 试剂A的名称是
(2) 若B是一种氧化物,写出盐酸与B反应的化学方程式:
(3) 若C是一种单质,则C的化学式为:
(4) 若D是碳酸钙,则生成无色气体的化学方程式为:

(1) 试剂A的名称是
紫色石蕊试液
。(2) 若B是一种氧化物,写出盐酸与B反应的化学方程式:
CuO+2HCl=CuCl₂+H₂O
。(3) 若C是一种单质,则C的化学式为:
Fe
。(4) 若D是碳酸钙,则生成无色气体的化学方程式为:
CaCO₃+2HCl=CaCl₂+CO₂↑+H₂O
。
答案:
4.
(1)紫色石蕊试液
(2)CuO+2HCl=CuCl₂+H₂O
(3)Fe
(4)CaCO₃+2HCl=CaCl₂+CO₂↑+H₂O
(1)紫色石蕊试液
(2)CuO+2HCl=CuCl₂+H₂O
(3)Fe
(4)CaCO₃+2HCl=CaCl₂+CO₂↑+H₂O
5. 四只烧杯中均盛有稀盐酸,并滴加了数滴紫色石蕊试液。现向这四只烧杯中不断加入下列物质,直至过量,其中能使溶液最后呈紫色的是(
A.Mg(OH)₂
B.NaOH
C.Na₂SO₄
D.CaO
A
)A.Mg(OH)₂
B.NaOH
C.Na₂SO₄
D.CaO
答案:
5.A
6. 向盛有稀盐酸的烧杯中逐滴加入NaOH溶液,测得烧杯中溶液的pH变化如图所示,下列说法正确的是(
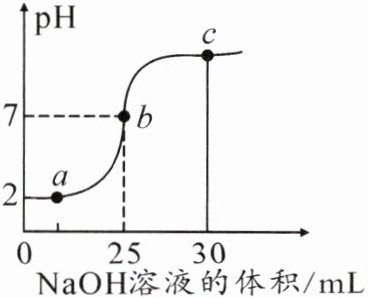
A.a点所示的溶液中含有的溶质是NaOH和NaCl
B.a、b、c点所示的溶液中都含有Na⁺、Cl⁻
C.c点表示NaOH和稀盐酸恰好完全反应
D.b点所示的溶液能使紫色石蕊试液变红
B
)
A.a点所示的溶液中含有的溶质是NaOH和NaCl
B.a、b、c点所示的溶液中都含有Na⁺、Cl⁻
C.c点表示NaOH和稀盐酸恰好完全反应
D.b点所示的溶液能使紫色石蕊试液变红
答案:
6.B
查看更多完整答案,请扫码查看


