第120页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
【变式】实验室用$ {MnO_{2}} $和浓盐酸制取氯气时有如下操作,操作顺序正确的是(
①连接好装置,检查装置气密性
②缓缓加热
③在烧瓶中加入少量的$ {MnO_{2}} $,向分液漏斗中加入浓盐酸
④通过分液漏斗慢慢向烧瓶中注入浓盐酸
⑤将多余的氯气用浓$ {NaOH} $溶液吸收
⑥当有连续气泡冒出时,开始用向上排空气法收集氯气
A. ①②③④⑤⑥
B. ③④②①⑥⑤
C. ①④③②⑥⑤
D. ①③④②⑥⑤
D
)①连接好装置,检查装置气密性
②缓缓加热
③在烧瓶中加入少量的$ {MnO_{2}} $,向分液漏斗中加入浓盐酸
④通过分液漏斗慢慢向烧瓶中注入浓盐酸
⑤将多余的氯气用浓$ {NaOH} $溶液吸收
⑥当有连续气泡冒出时,开始用向上排空气法收集氯气
A. ①②③④⑤⑥
B. ③④②①⑥⑤
C. ①④③②⑥⑤
D. ①③④②⑥⑤
答案:
D 制取氯气的实验操作依次为连接好装置,检查装置气密性,防止装置连接处漏气;向烧瓶中加入固体试剂$MnO_{2}$粉末,从分液漏斗中缓缓加入浓盐酸,加热;待气体均匀放出时收集气体;因氯气有毒,最后将多余的氯气用浓$NaOH$溶液吸收,防止污染空气。
1. 实验室利用如图所示的装置制备氯气,图中涉及气体发生、除杂、干燥、收集、尾气处理装置,其中错误的是(

A. ①②③
B. ①②④
C. ②③④
D. ①③④
C
)
A. ①②③
B. ①②④
C. ②③④
D. ①③④
答案:
C 应用饱和食盐水除去$HCl$,不能用饱和$NaOH$溶液,因为$NaOH$可以与氯气反应,②错误;干燥装置应从长导管进气,否则浓硫酸会被压入其右侧装置,③错误;澄清石灰水中$Ca(OH)_{2}$浓度较低,无法完全吸收氯气,应用氢氧化钠溶液吸收氯气,④错误。
2. 实验室利用浓盐酸和二氧化锰制取氯气,制取装置中应使用分液漏斗而不能使用长颈漏斗,下列有关理由叙述错误的是(
A. 防止氯气扩散到空气中造成污染
B. 便于控制加入浓盐酸的量
C. 便于添加液体
D. 尽量避免氯化氢挥发到空气中
C
)A. 防止氯气扩散到空气中造成污染
B. 便于控制加入浓盐酸的量
C. 便于添加液体
D. 尽量避免氯化氢挥发到空气中
答案:
C 用分液漏斗既可以防止$HCl$和$Cl_{2}$挥发,以防污染环境,同时又可以控制滴加浓盐酸的量和快慢,从而控制反应速率,提高盐酸的利用率。
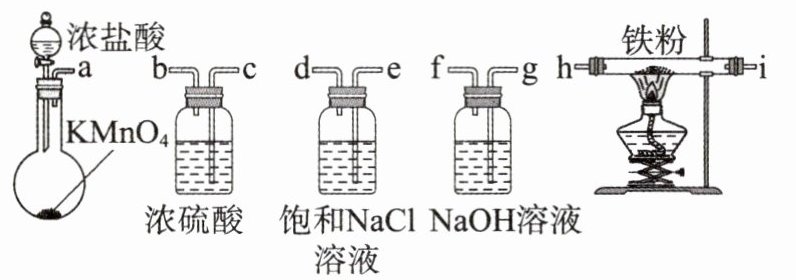
3. 如图所示的仪器可用于实验室制备少量无水$ {FeCl_{3}} $,仪器的连接顺序正确的是(
A. $ {a→b→c→d→e→f→g→h} $
B. $ {a→e→d→c→b→h→i→g} $
C. $ {a→d→e→c→b→h→i→g} $
D. $ {a→c→b→d→e→h→i→f} $
B
)
A. $ {a→b→c→d→e→f→g→h} $
B. $ {a→e→d→c→b→h→i→g} $
C. $ {a→d→e→c→b→h→i→g} $
D. $ {a→c→b→d→e→h→i→f} $
答案:
B 实验室利用铁粉与氯气的反应制备无水$FeCl_{3}$,需要首先制得干燥的氯气,按制气→除$HCl$→除$H_{2}O$→制备$FeCl_{3}$→吸收多余氯气的顺序进行连接。
4. 某校化学兴趣小组为研究$ {Cl_{2}} $的性质,设计如图所示的装置进行实验。装置Ⅲ中夹持装置已略去,其中$ {a} $为干燥的品红试纸,$ {b} $为湿润的品红试纸。

(1)装置Ⅰ中仪器$ {c} $的名称是
(2)装置Ⅱ的作用是
(3)若产生的$ {Cl_{2}} $足量,实验过程中装置Ⅳ中的实验现象是
(4)实验结束后,该组同学在装置Ⅲ中观察到$ {b} $的红色褪去,但是并未观察到“$ {a} $无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在装置Ⅱ与Ⅲ之间添加如图所示的


(1)装置Ⅰ中仪器$ {c} $的名称是
分液漏斗
,实验室用$ {MnO_{2}} $和浓盐酸制取$ {Cl_{2}} $的离子方程式为$MnO_{2}+4H^{+}+2Cl^{-}\xlongequal {△}Mn^{2+}+Cl_{2}\uparrow +2H_{2}O$
。(2)装置Ⅱ的作用是
除去$Cl_{2}$中的$HCl$气体
。(3)若产生的$ {Cl_{2}} $足量,实验过程中装置Ⅳ中的实验现象是
溶液先变红,后褪色
。(4)实验结束后,该组同学在装置Ⅲ中观察到$ {b} $的红色褪去,但是并未观察到“$ {a} $无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在装置Ⅱ与Ⅲ之间添加如图所示的
④
(填序号)装置。
答案:
(1)分液漏斗 $MnO_{2}+4H^{+}+2Cl^{-}\xlongequal {△}Mn^{2+}+Cl_{2}\uparrow +2H_{2}O$
(2)除去$Cl_{2}$中的$HCl$气体
(3)溶液先变红,后褪色
(4)④
【解析】
(2)装置Ⅰ中$MnO_{2}$和浓盐酸反应生成$Cl_{2}$,浓盐酸具有挥发性,制取的$Cl_{2}$中会混有$HCl$气体,用饱和食盐水可以除去杂质$HCl$。
(4)a、b 构成对照实验,干燥的$Cl_{2}$本身没有漂白作用,遇水生成$HClO$,$HClO$具有漂白作用。但是并未观察到“a 无明显变化”这一预期现象,因为$Cl_{2}$未经干燥,本身带有水蒸气,所以需要在装置Ⅱ与Ⅲ之间添加一个干燥装置;碱石灰和浓硫酸是常用的干燥剂,但是$Cl_{2}$会和碱石灰反应,所以应选择浓硫酸。
(1)分液漏斗 $MnO_{2}+4H^{+}+2Cl^{-}\xlongequal {△}Mn^{2+}+Cl_{2}\uparrow +2H_{2}O$
(2)除去$Cl_{2}$中的$HCl$气体
(3)溶液先变红,后褪色
(4)④
【解析】
(2)装置Ⅰ中$MnO_{2}$和浓盐酸反应生成$Cl_{2}$,浓盐酸具有挥发性,制取的$Cl_{2}$中会混有$HCl$气体,用饱和食盐水可以除去杂质$HCl$。
(4)a、b 构成对照实验,干燥的$Cl_{2}$本身没有漂白作用,遇水生成$HClO$,$HClO$具有漂白作用。但是并未观察到“a 无明显变化”这一预期现象,因为$Cl_{2}$未经干燥,本身带有水蒸气,所以需要在装置Ⅱ与Ⅲ之间添加一个干燥装置;碱石灰和浓硫酸是常用的干燥剂,但是$Cl_{2}$会和碱石灰反应,所以应选择浓硫酸。
查看更多完整答案,请扫码查看


