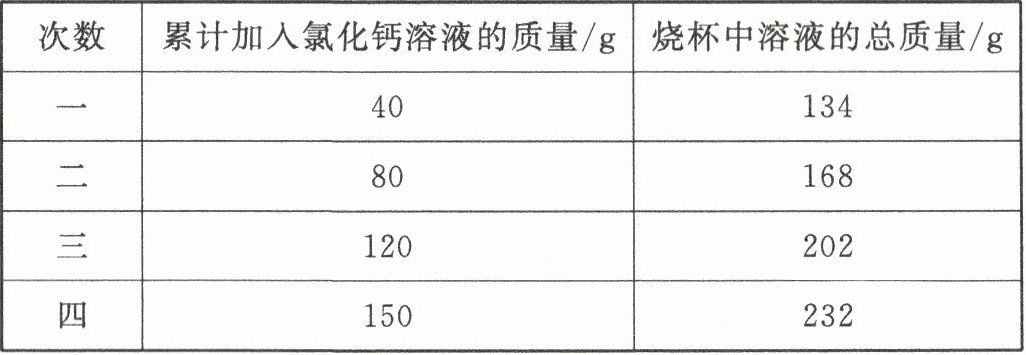
17. 实验室用碳酸钠溶液与氯化钙溶液反应制取高纯度碳酸钙粉末,烧杯中现有 100 g 碳酸钠溶液,将 150 g 氯化钙溶液分四次加入,充分反应,四次测量所得数据如表所示:
(1)恰好完全反应时,生成沉淀的质量为
(2)第四次测量时,溶液中的溶质有
(3)计算氯化钙溶液的溶质质量分数(写出计算过程)。
(1)恰好完全反应时,生成沉淀的质量为
18
g。(2)第四次测量时,溶液中的溶质有
NaCl和CaCl₂
(填化学式)。(3)计算氯化钙溶液的溶质质量分数(写出计算过程)。

答案:
(1)18
(2)NaCl和CaCl₂
(3)解:设氯化钙溶液的溶质质量分数为x。
CaCl₂+Na₂CO₃=CaCO₃↓+2NaCl
111 100
40 g×x (100+40-134)g
$\frac{111}{100}$=$\frac{40\mathrm{g}× x}{(100+40-134)\mathrm{g}}$
x=16.65%
答:氯化钙溶液的溶质质量分数为16.65%。
(1)18
(2)NaCl和CaCl₂
(3)解:设氯化钙溶液的溶质质量分数为x。
CaCl₂+Na₂CO₃=CaCO₃↓+2NaCl
111 100
40 g×x (100+40-134)g
$\frac{111}{100}$=$\frac{40\mathrm{g}× x}{(100+40-134)\mathrm{g}}$
x=16.65%
答:氯化钙溶液的溶质质量分数为16.65%。
查看更多完整答案,请扫码查看


