第98页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
典例示范
例 (2022广州)二甲基亚砜(DMSO)工业废渣含NaNO₃及少量有毒的NaNO₂,以该废渣为原料制备农用KNO₃,既实现资源回收利用又保护了环境。工艺流程如下:
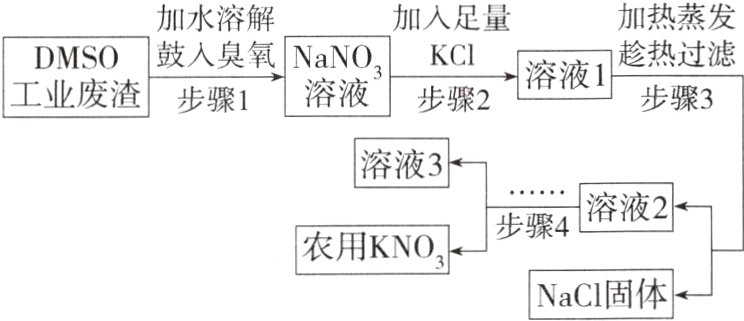
(1)农用KNO₃为农作物提供的营养元素有________________。
(2)步骤1的作用是除去NaNO₂,NaNO₂中氮元素的化合价为__________。
(3)结合溶解度曲线分析,步骤3“加热蒸发”时可控制只析出NaCl固体,原因是______________________________。

0 20 40 60 温度/℃ 80 100
(4)步骤4的操作是__________、过滤。
(5)KCl用量的估算依据是______(填标号)。
A.KCl与NaNO₃的粒子个数比为1∶1
B.KCl与NaNO₃的质量比为1∶1
C.KCl与NaNO₃在溶液中的质量分数之比为1∶1
(6)该工艺所得农用KNO₃混有一定量NaCl。取25 g样品加足量水溶解,向溶液中加入足量的AgNO₃溶液,生成沉淀的质量为14.35 g,则样品中杂质NaCl的质量是__________g,样品含KNO₃__________%(质量分数)。(相对分子质量:KNO₃ 101 NaCl 58.5 AgNO₃ 170 AgCl 143.5)
解析 (5)步骤2中加入KCl的目的是使溶液中的钠离子和氯离子结合形成溶解度较小的氯化钠从而析出,根据KCl、NaNO₃以及NaCl中阴、阳离子个数比可知,KCl和NaNO₃的粒子个数比为1∶1,此时其质量比为74.5∶85。
(6)设样品中NaCl的质量为x,
AgNO₃+NaCl$\xlongequal{\;\;}$NaNO₃+AgCl↓
58.5 143.5
x 14.35 g
$\frac{58.5}{143.5}=\frac{x}{14.35g}$ x = 5.85 g
样品中KNO₃的质量为25 g - 5.85 g = 19.15 g,质量分数为$\frac{19.15g}{25g}$×100% = 76.6%。
答案 (1)钾元素和氮元素 (2)+3 (3)加热至较高温度后,NaCl在溶液中的溶解度最小,随着水分蒸发NaCl固体先析出 (4)降温结晶 (5)A (6)5.85 76.6
例 (2022广州)二甲基亚砜(DMSO)工业废渣含NaNO₃及少量有毒的NaNO₂,以该废渣为原料制备农用KNO₃,既实现资源回收利用又保护了环境。工艺流程如下:

(1)农用KNO₃为农作物提供的营养元素有________________。
(2)步骤1的作用是除去NaNO₂,NaNO₂中氮元素的化合价为__________。
(3)结合溶解度曲线分析,步骤3“加热蒸发”时可控制只析出NaCl固体,原因是______________________________。

0 20 40 60 温度/℃ 80 100
(4)步骤4的操作是__________、过滤。
(5)KCl用量的估算依据是______(填标号)。
A.KCl与NaNO₃的粒子个数比为1∶1
B.KCl与NaNO₃的质量比为1∶1
C.KCl与NaNO₃在溶液中的质量分数之比为1∶1
(6)该工艺所得农用KNO₃混有一定量NaCl。取25 g样品加足量水溶解,向溶液中加入足量的AgNO₃溶液,生成沉淀的质量为14.35 g,则样品中杂质NaCl的质量是__________g,样品含KNO₃__________%(质量分数)。(相对分子质量:KNO₃ 101 NaCl 58.5 AgNO₃ 170 AgCl 143.5)
解析 (5)步骤2中加入KCl的目的是使溶液中的钠离子和氯离子结合形成溶解度较小的氯化钠从而析出,根据KCl、NaNO₃以及NaCl中阴、阳离子个数比可知,KCl和NaNO₃的粒子个数比为1∶1,此时其质量比为74.5∶85。
(6)设样品中NaCl的质量为x,
AgNO₃+NaCl$\xlongequal{\;\;}$NaNO₃+AgCl↓
58.5 143.5
x 14.35 g
$\frac{58.5}{143.5}=\frac{x}{14.35g}$ x = 5.85 g
样品中KNO₃的质量为25 g - 5.85 g = 19.15 g,质量分数为$\frac{19.15g}{25g}$×100% = 76.6%。
答案 (1)钾元素和氮元素 (2)+3 (3)加热至较高温度后,NaCl在溶液中的溶解度最小,随着水分蒸发NaCl固体先析出 (4)降温结晶 (5)A (6)5.85 76.6
答案:
答案
(1)钾元素和氮元素
(2)+3
(3)加热至较高温度后,NaCl在溶液中的溶解度最小,随着水分蒸发NaCl固体先析出
(4)降温结晶
(5)A
(6)5.85 76.6
解析
(5)步骤2中加入KCl的目的是使溶液中的钠离子和氯离子结合形成溶解度较小的氯化钠从而析出,根据KCl、NaNO₃以及NaCl中阴、阳离子个数比可知,KCl和NaNO₃的粒子个数比为1∶1,此时其质量比为74.5∶85。
(6)设样品中NaCl的质量为x,
AgNO₃+NaCl$\xlongequal{\;\;}$NaNO₃+AgCl↓
58.5 143.5
x 14.35 g
$\frac{58.5}{143.5}=\frac{x}{14.35g}$ x = 5.85 g
样品中KNO₃的质量为25 g - 5.85 g = 19.15 g,质量分数为$\frac{19.15g}{25g}$×100% = 76.6%。
(1)钾元素和氮元素
(2)+3
(3)加热至较高温度后,NaCl在溶液中的溶解度最小,随着水分蒸发NaCl固体先析出
(4)降温结晶
(5)A
(6)5.85 76.6
解析
(5)步骤2中加入KCl的目的是使溶液中的钠离子和氯离子结合形成溶解度较小的氯化钠从而析出,根据KCl、NaNO₃以及NaCl中阴、阳离子个数比可知,KCl和NaNO₃的粒子个数比为1∶1,此时其质量比为74.5∶85。
(6)设样品中NaCl的质量为x,
AgNO₃+NaCl$\xlongequal{\;\;}$NaNO₃+AgCl↓
58.5 143.5
x 14.35 g
$\frac{58.5}{143.5}=\frac{x}{14.35g}$ x = 5.85 g
样品中KNO₃的质量为25 g - 5.85 g = 19.15 g,质量分数为$\frac{19.15g}{25g}$×100% = 76.6%。
查看更多完整答案,请扫码查看


