2025年5年高考3年模拟高中化学必修第二册苏教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年5年高考3年模拟高中化学必修第二册苏教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
19.(10分)铝镁合金是轮船制造、化工生产等的重要材料。某研究性学习
小组的三位同学为测定某含镁$3\%\sim5\%$的铝镁合金(不含其他元素)中
镁的质量分数,设计下列两种实验方案进行探究。填写下列空白:
探究一
实验方案:铝镁合金$\xrightarrow{NaOH溶液}$测定剩余固体质量。
(1)实验中发生反应的化学方程式是
。
(2)称取$5.4\ {g}$铝镁合金粉末样品,投入体积为$V\ {mL}$、浓度为$2.0\ {mol· L^{-1}}$
的$NaOH$溶液中,充分反应。为保证合金充分反应,$V\geqslant$
。
(3)过滤、洗涤、干燥、称量固体。该步骤中若未洗涤固体,测得镁的质
量分数将(填“偏大”或“偏小”)。
探究二
实验方案:铝镁合金$\xrightarrow{盐酸}$测定生成气体的体积(实验装置如图所示)。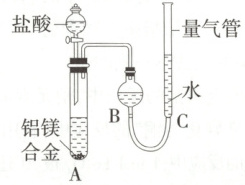
(4)为使测定结果尽可能精确,实验中应注意的问题有:①
,
②。
小组的三位同学为测定某含镁$3\%\sim5\%$的铝镁合金(不含其他元素)中
镁的质量分数,设计下列两种实验方案进行探究。填写下列空白:
探究一
实验方案:铝镁合金$\xrightarrow{NaOH溶液}$测定剩余固体质量。
(1)实验中发生反应的化学方程式是
。
(2)称取$5.4\ {g}$铝镁合金粉末样品,投入体积为$V\ {mL}$、浓度为$2.0\ {mol· L^{-1}}$
的$NaOH$溶液中,充分反应。为保证合金充分反应,$V\geqslant$
。
(3)过滤、洗涤、干燥、称量固体。该步骤中若未洗涤固体,测得镁的质
量分数将(填“偏大”或“偏小”)。
探究二
实验方案:铝镁合金$\xrightarrow{盐酸}$测定生成气体的体积(实验装置如图所示)。

(4)为使测定结果尽可能精确,实验中应注意的问题有:①
,
②。
答案:
(1)2Al + 2NaOH + 2H₂O = 2NaAlO₂ + 3H₂↑
(2)100
(3)偏大
(4)①装置气密性良好
②读数前冷却至室温,且量气管中液面与水准管液面相平
(2)100
(3)偏大
(4)①装置气密性良好
②读数前冷却至室温,且量气管中液面与水准管液面相平
20.(12分)实验室由硫铁矿烧渣(主要成分为${Fe_{2}O_{3}}$、${SiO_{2}}$、${Al_{2}O_{3}}$)制备软
磁性材料$\alpha –{Fe_{2}O_{3}}$。主要转化流程如下:
(1)制绿矾。烧渣到绿矾的工艺中涉及“酸浸”“还原”“除杂”“结晶”
等实验流程。
①酸浸。烧渣酸浸时${Fe_{2}O_{3}}$与稀硫酸反应的化学方程式为
。
②还原。向“酸浸”后的溶液中加入过量铁粉,使${Fe^{3+}}$完全转化为
${Fe^{2+}}$,该过程除生成${Fe^{2+}}$外,还会生成(填化学式);检验${Fe^{3+}}$是否
被完全还原的实验操作是
。
③除杂。向“还原”后的滤液中加入$NaOH$溶液,调节$ pH$,除去${Al^{3+}}$。
④结晶。由${FeSO_{4}}$溶液经一系列操作得到${FeSO_{4}}· 7{H_{2}O}$。
(2)制${FeCO_{3}}$。将${FeSO_{4}}$溶液与氨水-${NH_{4}HCO_{3}}$
混合溶液中的一种加入三颈烧瓶中(装置如图),
通过分液漏斗缓慢滴加另一种溶液,充分反应,
过滤。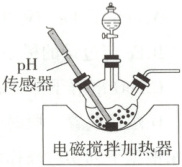
①分液漏斗中的溶液是
;生
成${FeCO_{3}}$的离子方程式为
。
②检验生成的${FeCO_{3}}$沉淀是否洗涤干净的方法是
。
(3)制$\alpha –{Fe_{2}O_{3}}$。将纯净的${FeCO_{3}}$放入管式炉内煅烧$2\ {h}$,获得产
品$\alpha –{Fe_{2}O_{3}}$。
磁性材料$\alpha –{Fe_{2}O_{3}}$。主要转化流程如下:

(1)制绿矾。烧渣到绿矾的工艺中涉及“酸浸”“还原”“除杂”“结晶”
等实验流程。
①酸浸。烧渣酸浸时${Fe_{2}O_{3}}$与稀硫酸反应的化学方程式为
。
②还原。向“酸浸”后的溶液中加入过量铁粉,使${Fe^{3+}}$完全转化为
${Fe^{2+}}$,该过程除生成${Fe^{2+}}$外,还会生成(填化学式);检验${Fe^{3+}}$是否
被完全还原的实验操作是
。
③除杂。向“还原”后的滤液中加入$NaOH$溶液,调节$ pH$,除去${Al^{3+}}$。
④结晶。由${FeSO_{4}}$溶液经一系列操作得到${FeSO_{4}}· 7{H_{2}O}$。
(2)制${FeCO_{3}}$。将${FeSO_{4}}$溶液与氨水-${NH_{4}HCO_{3}}$
混合溶液中的一种加入三颈烧瓶中(装置如图),
通过分液漏斗缓慢滴加另一种溶液,充分反应,
过滤。

①分液漏斗中的溶液是
;生
成${FeCO_{3}}$的离子方程式为
。
②检验生成的${FeCO_{3}}$沉淀是否洗涤干净的方法是
。
(3)制$\alpha –{Fe_{2}O_{3}}$。将纯净的${FeCO_{3}}$放入管式炉内煅烧$2\ {h}$,获得产
品$\alpha –{Fe_{2}O_{3}}$。
答案:
(1)①${Fe2O3 + 3H2SO4 = Fe2(SO4)3 + 3H2O}$
②${H2}$;取少量还原后的溶液,滴加${KSCN}$溶液,若溶液不变红,则${Fe^{3+}}$已完全还原
(2)①氨水-${NH4HCO3}$混合溶液;${Fe^{2+} + 2HCO3^- = FeCO3↓ + CO2↑ + H2O}$
②取最后一次洗涤液,滴加盐酸酸化的${BaCl2}$溶液,若无白色沉淀生成,则沉淀已洗涤干净
(1)①${Fe2O3 + 3H2SO4 = Fe2(SO4)3 + 3H2O}$
②${H2}$;取少量还原后的溶液,滴加${KSCN}$溶液,若溶液不变红,则${Fe^{3+}}$已完全还原
(2)①氨水-${NH4HCO3}$混合溶液;${Fe^{2+} + 2HCO3^- = FeCO3↓ + CO2↑ + H2O}$
②取最后一次洗涤液,滴加盐酸酸化的${BaCl2}$溶液,若无白色沉淀生成,则沉淀已洗涤干净
查看更多完整答案,请扫码查看


