2025年5年高考3年模拟高中化学必修第二册苏教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年5年高考3年模拟高中化学必修第二册苏教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
16.(10分)钛($Ti$)及其合金是理想的高强度、低密度结构材料。以钛渣
(主要成分为${TiO_{2}}$,含少量$V$、$Si$和$Al$的氧化物杂质)为原料,制备金属
钛的工艺流程如下: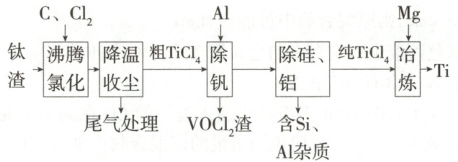
已知:${TiO_{2}}$与$C$、${Cl_{2}}$在$600\ {\degreeCelsius}$的沸腾炉中充分反应后,尾气中每产生
$28\ {g}\ CO$的同时生成$88\ {g}\ {CO_{2}}$。
(1)尾气中$CO$与${CO_{2}}$的物质的量之比为;沸腾氯化过程中
氧化剂是(填化学式)。
(2)该温度下,${TiO_{2}}$与$C$、${Cl_{2}}$反应的总化学方程式为
。
(3)随着温度升高,尾气中$CO$的含量升高,原因是
。
(4)加入$Mg$冶炼$Ti$的化学方程式为
,
该过程要在氩气($Ar$)氛围中进行的原因是
。
(主要成分为${TiO_{2}}$,含少量$V$、$Si$和$Al$的氧化物杂质)为原料,制备金属
钛的工艺流程如下:

已知:${TiO_{2}}$与$C$、${Cl_{2}}$在$600\ {\degreeCelsius}$的沸腾炉中充分反应后,尾气中每产生
$28\ {g}\ CO$的同时生成$88\ {g}\ {CO_{2}}$。
(1)尾气中$CO$与${CO_{2}}$的物质的量之比为;沸腾氯化过程中
氧化剂是(填化学式)。
(2)该温度下,${TiO_{2}}$与$C$、${Cl_{2}}$反应的总化学方程式为
。
(3)随着温度升高,尾气中$CO$的含量升高,原因是
。
(4)加入$Mg$冶炼$Ti$的化学方程式为
,
该过程要在氩气($Ar$)氛围中进行的原因是
。
答案:
(1)1:2;Cl₂
(2)5TiO₂ + 6C + 10Cl₂ $\xlongequal{600℃}$ 5TiCl₄ + 2CO + 4CO₂
(3)温度升高,C与CO₂反应生成更多CO(或高温下更易生成CO)
(4)TiCl₄ + 2Mg $\xlongequal{高温}$ Ti + 2MgCl₂;防止Mg和Ti被空气中的氧气氧化
(1)1:2;Cl₂
(2)5TiO₂ + 6C + 10Cl₂ $\xlongequal{600℃}$ 5TiCl₄ + 2CO + 4CO₂
(3)温度升高,C与CO₂反应生成更多CO(或高温下更易生成CO)
(4)TiCl₄ + 2Mg $\xlongequal{高温}$ Ti + 2MgCl₂;防止Mg和Ti被空气中的氧气氧化
17.(11分)${FeSO_{4}}$是常见的补铁药物,可用于各种原因引起的缺铁性贫血。
请用所学的相关知识,回答下列问题:
(1)长期放置的${FeSO_{4}}$溶液易被溶液中溶解的氧气(填“氧化”
或“还原”)而变质。
(2)某实验小组设计实验方案检验${FeSO_{4}}$溶液的变质情况,进行了如下实验:
③若要使变质的${FeSO_{4}}$复原,方法是
(用离子方程式表示)。
(3)设计实验继续探究${FeSO_{4}}$性质。

②对实验Ⅱ所得白色沉淀进行研究(已知${Fe^{2+}}$与${HCO^{-}_{3}}$在溶液中不能
大量共存)。
操作ⅰ:取Ⅱ中少量白色沉淀,充分洗涤,向其中加入稀硫酸,沉淀完全
溶解,产生无色气泡;
操作ⅱ:向操作ⅰ所得溶液中滴入$KSCN$溶液,溶液不变红;
操作ⅲ:向操作ⅱ所得溶液中再滴入少量${H_{2}O_{2}}$溶液,溶液立即变为
红色。
根据以上现象判断实验Ⅱ中生成的白色沉淀的化学式为
。
③研究过程中发现实验Ⅱ中白色沉淀在空气中久置最终也变为红褐
色,写出反应的化学方程式:
。
请用所学的相关知识,回答下列问题:
(1)长期放置的${FeSO_{4}}$溶液易被溶液中溶解的氧气(填“氧化”
或“还原”)而变质。
(2)某实验小组设计实验方案检验${FeSO_{4}}$溶液的变质情况,进行了如下实验:
③若要使变质的${FeSO_{4}}$复原,方法是
(用离子方程式表示)。
(3)设计实验继续探究${FeSO_{4}}$性质。

②对实验Ⅱ所得白色沉淀进行研究(已知${Fe^{2+}}$与${HCO^{-}_{3}}$在溶液中不能
大量共存)。
操作ⅰ:取Ⅱ中少量白色沉淀,充分洗涤,向其中加入稀硫酸,沉淀完全
溶解,产生无色气泡;
操作ⅱ:向操作ⅰ所得溶液中滴入$KSCN$溶液,溶液不变红;
操作ⅲ:向操作ⅱ所得溶液中再滴入少量${H_{2}O_{2}}$溶液,溶液立即变为
红色。
根据以上现象判断实验Ⅱ中生成的白色沉淀的化学式为
。
③研究过程中发现实验Ⅱ中白色沉淀在空气中久置最终也变为红褐
色,写出反应的化学方程式:
。
答案:
(1)氧化
(2)③ 2Fe³⁺ + Fe = 3Fe²⁺
(3)① 先产生白色沉淀,迅速变为灰绿色,最终变为红褐色
② FeCO₃
③ 4FeCO₃ + O₂ + 6H₂O = 4Fe(OH)₃ + 4CO₂
(2)③ 2Fe³⁺ + Fe = 3Fe²⁺
(3)① 先产生白色沉淀,迅速变为灰绿色,最终变为红褐色
② FeCO₃
③ 4FeCO₃ + O₂ + 6H₂O = 4Fe(OH)₃ + 4CO₂
查看更多完整答案,请扫码查看


