2025年168优化重组卷五年高考真题分类汇编高中化学全一册通用版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年168优化重组卷五年高考真题分类汇编高中化学全一册通用版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第92页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
40. (2021·河北卷,14分)当今,世界多国相继规划了碳达峰、碳中和的时间节点,因此,研发二氧化碳利用技术、降低空气中二氧化碳含量成为研究热点。
(1)大气中的二氧化碳主要来自煤、石油及其他含碳化合物的燃烧。已知25℃时,相关物质的燃烧热数据如下表:
则25℃时$H_{2}(g)$和C(石墨,s)生成$C_{6}H_{6}(l)$的热化学方程式为。
(2)雨水中含有来自大气的$CO_{2}$,溶于水中的$CO_{2}$进一步和水反应,发生电离:
①$CO_{2}(g)\rightleftharpoons CO_{2}(aq)$
②$CO_{2}(aq)+H_{2}O(l)\rightleftharpoons H^{+}(aq)+HCO_{3}^{-}(aq)$
25℃时,反应②的平衡常数为$K_{2}$。
溶液中$CO_{2}$的浓度与其在空气中的分压成正比(分压=总压×物质的量分数),比例系数为$y mol· L^{-1}· kPa^{-1}$,当大气压强为p kPa,大气中$CO_{2}(g)$的物质的量分数为x时,溶液中$H^{+}$浓度为$mol· L^{-1}$(写出表达式,考虑水的电离,忽略$HCO_{3}^{-}$的电离)。
(3)105℃时,将足量的某碳酸氢盐($MHCO_{3}$)固体置于真空恒容容器中,存在如下平衡:
$2MHCO_{3}(s)\xlongequal {\triangle }M_{2}CO_{3}(s)+H_{2}O(g)+CO_{2}(g)$
上述反应达平衡时体系的总压为46 kPa。保持温度不变,开始时在体系中先通入一定量的$CO_{2}(g)$,再加入足量$MHCO_{3}(s)$,欲使平衡时体系中水蒸气的分压小于5 kPa,$CO_{2}(g)$的初始压强应大于kPa。
(4)我国科学家研究$Li-CO_{2}$电池,取得了重大科研成果。回答下列问题:
①$Li-CO_{2}$电池中,Li为单质锂片,则该电池中的$CO_{2}$在(填“正”或“负”)极发生电化学反应。研究表明,该电池反应产物为碳酸锂和单质碳,且$CO_{2}$电还原后与锂离子结合形成碳酸锂按以下4个步骤进行,写出步骤Ⅲ的离子方程式。

Ⅰ.$2CO_{2}+2e^{-}=C_{2}O_{4}^{2-}$
Ⅱ.$C_{2}O_{4}^{2-}=CO_{2}+CO_{3}^{2-}$
Ⅲ.
Ⅳ.$CO_{3}^{2-}+2Li^{+}=Li_{2}CO_{3}$
②研究表明,在电解质水溶液中,$CO_{2}$气体可被电化学还原。
Ⅰ.$CO_{2}$在碱性介质中电还原为正丙醇($CH_{3}CH_{2}CH_{2}OH$)的电极反应方程式为。
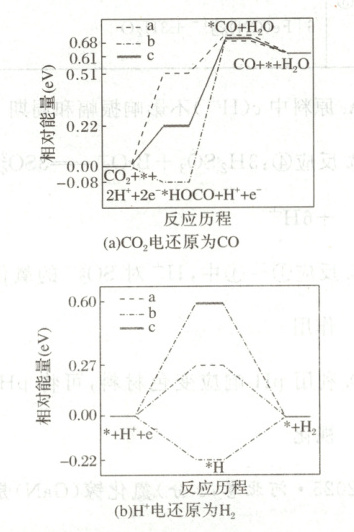
Ⅱ.在电解质水溶液中,三种不同催化剂(a、b、c)上$CO_{2}$电还原为CO的反应进程中($H^{+}$电还原为$H_{2}$的反应可同时发生),相对能量变化如图。由此判断,$CO_{2}$电还原为CO从易到难的顺序为(用a、b、c字母排序)。
(1)大气中的二氧化碳主要来自煤、石油及其他含碳化合物的燃烧。已知25℃时,相关物质的燃烧热数据如下表:
则25℃时$H_{2}(g)$和C(石墨,s)生成$C_{6}H_{6}(l)$的热化学方程式为。
(2)雨水中含有来自大气的$CO_{2}$,溶于水中的$CO_{2}$进一步和水反应,发生电离:
①$CO_{2}(g)\rightleftharpoons CO_{2}(aq)$
②$CO_{2}(aq)+H_{2}O(l)\rightleftharpoons H^{+}(aq)+HCO_{3}^{-}(aq)$
25℃时,反应②的平衡常数为$K_{2}$。
溶液中$CO_{2}$的浓度与其在空气中的分压成正比(分压=总压×物质的量分数),比例系数为$y mol· L^{-1}· kPa^{-1}$,当大气压强为p kPa,大气中$CO_{2}(g)$的物质的量分数为x时,溶液中$H^{+}$浓度为$mol· L^{-1}$(写出表达式,考虑水的电离,忽略$HCO_{3}^{-}$的电离)。
(3)105℃时,将足量的某碳酸氢盐($MHCO_{3}$)固体置于真空恒容容器中,存在如下平衡:
$2MHCO_{3}(s)\xlongequal {\triangle }M_{2}CO_{3}(s)+H_{2}O(g)+CO_{2}(g)$
上述反应达平衡时体系的总压为46 kPa。保持温度不变,开始时在体系中先通入一定量的$CO_{2}(g)$,再加入足量$MHCO_{3}(s)$,欲使平衡时体系中水蒸气的分压小于5 kPa,$CO_{2}(g)$的初始压强应大于kPa。
(4)我国科学家研究$Li-CO_{2}$电池,取得了重大科研成果。回答下列问题:
①$Li-CO_{2}$电池中,Li为单质锂片,则该电池中的$CO_{2}$在(填“正”或“负”)极发生电化学反应。研究表明,该电池反应产物为碳酸锂和单质碳,且$CO_{2}$电还原后与锂离子结合形成碳酸锂按以下4个步骤进行,写出步骤Ⅲ的离子方程式。

Ⅰ.$2CO_{2}+2e^{-}=C_{2}O_{4}^{2-}$
Ⅱ.$C_{2}O_{4}^{2-}=CO_{2}+CO_{3}^{2-}$
Ⅲ.
Ⅳ.$CO_{3}^{2-}+2Li^{+}=Li_{2}CO_{3}$
②研究表明,在电解质水溶液中,$CO_{2}$气体可被电化学还原。
Ⅰ.$CO_{2}$在碱性介质中电还原为正丙醇($CH_{3}CH_{2}CH_{2}OH$)的电极反应方程式为。
Ⅱ.在电解质水溶液中,三种不同催化剂(a、b、c)上$CO_{2}$电还原为CO的反应进程中($H^{+}$电还原为$H_{2}$的反应可同时发生),相对能量变化如图。由此判断,$CO_{2}$电还原为CO从易到难的顺序为(用a、b、c字母排序)。

答案:
(1)$3H_{2}(g)+6C(石墨,s)=C_{6}H_{6}(l)$
(2)$\sqrt {K_{2}ypx}$
(3)100.8
(4)①正$2CO_{3}^{2-}+CO_{2}=2CO_{3}^{2-}+C$②Ⅰ.$3CO_{2}+18e^{-}+13H_{2}O=CH_{3}CH_{2}CH_{2}OH+18OH^{-}$Ⅱ.cab
答案
(1)$3H_{2}(g)+6C(石墨,s)=C_{6}H_{6}(l)$
$\Delta H=+49.1kJ· mol^{-1}$
(2)$\sqrt {K_{2}ypx}$
(3)100.8
(4)①正$2CO_{3}^{2-}+CO_{2}=2CO_{3}^{2-}+C$②Ⅰ.$3CO_{2}+18e^{-}+13H_{2}O=CH_{3}CH_{2}CH_{2}OH+18OH^{-}$Ⅱ.cab
查看更多完整答案,请扫码查看


