2025年168优化重组卷五年高考真题分类汇编高中化学全一册通用版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年168优化重组卷五年高考真题分类汇编高中化学全一册通用版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第64页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
23.(2021·山东卷)利用惰性电极电解制备$Na_2Cr_2O_7$的总反应方程式为:$4Na_2CrO_4+4H_2O\xlongequal{通电}2Na_2Cr_2O_7+4NaOH+2H_2\uparrow+O_2\uparrow$。则$Na_2Cr_2O_7$在
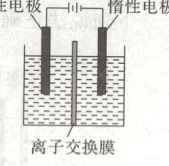
阳
(填“阴”或“阳”)极室制得,电解时通过膜的离子主要为CrO₄²⁻
。
答案:
23.解析 由$4Na₂Cr₂O₄+4H₂O\overset{通电}{=}2Na₂Cr₂O₇+4NaOH+$
2H₂↑+O₂↑可知,电解过程中实质是电解水,阳极上OH⁻失去电子生成H₂O和O₂,阴极上H⁺得到电子生成H₂,由2CrO₄²⁻+H₂O⇌Cr₂O₇²⁻+2OH⁻可知,Cr₂O₇²⁻在c(OH⁻)减小的电极室中制得,即Na₂Cr₂O₇在阳极室产生;电解过程中,阳极室中c(OH⁻)减小,CrO₄²⁻水解平衡正向移动,c(CrO₄²⁻)减小,c(Cr₂O₇²⁻)增大,为提高制备Na₂Cr₂O₇的效率,CrO₄²⁻通过离子交换膜移向阳极。
答案 阳 CrO₄²⁻
2H₂↑+O₂↑可知,电解过程中实质是电解水,阳极上OH⁻失去电子生成H₂O和O₂,阴极上H⁺得到电子生成H₂,由2CrO₄²⁻+H₂O⇌Cr₂O₇²⁻+2OH⁻可知,Cr₂O₇²⁻在c(OH⁻)减小的电极室中制得,即Na₂Cr₂O₇在阳极室产生;电解过程中,阳极室中c(OH⁻)减小,CrO₄²⁻水解平衡正向移动,c(CrO₄²⁻)减小,c(Cr₂O₇²⁻)增大,为提高制备Na₂Cr₂O₇的效率,CrO₄²⁻通过离子交换膜移向阳极。
答案 阳 CrO₄²⁻
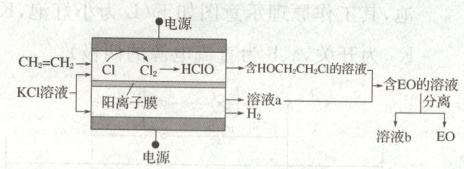
24.(2021·北京卷)环氧乙烷( ,简称EO)是一种重要的工业原料和消毒剂。由乙烯经电解制备EO的原理示意图如下。
,简称EO)是一种重要的工业原料和消毒剂。由乙烯经电解制备EO的原理示意图如下。
(1)①阳极室产生$Cl_2$后发生的反应有:
$CH_2\xlongequal{}CH_2+HClO\xlongequal{}HOCH_2CH_2Cl$。
②结合电极反应式说明生成溶液a的原理
(2)一定条件下,反应物按一定流速通过该装置。电解效率$\eta$和选择性$S$的定义:
$\eta(B)=\frac{n(生成B所用的电子)}{n(通过电极的电子)}×100\%$
$S(B)=\frac{n(生成B所用的乙烯)}{n(转化的乙烯)}×100\%$
①若$\eta(EO)=100\%$,则溶液b的溶质为
②当乙烯完全消耗时,测得$\eta(EO)\approx70\%$,$S(EO)\approx97\%$,推测$\eta(EO)\approx70\%$的原因:
Ⅰ. 阳极有$H_2O$放电
Ⅱ. 阳极有乙烯放电
Ⅲ. 阳极室流出液中含有$Cl_2$和$HClO$
……
i. 检验电解产物,推测Ⅰ不成立。需要检验的物质是
ii. 假设没有生成EO的乙烯全部在阳极放电生成$CO_2$,$\eta(CO_2)\approx$
iii. 实验证实推测Ⅲ成立,所用试剂及现象是
可选试剂:$AgNO_3$溶液、$KI$溶液、淀粉溶液、品红溶液。
 ,简称EO)是一种重要的工业原料和消毒剂。由乙烯经电解制备EO的原理示意图如下。
,简称EO)是一种重要的工业原料和消毒剂。由乙烯经电解制备EO的原理示意图如下。(1)①阳极室产生$Cl_2$后发生的反应有:
$CH_2\xlongequal{}CH_2+HClO\xlongequal{}HOCH_2CH_2Cl$。
②结合电极反应式说明生成溶液a的原理
阴极发生反应:2H₂O+2e⁻=H₂↑+2OH⁻生成OH⁻,K⁺通过阳离子交换膜从阳极迁移到阴极,形成KOH和KCl的混合溶液
。(2)一定条件下,反应物按一定流速通过该装置。电解效率$\eta$和选择性$S$的定义:
$\eta(B)=\frac{n(生成B所用的电子)}{n(通过电极的电子)}×100\%$
$S(B)=\frac{n(生成B所用的乙烯)}{n(转化的乙烯)}×100\%$
①若$\eta(EO)=100\%$,则溶液b的溶质为
KCl
。②当乙烯完全消耗时,测得$\eta(EO)\approx70\%$,$S(EO)\approx97\%$,推测$\eta(EO)\approx70\%$的原因:
Ⅰ. 阳极有$H_2O$放电
Ⅱ. 阳极有乙烯放电
Ⅲ. 阳极室流出液中含有$Cl_2$和$HClO$
……
i. 检验电解产物,推测Ⅰ不成立。需要检验的物质是
O₂
。ii. 假设没有生成EO的乙烯全部在阳极放电生成$CO_2$,$\eta(CO_2)\approx$
13
$\%$。经检验阳极放电产物没有$CO_2$。iii. 实验证实推测Ⅲ成立,所用试剂及现象是
KI溶液和淀粉溶液,溶液变蓝
。可选试剂:$AgNO_3$溶液、$KI$溶液、淀粉溶液、品红溶液。

答案:
24.解析
(1)阳极产生氯气后,可以和水发生反应生成次氯酸方程式为:Cl₂+H₂O=HCl+HClO;溶液a是阴极的产物,在阴极发生反应2H₂O+2e⁻=H₂↑+2OH⁻,同时阳极的钾离子会向阴极移动和氢氧根结合形成氢氧化钾,故答案为:阴极发生反应:2H₂O+2e⁻=H₂↑+2OH⁻生成OH⁻,K⁺通过阳离子交换膜从阳极迁移到阴极,形成KOH和KCl的混合溶液;
(2)①若η(EO)=100%则说明在电解过程中只有乙烯中的碳化合价发生变化,其他元素化合价没有变,故溶液b的溶质为:KCl;②i.阳极有H₂O放电时会产生氧气,故需要检验的物质是O₂;ii.设EO的物质的量为a mol则转化的乙烯的物质的量为:$\frac{a}{97\%};$生成EO转化的电子的物质的量:2a mol;此过程转移电子的总物质的量:$\frac{2a}{70\%};$生成CO₂的物质的量:$2×\frac{a}{97\%}×3%;$生成CO₂转移的电子的物质的量:$2×\frac{a}{97\%}×3%×6,$则$η(CO₂)=\frac{\frac{2a}{97\%}×3\%×6}{2a}×\frac{2a}{70\%}≈13\%;$
iii.实验证实推测Ⅲ成立,则会产生氯气,验证氯气即可,故答案为:KCl溶液和淀粉溶液,溶液变蓝。
答案
(1)Cl₂+H₂O=HCl+HClO ②阴极发生反应:
2H₂O+2e⁻=H₂↑+2OH⁻生成OH⁻,K⁺通过阳离子交换膜从阳极迁移到阴极,形成KOH和KCl的混合溶液
(2)①KCl ②O₂ 13 KI溶液和淀粉溶液,溶液变蓝
(1)阳极产生氯气后,可以和水发生反应生成次氯酸方程式为:Cl₂+H₂O=HCl+HClO;溶液a是阴极的产物,在阴极发生反应2H₂O+2e⁻=H₂↑+2OH⁻,同时阳极的钾离子会向阴极移动和氢氧根结合形成氢氧化钾,故答案为:阴极发生反应:2H₂O+2e⁻=H₂↑+2OH⁻生成OH⁻,K⁺通过阳离子交换膜从阳极迁移到阴极,形成KOH和KCl的混合溶液;
(2)①若η(EO)=100%则说明在电解过程中只有乙烯中的碳化合价发生变化,其他元素化合价没有变,故溶液b的溶质为:KCl;②i.阳极有H₂O放电时会产生氧气,故需要检验的物质是O₂;ii.设EO的物质的量为a mol则转化的乙烯的物质的量为:$\frac{a}{97\%};$生成EO转化的电子的物质的量:2a mol;此过程转移电子的总物质的量:$\frac{2a}{70\%};$生成CO₂的物质的量:$2×\frac{a}{97\%}×3%;$生成CO₂转移的电子的物质的量:$2×\frac{a}{97\%}×3%×6,$则$η(CO₂)=\frac{\frac{2a}{97\%}×3\%×6}{2a}×\frac{2a}{70\%}≈13\%;$
iii.实验证实推测Ⅲ成立,则会产生氯气,验证氯气即可,故答案为:KCl溶液和淀粉溶液,溶液变蓝。
答案
(1)Cl₂+H₂O=HCl+HClO ②阴极发生反应:
2H₂O+2e⁻=H₂↑+2OH⁻生成OH⁻,K⁺通过阳离子交换膜从阳极迁移到阴极,形成KOH和KCl的混合溶液
(2)①KCl ②O₂ 13 KI溶液和淀粉溶液,溶液变蓝
(2022·广东,4分)为检验牺牲阳极的阴极保护法对钢铁防腐的效果,将镀层有破损的镀锌铁片放入酸化的$3\%\ NaCl$溶液中。一段时间后,取溶液分别实验,能说明铁片没有被腐蚀
的是 (
A.加入$AgNO_3$溶液产生沉淀
B.加入淀粉碘化钾溶液无蓝色出现
C.加入$KSCN$溶液无红色出现
D.加入$K_3[Fe(CN_6)]$溶液无蓝色沉淀生成
的是 (
D
)A.加入$AgNO_3$溶液产生沉淀
B.加入淀粉碘化钾溶液无蓝色出现
C.加入$KSCN$溶液无红色出现
D.加入$K_3[Fe(CN_6)]$溶液无蓝色沉淀生成
答案:
D
查看更多完整答案,请扫码查看


