2025年暑假生活北京师范大学出版社高一化学人教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年暑假生活北京师范大学出版社高一化学人教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
一、氮气与氮的固定
1. 氮气的物理性质
$N_{2}$是一种无色、无味的气体,密度比空气的略小,难溶于水。
2. 氮气的结构与化学性质
(1)结构
$N_{2}$的结构式为
(2)化学性质
在
①
②
③
3. 氮的固定
将大气中
(1)自然固氮
大自然通过闪电释放的能量将空气中的氮气转化为含氮的化合物,或者通过豆科植物的根瘤菌等将氮气转化成含氮的化合物。
(2)人工固氮
人类通过控制条件,将氮气氧化或还原为氮的化合物,实现人工固氮。最重要的人工固氮途径就是
1. 氮气的物理性质
$N_{2}$是一种无色、无味的气体,密度比空气的略小,难溶于水。
2. 氮气的结构与化学性质
(1)结构
$N_{2}$的结构式为
$ N \equiv N $
,氮氮三键很难断裂,$N_{2}$的化学性质很稳定。(2)化学性质
在
高温、放电
等条件下,$N_{2}$获得了足够的能量,使氮氮三键断裂。分别写出$N_{2}与Mg$、$H_{2}$、$O_{2}$反应的化学方程式。①
$ N_{2} + 3Mg \xlongequal{点燃} Mg_{3}N_{2} $
;②
$ N_{2} + 3H_{2} \xrightleftharpoons[催化剂]{高温、高压} 2NH_{3} $
;③
$ N_{2} + O_{2} \xlongequal{放电或高温} 2NO $
。3. 氮的固定
将大气中
游离态
的氮转化为氮的化合物
的过程叫做氮的固定。(1)自然固氮
大自然通过闪电释放的能量将空气中的氮气转化为含氮的化合物,或者通过豆科植物的根瘤菌等将氮气转化成含氮的化合物。
(2)人工固氮
人类通过控制条件,将氮气氧化或还原为氮的化合物,实现人工固氮。最重要的人工固氮途径就是
工业合成氨
。
答案:
2.
(1)$ N \equiv N $
(2)高温、放电 ①$ N_{2} + 3Mg \xlongequal{点燃} Mg_{3}N_{2} $ ②$ N_{2} + 3H_{2} \xrightleftharpoons[催化剂]{高温、高压} 2NH_{3} $ ③$ N_{2} + O_{2} \xlongequal{放电或高温} 2NO $ 3. 游离态 氮的化合物
(2)工业合成氨
(1)$ N \equiv N $
(2)高温、放电 ①$ N_{2} + 3Mg \xlongequal{点燃} Mg_{3}N_{2} $ ②$ N_{2} + 3H_{2} \xrightleftharpoons[催化剂]{高温、高压} 2NH_{3} $ ③$ N_{2} + O_{2} \xlongequal{放电或高温} 2NO $ 3. 游离态 氮的化合物
(2)工业合成氨
二、一氧化氮与二氧化氮的对比

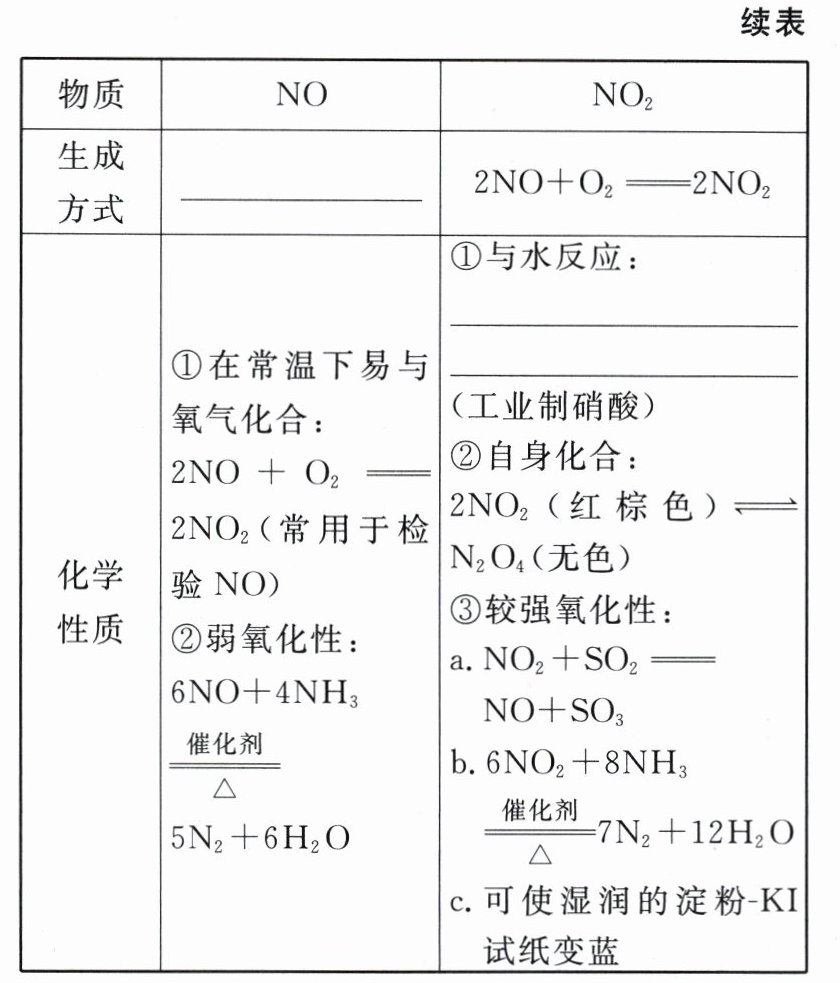


$ N_{2} + O_{2} \xlongequal{放电或高温} 2NO $
$ 3NO_{2} + H_{2}O = 2HNO_{3} + NO $
答案:
$ N_{2} + O_{2} \xlongequal{放电或高温} 2NO $ $ 3NO_{2} + H_{2}O = 2HNO_{3} + NO $
三、氨和铵盐
1. 氨的化学性质
(1)氨与水反应
氨极易溶于水,也易与水反应:
$NH_{3} + H_{2}O\overset{化合}{\underset{分解}{\rightleftharpoons }}NH_{3}\cdot H_{2}O\overset{电离}{\underset{结合}{\rightleftharpoons }}NH_{4}^{+} + OH^{-}$
(2)氨与酸反应
氨与酸反应的实质是$NH_{3}与H^{+}$结合形成$NH_{4}^{+}$。氨几乎能与所有的酸(难溶性酸如$H_{2}SiO_{3}$等除外)反应生成铵盐。
(3)氨的还原性
①催化氧化:
②在纯氧中燃烧:$4NH_{3} + 3O_{2}\xlongequal{点燃}2N_{2} + 6H_{2}O$($O_{2}$置换出$N_{2}$)。
③与$Cl_{2}$反应:$2NH_{3} + 3Cl_{2} = N_{2} + 6HCl或8NH_{3} + 3Cl_{2} = N_{2} + 6NH_{4}Cl$(产生白烟)。
④还原灼热的$CuO$:$2NH_{3} + 3CuO\xlongequal{\triangle}N_{2} + 3Cu + 3H_{2}O$。
⑤还原NO、$NO_{2}$:$4NH_{3} + 6NO\xlongequal[\triangle]{催化剂}5N_{2} + 6H_{2}O$,$8NH_{3} + 6NO_{2}\xlongequal[\triangle]{催化剂}7N_{2} + 12H_{2}O$(治理氮氧化物引起的污染)。
2. 铵盐
表2-2
|组成|$NH_{4}^{+}$和酸根离子|
|物理性质|固体,绝大多数铵盐易溶于水|
|化学性质|(1)铵盐受热易分解,如碳酸氢铵分解:
|$NH_{4}^{+}$的检验|取少量固体样品或溶液加入试管中,再加入$NaOH$溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体(或将蘸有浓盐酸的玻璃棒靠近试管口,有白烟产生),证明固体样品或溶液中含有$NH_{4}^{+}$|
1. 氨的化学性质
(1)氨与水反应
氨极易溶于水,也易与水反应:
$NH_{3} + H_{2}O\overset{化合}{\underset{分解}{\rightleftharpoons }}NH_{3}\cdot H_{2}O\overset{电离}{\underset{结合}{\rightleftharpoons }}NH_{4}^{+} + OH^{-}$
(2)氨与酸反应
氨与酸反应的实质是$NH_{3}与H^{+}$结合形成$NH_{4}^{+}$。氨几乎能与所有的酸(难溶性酸如$H_{2}SiO_{3}$等除外)反应生成铵盐。
(3)氨的还原性
①催化氧化:
$ 4NH_{3} + 5O_{2} \xlongequal[\triangle]{催化剂} 4NO + 6H_{2}O $
(注意:生成NO而不是$NO_{2}$)。②在纯氧中燃烧:$4NH_{3} + 3O_{2}\xlongequal{点燃}2N_{2} + 6H_{2}O$($O_{2}$置换出$N_{2}$)。
③与$Cl_{2}$反应:$2NH_{3} + 3Cl_{2} = N_{2} + 6HCl或8NH_{3} + 3Cl_{2} = N_{2} + 6NH_{4}Cl$(产生白烟)。
④还原灼热的$CuO$:$2NH_{3} + 3CuO\xlongequal{\triangle}N_{2} + 3Cu + 3H_{2}O$。
⑤还原NO、$NO_{2}$:$4NH_{3} + 6NO\xlongequal[\triangle]{催化剂}5N_{2} + 6H_{2}O$,$8NH_{3} + 6NO_{2}\xlongequal[\triangle]{催化剂}7N_{2} + 12H_{2}O$(治理氮氧化物引起的污染)。
2. 铵盐
表2-2
|组成|$NH_{4}^{+}$和酸根离子|
|物理性质|固体,绝大多数铵盐易溶于水|
|化学性质|(1)铵盐受热易分解,如碳酸氢铵分解:
$ NH_{4}HCO_{3} \xlongequal{\triangle} NH_{3} \uparrow + CO_{2} \uparrow + H_{2}O $
;氯化铵分解:$ NH_{4}Cl \xlongequal{\triangle} NH_{3} \uparrow + HCl \uparrow $
(气体遇冷生成白色固体)(2)铵盐与碱反应,如:$(NH_{4})_{2}SO_{4} + 2NaOH\xlongequal{\triangle}Na_{2}SO_{4} + 2NH_{3}\uparrow + 2H_{2}O$(固体共热)||$NH_{4}^{+}$的检验|取少量固体样品或溶液加入试管中,再加入$NaOH$溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体(或将蘸有浓盐酸的玻璃棒靠近试管口,有白烟产生),证明固体样品或溶液中含有$NH_{4}^{+}$|
答案:
1.
(3)①$ 4NH_{3} + 5O_{2} \xlongequal[\triangle]{催化剂} 4NO + 6H_{2}O $ 2.
(1)$ NH_{4}HCO_{3} \xlongequal{\triangle} NH_{3} \uparrow + CO_{2} \uparrow + H_{2}O $ $ NH_{4}Cl \xlongequal{\triangle} NH_{3} \uparrow + HCl \uparrow $
(3)①$ 4NH_{3} + 5O_{2} \xlongequal[\triangle]{催化剂} 4NO + 6H_{2}O $ 2.
(1)$ NH_{4}HCO_{3} \xlongequal{\triangle} NH_{3} \uparrow + CO_{2} \uparrow + H_{2}O $ $ NH_{4}Cl \xlongequal{\triangle} NH_{3} \uparrow + HCl \uparrow $
查看更多完整答案,请扫码查看


