1. 无数实验证明,参加化学反应的各物质的______等于反应后生成的各物质的______,这个规律叫作质量守恒定律。
答案:
质量总和 质量总和
2. 质量守恒的原因(微观解释):在化学变化中,组成物质的元素的种类______,各元素的原子的种类______,原子的数目______,原子的质量也______。
答案:
不变 不变 不变 不变
3.(2025·北京朝阳区期末)下列关于Fe在$O_2$中燃烧的反应叙述不正确的是( )。
A.放出热量
B.生成黑色固体$Fe_3O_4$
C.反应前后固体质量相等
D.参加反应的Fe与生成物中铁元素质量相等
A.放出热量
B.生成黑色固体$Fe_3O_4$
C.反应前后固体质量相等
D.参加反应的Fe与生成物中铁元素质量相等
答案:
C
4. 铜在空气中锈蚀会生成铜绿$[Cu_2(OH)_2CO_3],$铜绿加热分解后不可能生成的物质是( )。
A.CuO
B.H_2O$$
C.CO_2$$
$D.NO_2$
A.CuO
B.H_2O$$
C.CO_2$$
$D.NO_2$
答案:
D [解析]铜绿由铜、氧、氢、碳四种元素组成,化学反应前后元素的种类不变,则铜绿加热后可能生成CuO、H₂O、CO₂,铜绿中不含氮元素,不可能生成NO₂。故选D。
5. 4.6g某物质在氧气中完全燃烧生成8.8g二氧化碳和5.4g水,则关于这种物质的说法正确的是( )。
A.该物质只含有碳元素和氢元素
B.该物质中碳元素与氢元素的质量比为12:1
C.该物质一定含有碳元素和氢元素,可能含有氧元素
D.该物质中C、H、O元素的原子个数比为2:6:1
A.该物质只含有碳元素和氢元素
B.该物质中碳元素与氢元素的质量比为12:1
C.该物质一定含有碳元素和氢元素,可能含有氧元素
D.该物质中C、H、O元素的原子个数比为2:6:1
答案:
D [解析]根据质量守恒定律,化学反应前后元素的种类和质量不变。氧气中含有氧元素,二氧化碳和水中含有碳、氢、氧元素,所以该物质中一定含有碳、氢元素。8.8 g CO₂中碳元素的质量=8.8 g×$\frac{12}{44}$×100%=2.4 g;5.4 g H₂O中氢元素质量=5.4 g×$\frac{2}{18}$×100%=0.6 g;该物质中碳元素与氢元素的质量比为2.4 g:0.6 g=4:1,B错误;因为碳、氢元素的质量和为2.4 g+0.6 g=3 g,小于4.6 g,所以该物质中一定还含有氧元素,氧元素的质量=4.6 g-3 g=1.6 g,A、C错误;该物质中碳、氢、氧元素的原子个数比为$\frac{2.4\mathrm{g}}{12}$:$\frac{0.6\mathrm{g}}{1}$:$\frac{1.6\mathrm{g}}{16}$=2:6:1,D正确。
6. 提分优练 质量守恒定律的发现对化学的发展做出了重要贡献。
(1)质量守恒定律是自然界最基本的规律之一。下列实验装置(天平省略)能用来验证质量守恒定律的是______(填字母)。
 (2)A中用红热的玻璃管引燃白磷,实验现象是白磷燃烧,产生______,放出大量热;实验中气球的作用除了使装置密闭之外,还有______作用;实验时若白磷的量不足,对实验的结果______(填“有”或“没有”)影响。
(2)A中用红热的玻璃管引燃白磷,实验现象是白磷燃烧,产生______,放出大量热;实验中气球的作用除了使装置密闭之外,还有______作用;实验时若白磷的量不足,对实验的结果______(填“有”或“没有”)影响。
(3)在空气中点燃红磷的实验过程中,固体的质量变化如图所示。
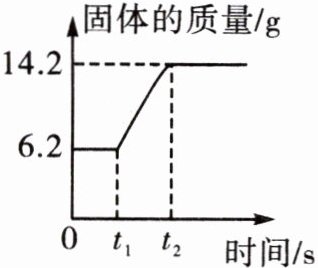
①从图像分析,固体质量在$t_1~t_2s$时间段质量发生变化的原因是______。
②该反应的文字或符号表达式为______。
③参加反应的氧气质量为______。
(1)质量守恒定律是自然界最基本的规律之一。下列实验装置(天平省略)能用来验证质量守恒定律的是______(填字母)。
 (2)A中用红热的玻璃管引燃白磷,实验现象是白磷燃烧,产生______,放出大量热;实验中气球的作用除了使装置密闭之外,还有______作用;实验时若白磷的量不足,对实验的结果______(填“有”或“没有”)影响。
(2)A中用红热的玻璃管引燃白磷,实验现象是白磷燃烧,产生______,放出大量热;实验中气球的作用除了使装置密闭之外,还有______作用;实验时若白磷的量不足,对实验的结果______(填“有”或“没有”)影响。(3)在空气中点燃红磷的实验过程中,固体的质量变化如图所示。

①从图像分析,固体质量在$t_1~t_2s$时间段质量发生变化的原因是______。
②该反应的文字或符号表达式为______。
③参加反应的氧气质量为______。
答案:
(1)A
(2)大量的白烟 平衡装置内外压强 没有
(3)①红磷燃烧生成五氧化二磷,固体中增加了氧元素的质量 ②磷+氧气$\xrightarrow{点燃}$五氧化二磷(或P+O₂$\xrightarrow{点燃}$P₂O₅) ③8 g
[解析]
(1)白磷在空气中燃烧,气球能使装置密闭,反应前后装置总质量不变,能用来验证质量守恒定律,A正确;红墨水注入水中并在水中扩散,没有新物质生成,属于物理变化,不能用来验证质量守恒定律,B错误;镁条在空气中燃烧,有氧气参与反应,并且生成的白烟会逸散到空气中,反应前后固体质量不相等,不能用来验证质量守恒定律,C错误;过氧化氢溶液在二氧化锰的催化作用下分解生成水和氧气,实验在敞口容器中进行,生成的氧气会逸散到空气中,不能用来验证质量守恒定律,D错误;
(2)A中用红热的玻璃管引燃白磷,实验现象是白磷燃烧,产生大量的白烟,放出大量热;实验中气球的作用除了使装置密闭之外,还有平衡装置内外压强的作用;因为该实验是验证质量守恒定律,所以实验时若白磷的量不足,对实验的结果没有影响;
(3)①该反应是红磷在空气中燃烧,t₁~t₂时间段固体质量发生变化的原因是红磷燃烧生成五氧化二磷,固体中增加了氧元素的质量;②该反应是红磷和氧气在点燃的条件下反应生成五氧化二磷;③根据质量守恒定律,反应前后物质的总质量相等,所以参加反应的氧气的质量为14.2 g-6.2 g=8 g。
(1)A
(2)大量的白烟 平衡装置内外压强 没有
(3)①红磷燃烧生成五氧化二磷,固体中增加了氧元素的质量 ②磷+氧气$\xrightarrow{点燃}$五氧化二磷(或P+O₂$\xrightarrow{点燃}$P₂O₅) ③8 g
[解析]
(1)白磷在空气中燃烧,气球能使装置密闭,反应前后装置总质量不变,能用来验证质量守恒定律,A正确;红墨水注入水中并在水中扩散,没有新物质生成,属于物理变化,不能用来验证质量守恒定律,B错误;镁条在空气中燃烧,有氧气参与反应,并且生成的白烟会逸散到空气中,反应前后固体质量不相等,不能用来验证质量守恒定律,C错误;过氧化氢溶液在二氧化锰的催化作用下分解生成水和氧气,实验在敞口容器中进行,生成的氧气会逸散到空气中,不能用来验证质量守恒定律,D错误;
(2)A中用红热的玻璃管引燃白磷,实验现象是白磷燃烧,产生大量的白烟,放出大量热;实验中气球的作用除了使装置密闭之外,还有平衡装置内外压强的作用;因为该实验是验证质量守恒定律,所以实验时若白磷的量不足,对实验的结果没有影响;
(3)①该反应是红磷在空气中燃烧,t₁~t₂时间段固体质量发生变化的原因是红磷燃烧生成五氧化二磷,固体中增加了氧元素的质量;②该反应是红磷和氧气在点燃的条件下反应生成五氧化二磷;③根据质量守恒定律,反应前后物质的总质量相等,所以参加反应的氧气的质量为14.2 g-6.2 g=8 g。
查看更多完整答案,请扫码查看


