1. 原子是由居于原子中心的______和核外______构成的。其中______带正电荷,______带负电荷,正电荷的总电量______(填“大于”“小于”或“等于”)负电荷的总电量,因此整个原子______(填“显”或“不显”)电性。原子核一般是由______和______两种微观粒子构成的,其中______不带电,每个质子带一个单位的______电荷。
答案:
原子核 电子 原子核 核外电子 等于 不显 质子 中子 中子 正
2. 原子核的半径大约是原子半径的______。原子核在原子中所占的体积极小,核外电子在核外空间作______运动。原子的质量几乎集中在______上,原子核里面一般既有带______电的______,又有不带电的______。
答案:
十万分之一 高速 原子核 正 质子 中子
3. 相对原子质量是以一种碳原子质量的______作为基准,其他原子的质量跟它相比较所得的比值。碳的相对原子质量为______,而某物质的相对分子质量等于______,如二氧化碳的相对分子质量为______。
答案:
$\frac{1}{12}$ 12 构成分子的各原子的相对原子质量的总和 44
4. 在化学反应中,原子得到电子,带______电,形成______离子;原子失去电子,带______电,形成______离子。金属钠在氯气中燃烧时,每个钠______失去一个______形成带正电荷的钠______,每个氯______得到一个______形成带负电荷的氯______,带有相反电荷的两种微观粒子之间相互作用,构成了氯化钠。
答案:
负 阴 正 阳 原子 电子 离子 原子 电子 离子
5. 探月卫星“嫦娥一号”主要任务之一是探测月球上氦-3的储量。如图是氦-3原子结构示意图,以下说法错误的是( )。

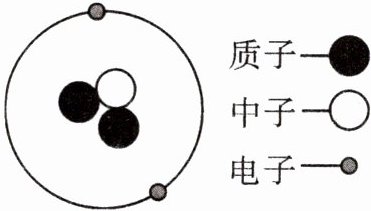
A.原子核内质子数等于核外电子数
B.氦-3原子由原子核和核外电子构成
C.氦-3原子核内质子数等于中子数
D.一个氦-3原子的原子核内有2个质子


A.原子核内质子数等于核外电子数
B.氦-3原子由原子核和核外电子构成
C.氦-3原子核内质子数等于中子数
D.一个氦-3原子的原子核内有2个质子
答案:
C [解析] 如图所示,原子核内质子数等于核外电子数,都是两个,A正确;原子都由原子核和核外电子构成,B正确;氦-3原子核内质子数是2,中子数是1,不相等,C错误;一个氦-3原子的原子核内有2个质子,D正确。
6. 镓原子的质子数为31,相对原子质量为70。则镓原子的核外电子数为( )。
A.31
B.39
C.70
D.101
A.31
B.39
C.70
D.101
答案:
A [解析] 在原子中核电荷数=质子数=核外电子数,由题意镓原子的质子数为31,则镓原子的核外电子数为31,故选A。
7. 如图是四种微观粒子的结构示意图。下列有关说法不正确的是( )。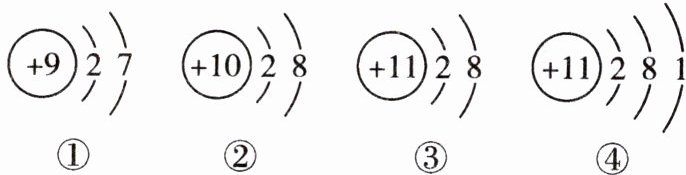
① ② ③ ④
A.④表示的微观粒子在化学变化中容易失电子
B.②③表示的微观粒子化学性质较稳定
C.①②④属于原子,③属于阴离子
D.①表示的微观粒子在化学反应中容易得电子

① ② ③ ④
A.④表示的微观粒子在化学变化中容易失电子
B.②③表示的微观粒子化学性质较稳定
C.①②④属于原子,③属于阴离子
D.①表示的微观粒子在化学反应中容易得电子
答案:
C [解析] ④表示的微观粒子最外层电子数为1,易失去电子,A正确;②③表示的微观粒子最外层电子数为8,化学性质比较稳定,B正确;①②④表示的微观粒子中,质子数=核外电子数,属于原子,③表示的微观粒子中,质子数>核外电子数,表示的是带正电荷的阳离子,C错误;①表示的微观粒子最外层电子数为7,易得电子,D正确。
8. 提分优练 列式并计算下列式子的相对分子质量:
$(1)CO_2$:______。
$(2)KMnO_4$:______。
$(3)Ca(OH)_2$:______。
$(4)CaCO_3$:______。
$(5)Cu(OH)_2$:______。
$(6)H_2SO_4$:______。
$(7)SO_3$:______。
$(1)CO_2$:______。
$(2)KMnO_4$:______。
$(3)Ca(OH)_2$:______。
$(4)CaCO_3$:______。
$(5)Cu(OH)_2$:______。
$(6)H_2SO_4$:______。
$(7)SO_3$:______。
答案:
(1)44
(2)158
(3)74
(4)100
(5)98
(6)98
(7)80
(1)44
(2)158
(3)74
(4)100
(5)98
(6)98
(7)80
查看更多完整答案,请扫码查看


