第9页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
10.(襄阳中考)小明同学取镁、铝、锌三种金属,分别放入盛有质量和质量分数都相等的稀盐酸的锥形瓶中,实验装置如图1所示,采集数据,得到如图2所示的气压变化曲线。
图2金属与稀盐酸反应时气压的变化曲线
(1)镁、铝、锌与稀盐酸反应产生的相同气体是H₂(填化学式)。
(2)铝对应的曲线是B,反应速率先慢后快,其主要原因是铝表面有一层致密的氧化铝薄膜,盐酸先与氧化铝反应,氧化铝反应完后,铝再与盐酸反应。
(3)从图2分析,以下结论正确的是____(填序号)。
①金属镁对应的气压变化曲线是A
②M点时参加反应的镁锌质量相等
③实验时取用的镁铝质量可能相等
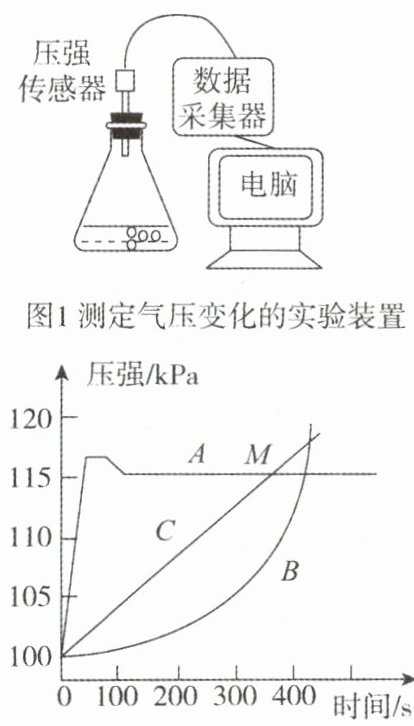
图2金属与稀盐酸反应时气压的变化曲线
(1)镁、铝、锌与稀盐酸反应产生的相同气体是H₂(填化学式)。
(2)铝对应的曲线是B,反应速率先慢后快,其主要原因是铝表面有一层致密的氧化铝薄膜,盐酸先与氧化铝反应,氧化铝反应完后,铝再与盐酸反应。
(3)从图2分析,以下结论正确的是____(填序号)。
①金属镁对应的气压变化曲线是A
②M点时参加反应的镁锌质量相等
③实验时取用的镁铝质量可能相等

答案:
(1)$H_{2}$
(2)铝的表面有一层致密的氧化铝薄膜,氧化铝先与稀盐酸反应生成氯化铝和水,氧化铝反应完,铝再与稀盐酸反应生成氯化铝和氢气
(3)①③
(1)$H_{2}$
(2)铝的表面有一层致密的氧化铝薄膜,氧化铝先与稀盐酸反应生成氯化铝和水,氧化铝反应完,铝再与稀盐酸反应生成氯化铝和氢气
(3)①③
11. 在加热的条件下浓硫酸与铜反应,反应的化学方程式为Cu+2H₂SO₄(浓) = CuSO₄+SO₂↑+2H₂O(请填上化学式使之成为完整的化学方程式),足量的铜和20克98%浓硫酸充分反应。
(1)理论上可以得到多少克硫酸铜?
(2)实际得到的溶液中硫酸铜没有这么多,原因是随着反应的进行,浓硫酸会变稀,而稀硫酸与铜不反应。
(1)理论上可以得到多少克硫酸铜?
(2)实际得到的溶液中硫酸铜没有这么多,原因是随着反应的进行,浓硫酸会变稀,而稀硫酸与铜不反应。
答案:
$H_{2}O$
(1)解:设理论上可以得到硫酸铜的质量为$x$。
$Cu + 2H_{2}SO_{4}(浓)\stackrel{\triangle}{=\!=\!=}CuSO_{4} + SO_{2}\uparrow + 2H_{2}O$
196 160
$20g×98\%$ $x$
$\frac{196}{20g×98\%}=\frac{160}{x}$ 解得:$x = 16g$
答:理论上可以得到16g硫酸铜。
(2)浓硫酸反应一段时间后变成稀硫酸,铜不能跟稀硫酸反应
(1)解:设理论上可以得到硫酸铜的质量为$x$。
$Cu + 2H_{2}SO_{4}(浓)\stackrel{\triangle}{=\!=\!=}CuSO_{4} + SO_{2}\uparrow + 2H_{2}O$
196 160
$20g×98\%$ $x$
$\frac{196}{20g×98\%}=\frac{160}{x}$ 解得:$x = 16g$
答:理论上可以得到16g硫酸铜。
(2)浓硫酸反应一段时间后变成稀硫酸,铜不能跟稀硫酸反应
查看更多完整答案,请扫码查看


