第58页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
9. 下列变化不能通过加稀盐酸反应实现的是 ( )
A. Al→AlCl₃
B. Zn→ZnCl₂
C. CaCO₃→CaCl₂
D. Fe→FeCl₃
A. Al→AlCl₃
B. Zn→ZnCl₂
C. CaCO₃→CaCl₂
D. Fe→FeCl₃
答案:
D
10. 下列除杂所选用的试剂,正确的是( )
A. 用稀盐酸除去铜粉中的铁粉
B. 用稀盐酸除去CaO中的CaCO₃
C. 用浓硫酸除去O₂中的CO₂
D. 用稀硫酸除去铁粉中的氧化铁
A. 用稀盐酸除去铜粉中的铁粉
B. 用稀盐酸除去CaO中的CaCO₃
C. 用浓硫酸除去O₂中的CO₂
D. 用稀硫酸除去铁粉中的氧化铁
答案:
A
11. 硫酸是工农业生产中使用非常广泛的一种试剂,实验室用质量分数为98%的浓硫酸(密度为1.84 g/cm³)配制49 g质量分数为20%的硫酸。
(1)经计算,所需水的质量为______g,所需98%的浓硫酸的体积为______mL(结果精确到0.1 mL)。
(2)量取上述体积的浓硫酸所选用的仪器为______(填字母)。
A. 10 mL量筒 B. 100 mL烧杯
C. 100 mL量筒 D. 胶头滴管
(3)稀释浓硫酸时,将浓硫酸沿烧杯壁缓慢注入盛有水的烧杯里,并用______不断搅拌。
(4)如果不慎将浓硫酸沾到皮肤上,应立即用大量______冲洗,然后涂上3%的小苏打溶液。
(1)经计算,所需水的质量为______g,所需98%的浓硫酸的体积为______mL(结果精确到0.1 mL)。
(2)量取上述体积的浓硫酸所选用的仪器为______(填字母)。
A. 10 mL量筒 B. 100 mL烧杯
C. 100 mL量筒 D. 胶头滴管
(3)稀释浓硫酸时,将浓硫酸沿烧杯壁缓慢注入盛有水的烧杯里,并用______不断搅拌。
(4)如果不慎将浓硫酸沾到皮肤上,应立即用大量______冲洗,然后涂上3%的小苏打溶液。
答案:
(1)39 5.4
(2)AD
(3)玻璃棒
(4)水
(1)39 5.4
(2)AD
(3)玻璃棒
(4)水
12. 盐酸是氯化氢气体(HCl)的水溶液,有挥发性,回答问题:
(1)打开盛浓盐酸的试剂瓶的瓶塞,闻到刺激性气味,体现分子具有的性质是______。
(2)加热条件下,浓盐酸与二氧化锰发生反应:MnO₂+4HCl $\triangle$ MnCl₂+X↑+2H₂O,X是一种气体单质,则X的化学式是______。
(3)实验室制取H₂的反应原理:Zn+H₂SO₄ = ZnSO₄+H₂↑,若用稀盐酸代替稀硫酸,制得的H₂中会混入的气体杂质是______。
(1)打开盛浓盐酸的试剂瓶的瓶塞,闻到刺激性气味,体现分子具有的性质是______。
(2)加热条件下,浓盐酸与二氧化锰发生反应:MnO₂+4HCl $\triangle$ MnCl₂+X↑+2H₂O,X是一种气体单质,则X的化学式是______。
(3)实验室制取H₂的反应原理:Zn+H₂SO₄ = ZnSO₄+H₂↑,若用稀盐酸代替稀硫酸,制得的H₂中会混入的气体杂质是______。
答案:
(1)运动(或不断运动)
(2)$Cl_{2}$
(3)$HCl$(或氯化氢)
(1)运动(或不断运动)
(2)$Cl_{2}$
(3)$HCl$(或氯化氢)
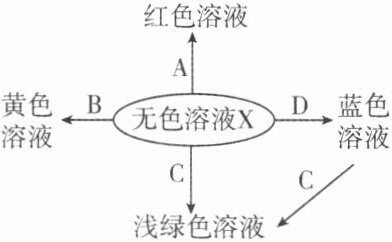
13. 如图化学反应的溶液颜色变化体现了“魔法世界,魅力化学”,请回答:
(1)溶液X是______(填“酸”或“碱”),试剂A的名称是______。
(2)若X是稀硫酸,B是氧化物,则B的化学式为______。
(3)若X是稀盐酸,C是单质,则C的名称是______。
(4)若X是稀硫酸,D是氧化物,则X与D反应的化学方程式为______。
(1)溶液X是______(填“酸”或“碱”),试剂A的名称是______。
(2)若X是稀硫酸,B是氧化物,则B的化学式为______。
(3)若X是稀盐酸,C是单质,则C的名称是______。
(4)若X是稀硫酸,D是氧化物,则X与D反应的化学方程式为______。

答案:
(1)酸 石蕊溶液
(2)$Fe_{2}O_{3}$
(3)铁
(4)$CuO+H_{2}SO_{4}=CuSO_{4}+H_{2}O$
(1)酸 石蕊溶液
(2)$Fe_{2}O_{3}$
(3)铁
(4)$CuO+H_{2}SO_{4}=CuSO_{4}+H_{2}O$
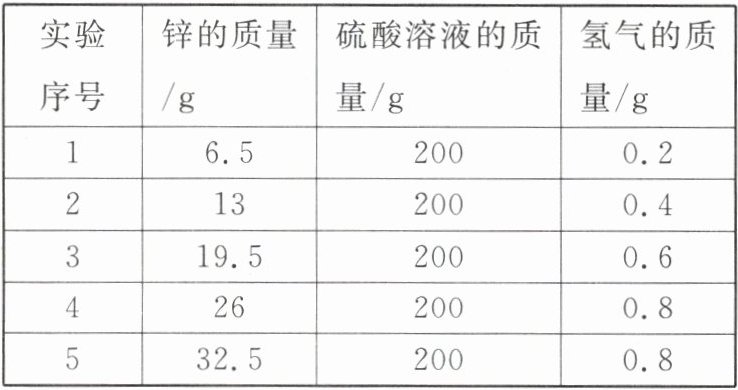
14. 用锌和硫酸反应,5次实验结果如下表所示,根据图表回答下列问题:
(1)第______次实验数据表明锌和硫酸完全反应。
(2)计算硫酸溶液的溶质质量分数。
(1)第______次实验数据表明锌和硫酸完全反应。
(2)计算硫酸溶液的溶质质量分数。

答案:
(1)4
(2)19.6%
(1)4
(2)19.6%
查看更多完整答案,请扫码查看


