第45页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
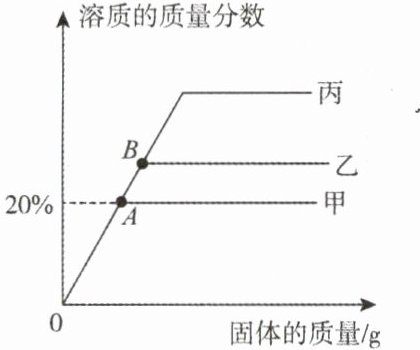
14.(郴州中考)T℃时,等质量的甲、乙、丙三种固体分别加入等质量的水中,加入固体的质量与溶液溶质质量分数的关系如图所示,请回答下列问题:
(1)该温度下,甲、乙、丙三种固体溶解度由大到小的顺序是甲>乙>丙。
(2)乙溶液在B点属于不饱和(填“饱和”或“不饱和”)。
(3)将甲的不饱和溶液变为饱和溶液,可用方法是增加溶质、蒸发溶剂、降低温度。
(4)该温度下,甲的溶解度为50g。
(5)已知乙的溶解度受温度影响较小,丙的溶解度受温度影响较大,当丙中混有少量乙,提纯方法是降温结晶。
(1)该温度下,甲、乙、丙三种固体溶解度由大到小的顺序是甲>乙>丙。
(2)乙溶液在B点属于不饱和(填“饱和”或“不饱和”)。
(3)将甲的不饱和溶液变为饱和溶液,可用方法是增加溶质、蒸发溶剂、降低温度。
(4)该温度下,甲的溶解度为50g。
(5)已知乙的溶解度受温度影响较小,丙的溶解度受温度影响较大,当丙中混有少量乙,提纯方法是降温结晶。

答案:
(1)丙>乙>甲
(2)饱和
(3)加入甲物质或蒸发溶剂
(4)25 g
(5)降温结晶
(1)丙>乙>甲
(2)饱和
(3)加入甲物质或蒸发溶剂
(4)25 g
(5)降温结晶
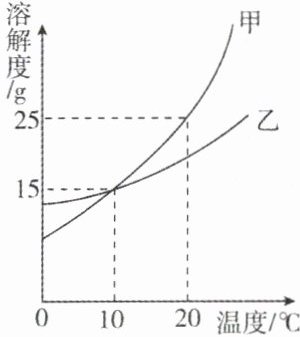
15.如图是甲、乙两种固体物质的溶解度曲线图,请回答下列问题:
(1)20℃时,将15g的甲物质充分溶解在50g水中,所形成溶液的溶质质量分数是 。
(2)10℃时,欲将150g乙物质的饱和溶液质量分数减小一半,需要加水 。
(3)某同学欲将20℃时300g20%的甲溶液溶质质量分数增大一倍。他采用恒温蒸发水的方法,并进行了如下计算:
解:设蒸发水的质量为x。
300g×20%=(300g−x)×40%
解得:x=150g
试分析:他能否达到目的,并说明理由。
(1)20℃时,将15g的甲物质充分溶解在50g水中,所形成溶液的溶质质量分数是 。
(2)10℃时,欲将150g乙物质的饱和溶液质量分数减小一半,需要加水 。
(3)某同学欲将20℃时300g20%的甲溶液溶质质量分数增大一倍。他采用恒温蒸发水的方法,并进行了如下计算:
解:设蒸发水的质量为x。
300g×20%=(300g−x)×40%
解得:x=150g
试分析:他能否达到目的,并说明理由。

答案:
(1)20%
(2)150
(3)他不能达到目的;因为20℃时20%的甲溶液为该温度下的饱和溶液,恒温蒸发水的过程中,温度不变,溶解度不变,其饱和溶液中的溶质质量分数不变。
(1)20%
(2)150
(3)他不能达到目的;因为20℃时20%的甲溶液为该温度下的饱和溶液,恒温蒸发水的过程中,温度不变,溶解度不变,其饱和溶液中的溶质质量分数不变。
16.(福建中考)请参加“氯化钠欢乐之旅”的实践活动。
任务一 参观盐场
(1)利用风吹和日晒使海水不断蒸发至有晶体析出,此过程溶液中NaCl的质量分数逐渐增大(填“增大”或“减小”)。
任务二 提纯粗盐
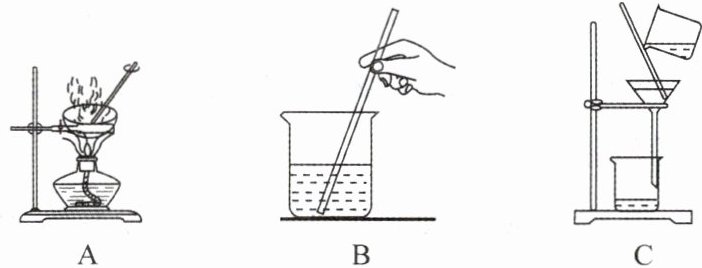
(2)粗盐提纯的有关操作如图所示。
①正确的操作顺序是________(填标号)。
②操作A中,当加热到蒸发皿中出现较多固体时,停止加热。
③操作C中,玻璃棒的作用是搅拌,防止局部过热,造成液滴飞溅。
任务三 应用食盐
(3)农业上常用质量分数为16%的NaCl 溶液选种。若在实验室中配制该溶液,需要的玻璃仪器有烧杯、玻璃棒、胶头滴管和量筒。
(4)NaCl是一种重要的化工原料。从元素守恒的视角,以NaCl为基本原料,可能制取的物质有氢氧化钠(写一种)。
任务一 参观盐场
(1)利用风吹和日晒使海水不断蒸发至有晶体析出,此过程溶液中NaCl的质量分数逐渐增大(填“增大”或“减小”)。
任务二 提纯粗盐
(2)粗盐提纯的有关操作如图所示。
①正确的操作顺序是________(填标号)。
②操作A中,当加热到蒸发皿中出现较多固体时,停止加热。
③操作C中,玻璃棒的作用是搅拌,防止局部过热,造成液滴飞溅。
任务三 应用食盐
(3)农业上常用质量分数为16%的NaCl 溶液选种。若在实验室中配制该溶液,需要的玻璃仪器有烧杯、玻璃棒、胶头滴管和量筒。
(4)NaCl是一种重要的化工原料。从元素守恒的视角,以NaCl为基本原料,可能制取的物质有氢氧化钠(写一种)。

答案:
(1)增大
(2)①BCA ②较多固体 ③引流
(3)量筒
(4)NaOH(或其他合理答案)
(1)增大
(2)①BCA ②较多固体 ③引流
(3)量筒
(4)NaOH(或其他合理答案)
查看更多完整答案,请扫码查看


