第13页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
12. 金属用途广泛,其结构和性质等是化学的重要研究内容。
(1) 如图是铝的原子结构示意图。下列说法不正确的是______(填序号)。

A. 铝原子的质子数为13
B. 在化合物中铝通常显 +3价
C. 铝是地壳中含量最多的元素
D. 铝可作导线是由于它具有良好的导电性
(2) 某化学小组用一定量的AgNO₃和Cu(NO₃)₂混合溶液进行了下图实验,并对溶液A和固体B的成分进行了分析和研究。
【提出问题】溶液A中的溶质可能有哪些?
【作出猜想】①只有Zn(NO₃)₂
②Zn(NO₃)₂、AgNO₃
③Zn(NO₃)₂、Cu(NO₃)₂
④Zn(NO₃)₂、Cu(NO₃)₂、AgNO₃
【交流讨论】不合理的猜想是______(填标号),其理由是______________________。
【实验探究】若猜想①成立,通过以下实验可确定固体B的成分,请将下面内容填写完整:
实验步骤:取少量固体B,滴加__________。
实验现象:有气泡产生。
实验解释:有关反应的化学方程式:______________________。
(1) 如图是铝的原子结构示意图。下列说法不正确的是______(填序号)。

A. 铝原子的质子数为13
B. 在化合物中铝通常显 +3价
C. 铝是地壳中含量最多的元素
D. 铝可作导线是由于它具有良好的导电性
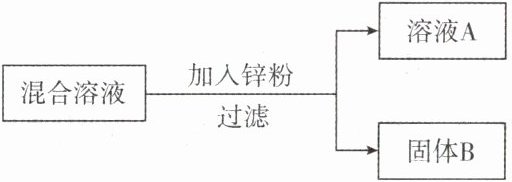
(2) 某化学小组用一定量的AgNO₃和Cu(NO₃)₂混合溶液进行了下图实验,并对溶液A和固体B的成分进行了分析和研究。
【提出问题】溶液A中的溶质可能有哪些?
【作出猜想】①只有Zn(NO₃)₂
②Zn(NO₃)₂、AgNO₃
③Zn(NO₃)₂、Cu(NO₃)₂
④Zn(NO₃)₂、Cu(NO₃)₂、AgNO₃
【交流讨论】不合理的猜想是______(填标号),其理由是______________________。
【实验探究】若猜想①成立,通过以下实验可确定固体B的成分,请将下面内容填写完整:
实验步骤:取少量固体B,滴加__________。
实验现象:有气泡产生。
实验解释:有关反应的化学方程式:______________________。

答案:
C
@@[交流讨论]② 猜想②中无硝酸铜,说明$Cu(NO_{3})_{2}$已与锌完全反应生成Cu,而铜能与硝酸银反应,所以不可能存在硝酸银[实验探究]稀盐酸 $Zn + 2HCl = ZnCl_{2} + H_{2}\uparrow$
@@[交流讨论]② 猜想②中无硝酸铜,说明$Cu(NO_{3})_{2}$已与锌完全反应生成Cu,而铜能与硝酸银反应,所以不可能存在硝酸银[实验探究]稀盐酸 $Zn + 2HCl = ZnCl_{2} + H_{2}\uparrow$
13. (陕西中考)白铜是铜、镍(Ni)合金,某学习小组同学欲利用废弃的白铜回收铜、镍两种金属。
(1) 先向盛有等量镍粉和锌粉的两支试管中分别加入溶质质量分数相同的稀硫酸,观察到都有气泡产生,且锌粉与稀硫酸反应更剧烈。镍粉与稀硫酸反应后的溶液为绿色,说明镍的金属活动性比锌______(填“强”或“弱”)。查阅资料可知,镍与稀硫酸反应的化学方程式为:Ni + H₂SO₄ = NiSO₄ + H₂↑。
(2) 接下来,同学们设计了如下实验流程回收铜和镍。
上图中,固体A是______________________,②中反应的化学方程式是______________________(只写一个)。
(3) 要验证Ni、Zn、Cu的金属活动性顺序,用下列各组药品进行实验,不能达到目的的是______(填字母)。
A. Ni、Zn、Cu、稀盐酸
B. Ni、Cu、ZnSO₄溶液
C. Zn、Cu、NiSO₄溶液
D. Ni、ZnSO₄溶液、CuSO₄溶液

(1) 先向盛有等量镍粉和锌粉的两支试管中分别加入溶质质量分数相同的稀硫酸,观察到都有气泡产生,且锌粉与稀硫酸反应更剧烈。镍粉与稀硫酸反应后的溶液为绿色,说明镍的金属活动性比锌______(填“强”或“弱”)。查阅资料可知,镍与稀硫酸反应的化学方程式为:Ni + H₂SO₄ = NiSO₄ + H₂↑。
(2) 接下来,同学们设计了如下实验流程回收铜和镍。
上图中,固体A是______________________,②中反应的化学方程式是______________________(只写一个)。
(3) 要验证Ni、Zn、Cu的金属活动性顺序,用下列各组药品进行实验,不能达到目的的是______(填字母)。
A. Ni、Zn、Cu、稀盐酸
B. Ni、Cu、ZnSO₄溶液
C. Zn、Cu、NiSO₄溶液
D. Ni、ZnSO₄溶液、CuSO₄溶液

答案:
(1)弱
(2)铜(或Cu)
$Zn + NiSO_{4} = ZnSO_{4} + Ni$或$Zn + H_{2}SO_{4} = ZnSO_{4} + H_{2}\uparrow$
(3)B
(2)铜(或Cu)
$Zn + NiSO_{4} = ZnSO_{4} + Ni$或$Zn + H_{2}SO_{4} = ZnSO_{4} + H_{2}\uparrow$
(3)B
查看更多完整答案,请扫码查看


