2025年点金训练精讲巧练高中化学必修第二册人教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年点金训练精讲巧练高中化学必修第二册人教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第39页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
1. 一定温度下,向1L密闭容器中加入1mol A气体和3mol B气体,发生反应:$A(g)+3B(g)\rightleftharpoons2C(g)$,测得5min内反应物A的物质的量由1mol降低到0.5mol,则反应速率$v(A)$为(
A.$0.1mol\cdot L^{-1}\cdot min^{-1}$
B.$0.2mol\cdot L^{-1}\cdot min^{-1}$
C.$0.3mol\cdot L^{-1}\cdot min^{-1}$
D.$0.5mol\cdot L^{-1}\cdot min^{-1}$
A
)A.$0.1mol\cdot L^{-1}\cdot min^{-1}$
B.$0.2mol\cdot L^{-1}\cdot min^{-1}$
C.$0.3mol\cdot L^{-1}\cdot min^{-1}$
D.$0.5mol\cdot L^{-1}\cdot min^{-1}$
答案:
1.A 解析:向1L密闭容器中加入1mol A气体和3mol
B气体,起始时A的浓度为$1\ mol\cdot L^{-1}$,5min内反应物A的物质的量由1mol降低到0.5mol,则A的浓度减少了$0.5\ mol\cdot L^{-1}$,则$v(A)=\frac{0.5\ mol\cdot L^{-1}}{5\ min}=0.1\ mol\cdot L^{-1}\cdot min^{-1}$。
B气体,起始时A的浓度为$1\ mol\cdot L^{-1}$,5min内反应物A的物质的量由1mol降低到0.5mol,则A的浓度减少了$0.5\ mol\cdot L^{-1}$,则$v(A)=\frac{0.5\ mol\cdot L^{-1}}{5\ min}=0.1\ mol\cdot L^{-1}\cdot min^{-1}$。
2. 将4mol A和2mol B在2L的密闭容器中混合,并在一定条件下发生如下反应:$2A(s)+B(g)\rightleftharpoons2C(g)$,反应2s后测得C的浓度为$0.6mol\cdot L^{-1}$。下列说法正确的是(
A.用物质A表示2s内的平均反应速率为$0.3mol\cdot L^{-1}\cdot s^{-1}$
B.用物质B表示2s内的平均反应速率为$0.6mol\cdot L^{-1}\cdot s^{-1}$
C.2s时$v(C)=0.3mol\cdot L^{-1}\cdot s^{-1}$
D.2s时物质B的浓度为$0.7mol\cdot L^{-1}$
D
)A.用物质A表示2s内的平均反应速率为$0.3mol\cdot L^{-1}\cdot s^{-1}$
B.用物质B表示2s内的平均反应速率为$0.6mol\cdot L^{-1}\cdot s^{-1}$
C.2s时$v(C)=0.3mol\cdot L^{-1}\cdot s^{-1}$
D.2s时物质B的浓度为$0.7mol\cdot L^{-1}$
答案:
2.D 解析:不能用固体物质的浓度表示化学反应速率,故A错误;据题目条件知$v(C)=\frac{0.6\ mol\cdot L^{-1}}{2\ s}=0.3\ mol\cdot L^{-1}\cdot s^{-1}$,则$v(B)=\frac{0.3\ mol\cdot L^{-1}\cdot s^{-1}}{2}=0.15\ mol\cdot L^{-1}\cdot s^{-1}$,故B错误;化学反应速率是平均值不是瞬时值,故C错误;2s时物质B的浓度为$\frac{2\ mol}{2\ L}-\frac{0.6\ mol\cdot L^{-1}}{2}=0.7\ mol\cdot L^{-1}$,故D正确。
3. 稀土是重要的战略资源,素有“工业味精”的美誉。CO和$NO_2$在氧化钕($Nd_2O_3$)等稀土催化剂的作用下可发生反应:$4CO+2NO_2\xlongequal{Nd_2O_3}N_2+4CO_2$,在不同条件下的化学反应速率如下,其中反应速率最大的是(
A.$v(CO)=0.05mol\cdot L^{-1}\cdot s^{-1}$
B.$v(NO_2)=0.7mol\cdot L^{-1}\cdot min^{-1}$
C.$v(N_2)=0.4mol\cdot L^{-1}\cdot min^{-1}$
D.$v(CO_2)=1.1mol\cdot L^{-1}\cdot min^{-1}$
A
)A.$v(CO)=0.05mol\cdot L^{-1}\cdot s^{-1}$
B.$v(NO_2)=0.7mol\cdot L^{-1}\cdot min^{-1}$
C.$v(N_2)=0.4mol\cdot L^{-1}\cdot min^{-1}$
D.$v(CO_2)=1.1mol\cdot L^{-1}\cdot min^{-1}$
答案:
3.A 解析:A项,$v(CO)=0.05\ mol\cdot L^{-1}\cdot s^{-1}$,则$v(N_2)=\frac{1}{4}×60\ s\cdot min^{-1}× v(CO)=0.75\ mol\cdot L^{-1}\cdot min^{-1}$;
B项,$v(NO_2)=0.7\ mol\cdot L^{-1}\cdot min^{-1}$,则$v(N_2)=\frac{1}{2}× v(NO_2)=0.35\ mol\cdot L^{-1}\cdot min^{-1}$;C项,$v(N_2)=0.4\ mol\cdot L^{-1}\cdot min^{-1}$;D项,$v(CO_2)=1.1\ mol\cdot L^{-1}\cdot min^{-1}$,则$v(N_2)=\frac{1}{4}× v(CO_2)=0.275\ mol\cdot L^{-1}\cdot min^{-1}$。故A项表示的反应速率最大。
B项,$v(NO_2)=0.7\ mol\cdot L^{-1}\cdot min^{-1}$,则$v(N_2)=\frac{1}{2}× v(NO_2)=0.35\ mol\cdot L^{-1}\cdot min^{-1}$;C项,$v(N_2)=0.4\ mol\cdot L^{-1}\cdot min^{-1}$;D项,$v(CO_2)=1.1\ mol\cdot L^{-1}\cdot min^{-1}$,则$v(N_2)=\frac{1}{4}× v(CO_2)=0.275\ mol\cdot L^{-1}\cdot min^{-1}$。故A项表示的反应速率最大。
4. 将等物质的量的A、B混合于2L的密闭容器中,发生如下反应:$3A(g)+B(g)\rightleftharpoons xC(g)+2D(g)$,5min后,测得D的浓度为$0.5mol\cdot L^{-1}$,$c(A):c(B)=3:5$,C的平均反应速率为$0.1mol\cdot L^{-1}\cdot min^{-1}$。
(1)此时A的浓度$c(A)=$
(2)B的平均反应速率:$v(B)=$____$mol\cdot L^{-1}\cdot min^{-1}$。
(3)x的值为
(1)此时A的浓度$c(A)=$
0.75
$mol\cdot L^{-1}$,反应开始前容器中A、B的物质的量:$n(A)=n(B)=$3
mol。(2)B的平均反应速率:$v(B)=$____$mol\cdot L^{-1}\cdot min^{-1}$。
(3)x的值为
2
。
答案:
4.
(1)0.75 3
(2)0.05
(3)2
(1)0.75 3
(2)0.05
(3)2
任务二 化学反应速率的影响因素
探究活动
活动1:工业生产硫酸时,要先将黄铁矿矿石(主要成分为$FeS_2$)粉碎后,再投入沸腾炉,为什么?
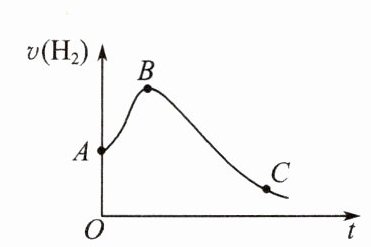
活动2:为了变废为宝,某同学利用废铁制取氢气。对于反应$Fe+H_2SO_4(稀)=FeSO_4+H_2↑$,改变某些条件会影响产生氢气的速率,$v(H_2)-t$图像中,为何AB段$v(H_2)$逐渐增大,BC段又逐渐减小?
探究活动
活动1:工业生产硫酸时,要先将黄铁矿矿石(主要成分为$FeS_2$)粉碎后,再投入沸腾炉,为什么?
活动2:为了变废为宝,某同学利用废铁制取氢气。对于反应$Fe+H_2SO_4(稀)=FeSO_4+H_2↑$,改变某些条件会影响产生氢气的速率,$v(H_2)-t$图像中,为何AB段$v(H_2)$逐渐增大,BC段又逐渐减小?

答案:
【探究活动】
1.提示:将黄铁矿粉碎是为了增大与空气的接触面积,增大反应速率。
2.提示:AB段$v(H_2)$逐渐增大,主要原因是反应放热,导致温度升高,反应速率逐渐增大;BC段$v(H_2)$逐渐减小,主要原因是随着反应的进行,溶液中$c(H^+)$减小,导致反应速率逐渐减小。
1.提示:将黄铁矿粉碎是为了增大与空气的接触面积,增大反应速率。
2.提示:AB段$v(H_2)$逐渐增大,主要原因是反应放热,导致温度升高,反应速率逐渐增大;BC段$v(H_2)$逐渐减小,主要原因是随着反应的进行,溶液中$c(H^+)$减小,导致反应速率逐渐减小。
查看更多完整答案,请扫码查看


