2025年阳光夺冠九年级化学下册
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年阳光夺冠九年级化学下册 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第13页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
1. 下列常见的金属矿石与相应的主要组分不正确的是 ( )
A. 赤铁矿(主要成分是Fe₂O₃)
B. 磁铁矿(主要成分是Fe₃O₄)
C. 铝土矿(主要成分是Al₂O₃)
D. 黄铜矿(主要成分是CuO)
A. 赤铁矿(主要成分是Fe₂O₃)
B. 磁铁矿(主要成分是Fe₃O₄)
C. 铝土矿(主要成分是Al₂O₃)
D. 黄铜矿(主要成分是CuO)
答案:
D
2. 早在春秋战国时期,我国就开始生产和使用铁器。铁矿石冶炼成铁是个复杂的过程,此过程不需要的物质是 ( )
A. 焦炭
B. 铁矿石
C. 生石灰
D. 石灰石
A. 焦炭
B. 铁矿石
C. 生石灰
D. 石灰石
答案:
C
3. 下列厨房用具,在空气中最易锈蚀的是 ( )
A. 铝壶
B. 铜盆
C. 不锈钢汤勺
D. 铁锅
A. 铝壶
B. 铜盆
C. 不锈钢汤勺
D. 铁锅
答案:
D
4. 下列措施有利于防止铁制品锈蚀的是 ( )
A. 家用剪刀不用时,涂上油并放在干燥处
B. 切过酸菜的菜刀不及时清洗
C. 工地上的钢管堆放在潮湿的地方
D. 农具上铁锈不及时除去
A. 家用剪刀不用时,涂上油并放在干燥处
B. 切过酸菜的菜刀不及时清洗
C. 工地上的钢管堆放在潮湿的地方
D. 农具上铁锈不及时除去
答案:
D
5. 菜刀在下列四种情况下放置,锈蚀由快到慢的顺序是 ( )
①切青菜后 ②切酸菜后 ③切青菜后擦干 ④切猪肉后用干布擦干再涂上一层豆油
A. ④③②①
B. ③②①④
C. ④③①②
D. ②①③④
①切青菜后 ②切酸菜后 ③切青菜后擦干 ④切猪肉后用干布擦干再涂上一层豆油
A. ④③②①
B. ③②①④
C. ④③①②
D. ②①③④
答案:
D
6. 下列关于金属材料的叙述错误的是 ( )
A. 回收利用废旧金属可减少对环境的污染
B. 在铁制品表面刷漆或镀耐腐蚀性金属都可以防止铁制品锈蚀
C. 铝块能制成铝箔是利用了铝的延展性
D. 铝比铁更容易跟氧气和其他物质反应,因而铝的抗腐蚀性能比铁差
A. 回收利用废旧金属可减少对环境的污染
B. 在铁制品表面刷漆或镀耐腐蚀性金属都可以防止铁制品锈蚀
C. 铝块能制成铝箔是利用了铝的延展性
D. 铝比铁更容易跟氧气和其他物质反应,因而铝的抗腐蚀性能比铁差
答案:
D
7.(怀化中考)港珠澳大桥的桥、岛、隧以及“雪龙2号”的船身等主要由金属材料制成。下列金属防护措施不正确的是 ( )
A. 在金属制品表面镀保护层
B. 改变金属结构制成合金使用
C. 在金属制品表面涂油漆
D. 用稀盐酸定期清洗金属制品
A. 在金属制品表面镀保护层
B. 改变金属结构制成合金使用
C. 在金属制品表面涂油漆
D. 用稀盐酸定期清洗金属制品
答案:
A
8. 金属材料在工农业生产、日常生活中应用广泛,下列说法错误的是 ( )
A. 铁制品锈蚀的过程实际上是铁与氧气发生的化学反应
B. 铝制品不易锈蚀的原因是铝与氧气作用在其表面形成致密的氧化物薄膜
C. 电池中含有铅、镍、镉、汞等金属,随意丢弃电池会造成污染
D. 合金的很多性能与组成它们的纯金属不同,合金具有更广泛的用途
A. 铁制品锈蚀的过程实际上是铁与氧气发生的化学反应
B. 铝制品不易锈蚀的原因是铝与氧气作用在其表面形成致密的氧化物薄膜
C. 电池中含有铅、镍、镉、汞等金属,随意丢弃电池会造成污染
D. 合金的很多性能与组成它们的纯金属不同,合金具有更广泛的用途
答案:
A
9. 为了节约成本,某汽车生产商采用价格相对便宜的普通钢板代替防腐性能较好的镀锌板,造成钢板生锈,给车主带来极大的安全隐患。以下实例采用的防锈措施与镀锌板不属于同一原理的是 ( )
A. 烤漆
B. 搪瓷
C. 涂油
D. 不锈钢
A. 烤漆
B. 搪瓷
C. 涂油
D. 不锈钢
答案:
D
10.(绥化中考)将一氧化碳和铁的氧化物FeₓOᵧ置于密闭容器中,一定条件下充分反应。反应过程中容器内部分物质的质量变化如图所示。下列说法正确的是 ( )
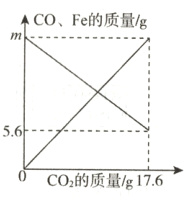
A. m的值为19.6
B. 参加反应的铁的氧化物的质量为16 g
C. 当CO₂质量为4.4 g时,容器内CO的质量为14 g
D. 铁的氧化物中x∶y=2∶3

A. m的值为19.6
B. 参加反应的铁的氧化物的质量为16 g
C. 当CO₂质量为4.4 g时,容器内CO的质量为14 g
D. 铁的氧化物中x∶y=2∶3
答案:
C
11.(日照中考)如图是探究铁钉锈蚀条件的4个实验,一段时间后观察现象。下列说法不正确的是 ( )
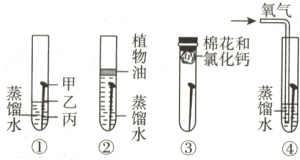
A. ①中甲、乙、丙三处比较,生锈最明显的地方是甲
B. ①②对比说明铁生锈需要空气,①③对比说明铁生锈需要水
C. ③中附着在棉花上的氯化钙的作用是作干燥剂
D. 四个实验中,生锈最快的是④中的铁钉

A. ①中甲、乙、丙三处比较,生锈最明显的地方是甲
B. ①②对比说明铁生锈需要空气,①③对比说明铁生锈需要水
C. ③中附着在棉花上的氯化钙的作用是作干燥剂
D. 四个实验中,生锈最快的是④中的铁钉
答案:
A
12. 用如图所示装置探究铜生锈的条件,一个月后发现铜丝未生锈。下列叙述错误的是 ( )
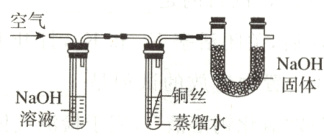
A. 金属的腐蚀是金属从单质变成化合物的过程
B. 在潮湿的空气中,铝比铁耐锈蚀
C. 在有氧气和水的条件下,铜比铁易生锈
D. 铜生锈可能与空气中的O₂、H₂O和CO₂有关

A. 金属的腐蚀是金属从单质变成化合物的过程
B. 在潮湿的空气中,铝比铁耐锈蚀
C. 在有氧气和水的条件下,铜比铁易生锈
D. 铜生锈可能与空气中的O₂、H₂O和CO₂有关
答案:
C
13. 炼铁厂以赤铁矿石、焦炭、石灰石、空气等为原料炼铁,主要反应过程如下图所示:
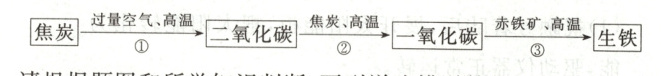
请根据题图和所学知识判断,下列说法错误的是 ( )
A. 生铁属于混合物
B. 炼铁过程中所有元素的化合价均发生了改变
C. 原料中焦炭的作用是提供能量和制取一氧化碳
D. 工业炼铁的设备是高炉

请根据题图和所学知识判断,下列说法错误的是 ( )
A. 生铁属于混合物
B. 炼铁过程中所有元素的化合价均发生了改变
C. 原料中焦炭的作用是提供能量和制取一氧化碳
D. 工业炼铁的设备是高炉
答案:
B
14.(深圳中考)下列说法错误的是 ( )
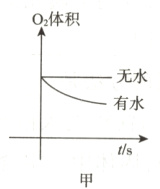
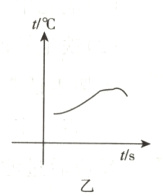
A. 铁钉是由铁合金制成的
B. 根据甲图,铁钉生锈过程中O₂体积不变
C. 根据甲图,铁钉在潮湿环境更容易生锈
D. 根据乙图,铁钉生锈过程中温度升高


A. 铁钉是由铁合金制成的
B. 根据甲图,铁钉生锈过程中O₂体积不变
C. 根据甲图,铁钉在潮湿环境更容易生锈
D. 根据乙图,铁钉生锈过程中温度升高
答案:
B
15. 如图所示是CO和Fe₂O₃反应的装置,下列关于图示实验的说法中正确的是 ( )
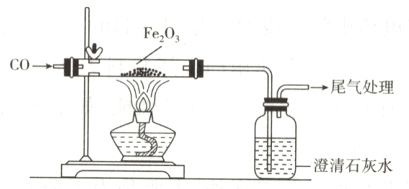
①说明Fe₂O₃具有氧化性 ②玻璃管中的红色粉末变成黑色粉末 ③玻璃管中的Fe₂O₃发生了还原反应 ④防止了CO对空气的污染 ⑤说明CO被还原的产物是CO₂
A. ①②④
B. ①②⑤
C. ①②③④
D. 全部

①说明Fe₂O₃具有氧化性 ②玻璃管中的红色粉末变成黑色粉末 ③玻璃管中的Fe₂O₃发生了还原反应 ④防止了CO对空气的污染 ⑤说明CO被还原的产物是CO₂
A. ①②④
B. ①②⑤
C. ①②③④
D. 全部
答案:
C
16.(2分)铁锅是生活中常用的炊具。在厨房中,防止铁锅生锈的方法是____________________;铁锅中的油着火后用锅盖盖灭的原理是____________________。
答案:
使用后擦洗干净 隔绝氧气
17.(2分)金属资源是有限的,因此要注意金属的回收利用。如回收______(填写一种具体用品),可以节约金属资源。另外,金属回收还可以减少对环境的污染,如回收废旧电池可防止__________(填金属名称)污染。
答案:
铝制易拉罐(合理即可) 汞
18.(3分)(贺州中考)2021年5月15日,中国首个火星探测器祝融号成功着陆火星,传回的图像在视觉上呈现为橘红色,是因为其地表广泛分布赤铁矿。
(1)祝融号着陆后,展开太阳能板,把太阳能转化为________能,驱动仪器正常运转。
(2)赤铁矿的主要成分是Fe₂O₃,工业上用赤铁矿炼铁的化学方程式为______________________________。
(3)每年因腐蚀而报废的金属数量惊人,请列举防止铁制品生锈的一条措施:______________________________。
(1)祝融号着陆后,展开太阳能板,把太阳能转化为________能,驱动仪器正常运转。
(2)赤铁矿的主要成分是Fe₂O₃,工业上用赤铁矿炼铁的化学方程式为______________________________。
(3)每年因腐蚀而报废的金属数量惊人,请列举防止铁制品生锈的一条措施:______________________________。
答案:
(1)电
(2)$Fe_{2}O_{3}+3CO\xlongequal{高温}2Fe + 3CO_{2}$
(3)刷漆等
(1)电
(2)$Fe_{2}O_{3}+3CO\xlongequal{高温}2Fe + 3CO_{2}$
(3)刷漆等
19.(5分)金属材料在生产生活中有着广泛的应用。
(1)地壳中含量最高的金属元素是________;
(2)铁生锈的条件是____________________,为了防止自行车的支架生锈常采用的方法是____________________;
(3)将一定质量的铁粉放入硝酸铜、硝酸锌的混合液中,充分反应后过滤,所得固体中一定含有的物质是______(用化学式表示),所得滤液中一定含有的溶质是____________________(用化学式表示)。
(1)地壳中含量最高的金属元素是________;
(2)铁生锈的条件是____________________,为了防止自行车的支架生锈常采用的方法是____________________;
(3)将一定质量的铁粉放入硝酸铜、硝酸锌的混合液中,充分反应后过滤,所得固体中一定含有的物质是______(用化学式表示),所得滤液中一定含有的溶质是____________________(用化学式表示)。
答案:
(1)铝元素
(2)与空气中的水和氧气同时接触 喷漆
(3)$Cu$ $Zn(NO_{3})_{2}$和$Fe(NO_{3})_{2}$
(1)铝元素
(2)与空气中的水和氧气同时接触 喷漆
(3)$Cu$ $Zn(NO_{3})_{2}$和$Fe(NO_{3})_{2}$
20.(4分)遍布全国的高速铁路,使人们的出行将更加方便、快捷。结合所学化学知识,回答下列问题:
(1)动车电路中的导线大多是用铜制的,这是利用了铜的延展性和________,动车使用的金属材料大多是合金而不是纯金属,这是因为合金具有更多优良性能,如钢比纯铁硬度______(填“大”或“小”)。
(2)动车表面喷漆除美观外,主要是为了防止外壳生锈,其防锈的原理是______________________________。
(3)铝的活泼性比铁强,但常温下,铝却具有较好的抗腐蚀性能。这是因为______________________________。
(1)动车电路中的导线大多是用铜制的,这是利用了铜的延展性和________,动车使用的金属材料大多是合金而不是纯金属,这是因为合金具有更多优良性能,如钢比纯铁硬度______(填“大”或“小”)。
(2)动车表面喷漆除美观外,主要是为了防止外壳生锈,其防锈的原理是______________________________。
(3)铝的活泼性比铁强,但常温下,铝却具有较好的抗腐蚀性能。这是因为______________________________。
答案:
(1)导电性大
(2)隔绝氧气和水
(3)铝在常温下易被氧化,其表面生成一层致密的氧化物薄膜,阻止铝进一步被氧化
(1)导电性大
(2)隔绝氧气和水
(3)铝在常温下易被氧化,其表面生成一层致密的氧化物薄膜,阻止铝进一步被氧化
21.(6分)铁是生产、生活中广泛应用的金属材料。
(1)铁锅作炊具主要是利用铁具有良好的________性。
(2)为减缓海水对铁质海轮外壳的腐蚀,制造海轮时,会在海轮船底四周镶嵌比铁更活泼的金属。下列金属适宜镶嵌在铁质船底的是________(填标号)。
A. Pb(铅) B. Cu C. Pt(铂) D. Zn
(3)对铁“发蓝”处理,使其表面形成致密氧化膜而有效避免腐蚀。
①致密氧化膜能有效阻止铁锈蚀的主要原因是______________________________。
②为检验“发蓝”处理的铁质零件表面是否形成致密氧化膜,将该零件浸泡于硫酸铜溶液中,发现零件表面出现红色物质。由此判断该零件“发蓝”处理效果________(填“好”或“不好”),理由是____________________(用化学方程式表示)。
(1)铁锅作炊具主要是利用铁具有良好的________性。
(2)为减缓海水对铁质海轮外壳的腐蚀,制造海轮时,会在海轮船底四周镶嵌比铁更活泼的金属。下列金属适宜镶嵌在铁质船底的是________(填标号)。
A. Pb(铅) B. Cu C. Pt(铂) D. Zn
(3)对铁“发蓝”处理,使其表面形成致密氧化膜而有效避免腐蚀。
①致密氧化膜能有效阻止铁锈蚀的主要原因是______________________________。
②为检验“发蓝”处理的铁质零件表面是否形成致密氧化膜,将该零件浸泡于硫酸铜溶液中,发现零件表面出现红色物质。由此判断该零件“发蓝”处理效果________(填“好”或“不好”),理由是____________________(用化学方程式表示)。
答案:
(1)导热
(2)D
(3)①隔绝水和氧气 ②不好 $Fe + CuSO_{4}=FeSO_{4}+Cu$
(1)导热
(2)D
(3)①隔绝水和氧气 ②不好 $Fe + CuSO_{4}=FeSO_{4}+Cu$
22.(9分)早在春秋战国时期,我国就开始生产和使用铁器。
(1)写出用CO和赤铁矿(主要成分Fe₂O₃)为原料炼铁的化学方程式______________________________。盛水的铁锅与水面接触的一圈最易生锈,钢铁生锈的条件是____________________。利用新技术能将不锈钢加工成柔软的金属丝,这是利用了不锈钢的________(填字母)。
A. 耐腐蚀性 B. 延展性 C. 导热性 D. 导电性
(2)设计从废水中回收硫酸亚铁固体和铜的实验方案如下图:

金属X是________,写出上述实验方案中有关反应的化学方程式:
①______________________________,②______________________________。
(1)写出用CO和赤铁矿(主要成分Fe₂O₃)为原料炼铁的化学方程式______________________________。盛水的铁锅与水面接触的一圈最易生锈,钢铁生锈的条件是____________________。利用新技术能将不锈钢加工成柔软的金属丝,这是利用了不锈钢的________(填字母)。
A. 耐腐蚀性 B. 延展性 C. 导热性 D. 导电性
(2)设计从废水中回收硫酸亚铁固体和铜的实验方案如下图:

金属X是________,写出上述实验方案中有关反应的化学方程式:
①______________________________,②______________________________。
答案:
(1)$3CO + Fe_{2}O_{3}\xlongequal{高温}2Fe + 3CO_{2}$ 与水和氧气同时接触 B
(2)$Fe$ $Fe + CuSO_{4}=Cu + FeSO_{4}$ $Fe + H_{2}SO_{4}=FeSO_{4}+H_{2}\uparrow$
(1)$3CO + Fe_{2}O_{3}\xlongequal{高温}2Fe + 3CO_{2}$ 与水和氧气同时接触 B
(2)$Fe$ $Fe + CuSO_{4}=Cu + FeSO_{4}$ $Fe + H_{2}SO_{4}=FeSO_{4}+H_{2}\uparrow$
23.(14分)(四川中考)工业上可用焦炭与赤铁矿冶炼铁。实验室用如图所示装置模拟冶炼铁并探究其产物。回答下列问题:

(1)酒精喷灯加热前,先打开活塞K₁和K₂,关闭K₃,将气囊中的N₂鼓入。通N₂的目的是______________________________。
(2)通适量N₂后,关闭活塞K₁和K₂,打开K₃,点燃酒精喷灯进行实验。B装置中盛放的试剂是________________(填“稀硫酸”“澄清石灰水”或“氯化钙溶液”),用于检测气体产物之一______(填化学式)。
(3)装置C的作用是________________。
(4)当A装置药品完全变黑后,停止实验。移走酒精喷灯停止加热前的操作是________________。
(5)用简单的化学方法证明已经冶炼出铁。取少量黑色产物于试管中,滴加________(填“稀硫酸”“澄清石灰水”或“硫酸镁溶液”),观察到________________,说明铁已生成。

(1)酒精喷灯加热前,先打开活塞K₁和K₂,关闭K₃,将气囊中的N₂鼓入。通N₂的目的是______________________________。
(2)通适量N₂后,关闭活塞K₁和K₂,打开K₃,点燃酒精喷灯进行实验。B装置中盛放的试剂是________________(填“稀硫酸”“澄清石灰水”或“氯化钙溶液”),用于检测气体产物之一______(填化学式)。
(3)装置C的作用是________________。
(4)当A装置药品完全变黑后,停止实验。移走酒精喷灯停止加热前的操作是________________。
(5)用简单的化学方法证明已经冶炼出铁。取少量黑色产物于试管中,滴加________(填“稀硫酸”“澄清石灰水”或“硫酸镁溶液”),观察到________________,说明铁已生成。
答案:
(1)排净装置内的空气
(2)澄清石灰水 $CO_{2}$
(3)收集一氧化碳气体
(4)先把$K_{3}$关闭
(5)稀硫酸 有无色气体产生
(1)排净装置内的空气
(2)澄清石灰水 $CO_{2}$
(3)收集一氧化碳气体
(4)先把$K_{3}$关闭
(5)稀硫酸 有无色气体产生
24.(6分)小嘉发现学校草地周围都做上了新的铁栅栏,师傅们在上面涂油漆。铁栅栏上为什么要涂油漆呢?某兴趣小组为此进行研究:
【方案】取四支试管编号为①、②、③、④,分别作如图处理,两周后,观察铁钉表面的锈蚀情况。

【分析】
(1)设置①③两支试管对照,基于的猜想是______________________________。
(2)若两周后观察到①中铁钉生锈而④中铁钉未生锈,据此可得出:导致铁钉生锈的因素为______________________________。
(3)若得出食盐会加速金属锈蚀,则实验中支持该结论的证据是______________________________。
【方案】取四支试管编号为①、②、③、④,分别作如图处理,两周后,观察铁钉表面的锈蚀情况。

【分析】
(1)设置①③两支试管对照,基于的猜想是______________________________。
(2)若两周后观察到①中铁钉生锈而④中铁钉未生锈,据此可得出:导致铁钉生锈的因素为______________________________。
(3)若得出食盐会加速金属锈蚀,则实验中支持该结论的证据是______________________________。
答案:
(1)铁钉生锈可能与氧气有关
(2)水分
(3)试管②中铁钉生锈的速度比①中的快
(1)铁钉生锈可能与氧气有关
(2)水分
(3)试管②中铁钉生锈的速度比①中的快
四、计算题(共4分)
25.(4分)(眉山中考)磁铁矿石(主要成分为Fe₃O₄)是常用的炼铁原料,工业上可通过如下反应:Fe₃O₄ + 4CO $\stackrel{高温}{=\!=\!=}$ 3Fe + 4CO₂将其中的Fe₃O₄转化为Fe。
(1)Fe₃O₄中铁、氧的微观粒子数目之比为______。
(2)假设炼铁过程中铁没有损耗,用含348吨Fe₃O₄的磁铁矿石理论上可以炼出含铁96%的生铁的质量是多少?(写出计算过程)
25.(4分)(眉山中考)磁铁矿石(主要成分为Fe₃O₄)是常用的炼铁原料,工业上可通过如下反应:Fe₃O₄ + 4CO $\stackrel{高温}{=\!=\!=}$ 3Fe + 4CO₂将其中的Fe₃O₄转化为Fe。
(1)Fe₃O₄中铁、氧的微观粒子数目之比为______。
(2)假设炼铁过程中铁没有损耗,用含348吨Fe₃O₄的磁铁矿石理论上可以炼出含铁96%的生铁的质量是多少?(写出计算过程)
答案:
(1)$3:4$
(2)解:设理论上可以炼出含铁96%的生铁的质量为$x$。
$Fe_{3}O_{4}+4CO\xlongequal{高温}3Fe + 4CO_{2}$
232 168
348t $96\%×x$
$\frac{232}{168}=\frac{348t}{96\%×x}$ 解得:$x = 262.5t$
答:理论上可以炼出含铁96%的生铁的质量为262.5t。
(1)$3:4$
(2)解:设理论上可以炼出含铁96%的生铁的质量为$x$。
$Fe_{3}O_{4}+4CO\xlongequal{高温}3Fe + 4CO_{2}$
232 168
348t $96\%×x$
$\frac{232}{168}=\frac{348t}{96\%×x}$ 解得:$x = 262.5t$
答:理论上可以炼出含铁96%的生铁的质量为262.5t。
1. 下列生活用品中,用金属材料制作的是 ( )
A. 瓷器
B. 铁罐
C. 玻璃瓶
D. 塑料杯
A. 瓷器
B. 铁罐
C. 玻璃瓶
D. 塑料杯
答案:
B
2. 金属不具有的物理通性是 ( )
A. 银白色光泽
B. 导热性
C. 延展性
D. 导电性
A. 银白色光泽
B. 导热性
C. 延展性
D. 导电性
答案:
A
3. 龙岩市研发出7μm超薄铜箔,该项技术全国领先。铜能加工成铜箔是利用铜的 ( )
A. 导电性
B. 延展性
C. 可燃性
D. 抗腐蚀性
A. 导电性
B. 延展性
C. 可燃性
D. 抗腐蚀性
答案:
B
4. 下列措施不利于保护金属资源的是 ( )
A. 过度开采金属矿物
B. 回收废旧金属
C. 寻找金属代用品
D. 防止金属被腐蚀
A. 过度开采金属矿物
B. 回收废旧金属
C. 寻找金属代用品
D. 防止金属被腐蚀
答案:
A
5. 修建地铁广泛使用金属材料,下列不属于合金的是 ( )
A. 锰钢
B. 生铁
C. 硬铝
D. 金刚石
A. 锰钢
B. 生铁
C. 硬铝
D. 金刚石
答案:
D
6. 有等质量的A、B两种金属,相对原子质量$A_{r}(A)\lt A_{r}(B)$。将A放入质量分数为15%的稀硫酸中,B放入质量分数为15%的稀盐酸中,在反应中A、B均显正二价,产生氢气的质量随时间变化曲线如右图所示。下列说法正确的是 ( )
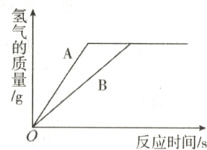
A. 产生氢气的速率A<B
B. 反应后,A、B一定都有剩余
C. 消耗的稀硫酸和稀盐酸质量一定不相等
D. 消耗B的质量一定小于消耗A的质量

A. 产生氢气的速率A<B
B. 反应后,A、B一定都有剩余
C. 消耗的稀硫酸和稀盐酸质量一定不相等
D. 消耗B的质量一定小于消耗A的质量
答案:
C
7. 下列指定反应的化学方程式正确的是 ( )
A. “湿法炼铜”:$2Fe + 3CuSO_{4}=Fe_{2}(SO_{4})_{3}+3Cu$
B. 铜置换银:$Cu + 2AgCl=CuCl_{2}+2Ag$
C. 铁的冶炼:$CO + Fe_{2}O_{3}\stackrel{高温}{=\!=\!=}Fe + CO_{2}$
D. 铝的“自我保护”:$4Al + 3O_{2}=2Al_{2}O_{3}$
A. “湿法炼铜”:$2Fe + 3CuSO_{4}=Fe_{2}(SO_{4})_{3}+3Cu$
B. 铜置换银:$Cu + 2AgCl=CuCl_{2}+2Ag$
C. 铁的冶炼:$CO + Fe_{2}O_{3}\stackrel{高温}{=\!=\!=}Fe + CO_{2}$
D. 铝的“自我保护”:$4Al + 3O_{2}=2Al_{2}O_{3}$
答案:
D
查看更多完整答案,请扫码查看


