第92页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
3. (2024安徽15题)碳酸锂(Li₂CO₃)是制备新能源汽车电池的重要原料。我国盐湖卤水中主要含有氯化锂、氯化钠、硫酸镁等溶质,一种以化学沉淀法从卤水中生产碳酸锂的工艺如图:
 ₃
₃
(1)步骤①发生反应的化学方程式为____________________。
(2)步骤②操作a的名称是______。
(3)步骤③中加入草酸钠,其中草酸根(C₂O₄²⁻)的化合价是 - 2价,则草酸钠的化学式为__________。
(4)滤液2中含有LiCl,步骤④中生成Li₂CO₃的反应类型是____________。
(5)该工艺中用到的氧化物有________________(写1种即可)。
 ₃
₃(1)步骤①发生反应的化学方程式为____________________。
(2)步骤②操作a的名称是______。
(3)步骤③中加入草酸钠,其中草酸根(C₂O₄²⁻)的化合价是 - 2价,则草酸钠的化学式为__________。
(4)滤液2中含有LiCl,步骤④中生成Li₂CO₃的反应类型是____________。
(5)该工艺中用到的氧化物有________________(写1种即可)。
答案:
(1)CaO + H₂O === Ca(OH)₂
(2)过滤
(3)Na₂C₂O₄
(4)复分解反应
(5)CaO(或H₂O)
(1)CaO + H₂O === Ca(OH)₂
(2)过滤
(3)Na₂C₂O₄
(4)复分解反应
(5)CaO(或H₂O)
4. (2023安徽15题)活性氧化铜用于印刷电路板制造,由普通氧化铜制备活性氧化铜的工艺流程如下。

(1)步骤①发生反应的化学方程式是____________________。
(2)下列说法正确的是______(填字母序号)。
A. 过滤时用玻璃棒在漏斗中不断搅拌
B. 步骤②溶液中的水参加了反应
C. Cu₂(OH)₂CO₃易溶于水
D. Na₂CO₃的俗名是纯碱
(3)步骤②加入Na₂CO₃溶液时有气泡产生,原因是____________________。
(4)步骤③发生反应的反应类型是__________。

(1)步骤①发生反应的化学方程式是____________________。
(2)下列说法正确的是______(填字母序号)。
A. 过滤时用玻璃棒在漏斗中不断搅拌
B. 步骤②溶液中的水参加了反应
C. Cu₂(OH)₂CO₃易溶于水
D. Na₂CO₃的俗名是纯碱
(3)步骤②加入Na₂CO₃溶液时有气泡产生,原因是____________________。
(4)步骤③发生反应的反应类型是__________。
答案:
(1)CuO + 2HCl === CuCl₂ + H₂O
(2)BD
(3)碳酸钠与过量的盐酸反应生成了二氧化碳气体
(4)分解反应
(1)CuO + 2HCl === CuCl₂ + H₂O
(2)BD
(3)碳酸钠与过量的盐酸反应生成了二氧化碳气体
(4)分解反应
5. (2024合肥经开区二模)碳酸亚铁(FeCO₃)可用于制作补铁药物,如图是用硫铁矿烧渣(主要成分为Fe₂O₃、SiO₂等)为原料制备碳酸亚铁的生产流程示意图。
资料:已知40℃以上时,(NH₄)₂CO₃易分解。

(1)(NH₄)₂CO₃属于______(填“酸”“碱”或“盐”)
(2)步骤①中发生反应的化学方程式是____________________。
(3)下列说法正确的是______(填字母序号)。
A. 步骤③的温度要控制在40℃以下
B. FeCO₃溶于水
C. 固体A是纯净物
D. 过滤时滤纸没有贴紧漏斗内壁,会影响过滤速度
(4)步骤③发生化学反应的基本反应类型是____________________。
资料:已知40℃以上时,(NH₄)₂CO₃易分解。

(1)(NH₄)₂CO₃属于______(填“酸”“碱”或“盐”)
(2)步骤①中发生反应的化学方程式是____________________。
(3)下列说法正确的是______(填字母序号)。
A. 步骤③的温度要控制在40℃以下
B. FeCO₃溶于水
C. 固体A是纯净物
D. 过滤时滤纸没有贴紧漏斗内壁,会影响过滤速度
(4)步骤③发生化学反应的基本反应类型是____________________。
答案:
(1)盐
(2)Fe₂O₃ + 3CO$\stackrel{高温}{=\!=\!=}$2Fe + 3CO₂
(3)AD
(4)复分解反应
(1)盐
(2)Fe₂O₃ + 3CO$\stackrel{高温}{=\!=\!=}$2Fe + 3CO₂
(3)AD
(4)复分解反应
6. (2024牡丹江)兴趣小组的同学们了解到Fe₂O₃是绘画颜料的成分之一,在老师的指导下,进行了从食品脱氧剂的废渣中提取氧化铁为项目主题的实践活动,并创作出“红梅图”作为项目成果进行展示。请结合如下实验流程回答问题。
温馨提示:①该食品脱氧剂废渣中含有Fe、Fe₂O₃、NaCl和炭粉。
②控制溶液pH,可使Fe(OH)₃完全沉淀。

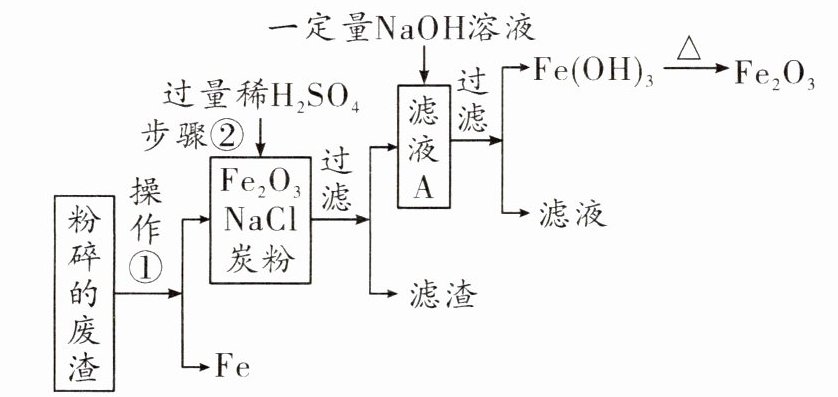
(1)操作①中分离出铁粉的方法是____________________。
(2)步骤②中发生反应的化学方程式为____________________。
(3)滤液A中溶质的成分是____________________(填化学式)。
(4)生产生活中常利用废料提取所需物质的意义是____________________。
温馨提示:①该食品脱氧剂废渣中含有Fe、Fe₂O₃、NaCl和炭粉。
②控制溶液pH,可使Fe(OH)₃完全沉淀。


(1)操作①中分离出铁粉的方法是____________________。
(2)步骤②中发生反应的化学方程式为____________________。
(3)滤液A中溶质的成分是____________________(填化学式)。
(4)生产生活中常利用废料提取所需物质的意义是____________________。
答案:
(1)用磁铁吸引
(2)Fe₂O₃ + 3H₂SO₄ === Fe₂(SO₄)₃ + 3H₂O
(3)Fe₂(SO₄)₃、H₂SO₄、NaCl
(4)废物利用(合理即可)
(1)用磁铁吸引
(2)Fe₂O₃ + 3H₂SO₄ === Fe₂(SO₄)₃ + 3H₂O
(3)Fe₂(SO₄)₃、H₂SO₄、NaCl
(4)废物利用(合理即可)
查看更多完整答案,请扫码查看


