第13页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
例(2019安徽改编)某兴趣小组研究发现:氯酸钾(KClO₃)分别与二氧化锰、氧化铁和氯化钾混合加热,也能很快产生氧气。同学们对KClO₃分解反应的催化剂进行研究,在相同的加热条件下,用如图装置完成表中实验。
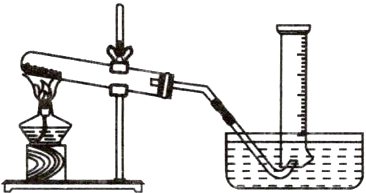
技巧点拨:
(1)明确探究问题:研究KClO₃分解反应的催化剂
(2)寻找影响因素:催化剂种类、催化剂质量、温度等
(3)判断方法
①定性判断:观察产生气泡的速率
②定量判断:做对比实验
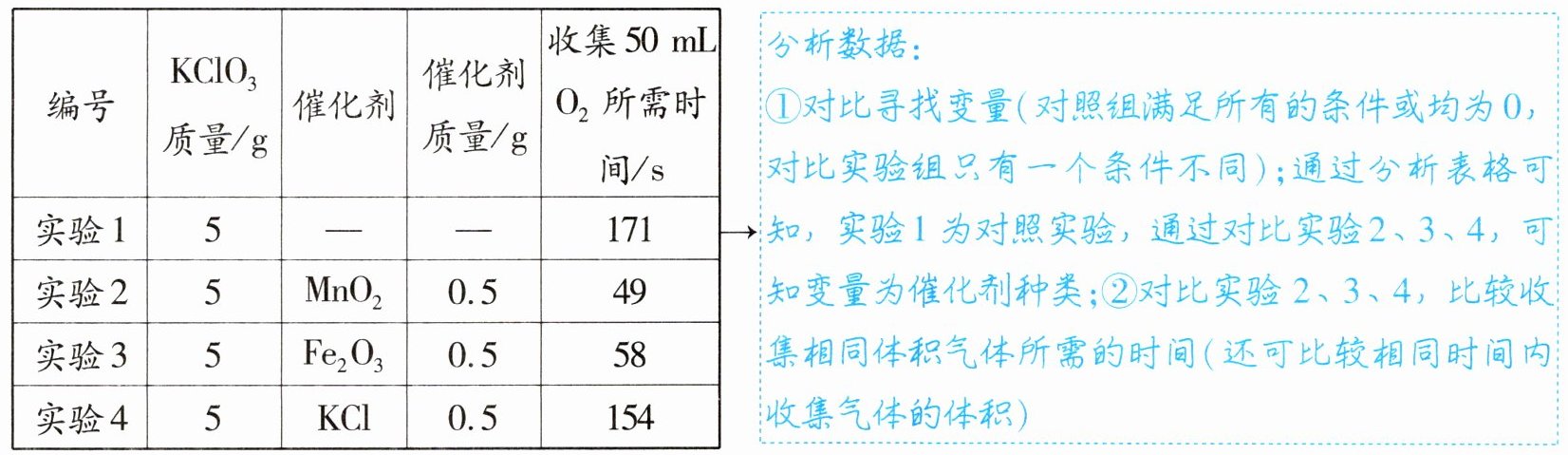
(1)设置实验1的目的是____________。
(2)表中所列3种催化剂的催化效果最佳的是________。
(3)KClO₃分解生成氯化钾和氧气,反应的化学方程式是______________________________。
(4)由实验1和实验4可知,KCl______(填“有”或“无”)催化作用。维持加热条件不变,用实验1再继续收集50 mL O₂,所需时间明显少于171 s,解释原因:______________________________。
(5)要比较KClO₃分解反应中不同催化剂的催化效果,除了测量收集50 mL O₂所需时间外,还可以测量相同时间内______________________。

技巧点拨:
(1)明确探究问题:研究KClO₃分解反应的催化剂
(2)寻找影响因素:催化剂种类、催化剂质量、温度等
(3)判断方法
①定性判断:观察产生气泡的速率
②定量判断:做对比实验

(1)设置实验1的目的是____________。
(2)表中所列3种催化剂的催化效果最佳的是________。
(3)KClO₃分解生成氯化钾和氧气,反应的化学方程式是______________________________。
(4)由实验1和实验4可知,KCl______(填“有”或“无”)催化作用。维持加热条件不变,用实验1再继续收集50 mL O₂,所需时间明显少于171 s,解释原因:______________________________。
(5)要比较KClO₃分解反应中不同催化剂的催化效果,除了测量收集50 mL O₂所需时间外,还可以测量相同时间内______________________。
答案:
(1)作对照实验
(2)$MnO_{2}$
(3)$2KClO_{3}\xlongequal[\triangle]{MnO_{2}}2KCl + 3O_{2}\uparrow$(或$2KClO_{3}\xlongequal[\triangle]{Fe_{2}O_{3}}2KCl + 3O_{2}\uparrow$或$2KClO_{3}\xlongequal[\triangle]{KCl}2KCl + 3O_{2}\uparrow$或$2KClO_{3}\xlongequal[\triangle]{催化剂}2KCl + 3O_{2}\uparrow$)
(4)有 随着反应的进行,生成的$KCl$越来越多,$KCl$对该反应有催化作用,使反应速率加快(合理即可)
(5)收集氧气的体积(合理即可)
(1)作对照实验
(2)$MnO_{2}$
(3)$2KClO_{3}\xlongequal[\triangle]{MnO_{2}}2KCl + 3O_{2}\uparrow$(或$2KClO_{3}\xlongequal[\triangle]{Fe_{2}O_{3}}2KCl + 3O_{2}\uparrow$或$2KClO_{3}\xlongequal[\triangle]{KCl}2KCl + 3O_{2}\uparrow$或$2KClO_{3}\xlongequal[\triangle]{催化剂}2KCl + 3O_{2}\uparrow$)
(4)有 随着反应的进行,生成的$KCl$越来越多,$KCl$对该反应有催化作用,使反应速率加快(合理即可)
(5)收集氧气的体积(合理即可)
1. 某校化学兴趣小组在老师的指导下,对过氧化氢溶液分解制取氧气进行再探究。
【提出问题】小组同学通过查阅资料得知,氯化铜溶液也可作为过氧化氢溶液分解的催化剂,氯化铜溶液中含有H₂O、Cu²⁺、Cl⁻,到底哪种粒子对过氧化氢溶液的分解起催化作用呢?
【作出猜想】猜想一:可能是H₂O。
猜想二:可能是________。
猜想三:可能是Cl⁻。
【分析交流】猜想一肯定是错误的,因为______________________________。
【实验探究】为了进一步验证猜想,小组同学设计了如下表实验:
|实验操作|实验现象|
|----|----|
|其他条件不变,向过氧化氢溶液中加入NaCl溶液|无明显变化|
|其他条件不变,向过氧化氢溶液中加入Na₂SO₄溶液|无明显变化|
|其他条件不变,向过氧化氢溶液中加入______(填化学式)溶液|立即产生大量气泡|
【结论反思】猜想______成立。
【拓展应用】与课本中二氧化锰相比,从循环利用的角度分析,__________(填“二氧化锰”或“氯化铜溶液”)更适合作该反应的催化剂。
【深入探究】小组同学查阅了不同金属离子对过氧化氢分解影响的实验资料得知,100 ℃时,在不同金属离子存在下,过氧化氢24 h的分解率如下表所示。

【交流反思】实验①的目的是__________,通过以上探究可得出的结论:______________________________(写一点即可)。
【提出问题】小组同学通过查阅资料得知,氯化铜溶液也可作为过氧化氢溶液分解的催化剂,氯化铜溶液中含有H₂O、Cu²⁺、Cl⁻,到底哪种粒子对过氧化氢溶液的分解起催化作用呢?
【作出猜想】猜想一:可能是H₂O。
猜想二:可能是________。
猜想三:可能是Cl⁻。
【分析交流】猜想一肯定是错误的,因为______________________________。
【实验探究】为了进一步验证猜想,小组同学设计了如下表实验:
|实验操作|实验现象|
|----|----|
|其他条件不变,向过氧化氢溶液中加入NaCl溶液|无明显变化|
|其他条件不变,向过氧化氢溶液中加入Na₂SO₄溶液|无明显变化|
|其他条件不变,向过氧化氢溶液中加入______(填化学式)溶液|立即产生大量气泡|
【结论反思】猜想______成立。
【拓展应用】与课本中二氧化锰相比,从循环利用的角度分析,__________(填“二氧化锰”或“氯化铜溶液”)更适合作该反应的催化剂。
【深入探究】小组同学查阅了不同金属离子对过氧化氢分解影响的实验资料得知,100 ℃时,在不同金属离子存在下,过氧化氢24 h的分解率如下表所示。

【交流反思】实验①的目的是__________,通过以上探究可得出的结论:______________________________(写一点即可)。
答案:
【作出猜想】$Cu^{2+}$ 【分析交流】过氧化氢溶液中含有$H_{2}O$ 【实验探究】$CuCl_{2}$ 【结论反思】二 【拓展应用】二氧化锰 【交流反思】作对照实验 $Al^{3+}$不能加快过氧化氢的分解速率(合理即可)
查看更多完整答案,请扫码查看


