第86页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
1[2025安徽合肥质检]三氧化二碳的化学性质与一氧化碳相似。下列关于三氧化二碳的说法中,不正确的是(
$A.C_2O_3$不能使澄清石灰水变浑浊
$B.C_2O_3$中碳元素的化合价为+2
$C.C_2O_3$在一定条件下能还原氧化铜
$D.C_2O_3$在$O_2$中充分燃烧的产物为$CO_2$
B
)$A.C_2O_3$不能使澄清石灰水变浑浊
$B.C_2O_3$中碳元素的化合价为+2
$C.C_2O_3$在一定条件下能还原氧化铜
$D.C_2O_3$在$O_2$中充分燃烧的产物为$CO_2$
答案:
B
如图为CO还原CuO的一体化装置,打开立式防风打火机,对准木炭加热3min,气球逐渐变大;再将立式防风打火机火焰对准表面烧黑的铜片加热2min左右(已知:CO能使湿润的氯化钯试纸变为蓝色)。下列相关说法正确的是(
A.气球逐渐变大的原因只是试管内气体受热膨胀
B.观察到湿润的氯化钯试纸变为蓝色,一段时间后再将立式防风打火机火焰对准铜片
C.表面烧黑的铜片加热后逐渐变为红色的反应属于分解反应
D.实验结束处理尾气时可将气球内的气体通入氢氧化钙溶液
B
)A.气球逐渐变大的原因只是试管内气体受热膨胀
B.观察到湿润的氯化钯试纸变为蓝色,一段时间后再将立式防风打火机火焰对准铜片
C.表面烧黑的铜片加热后逐渐变为红色的反应属于分解反应
D.实验结束处理尾气时可将气球内的气体通入氢氧化钙溶液
答案:
B
3[2025河南周口质检,中]CO和$CO_2$的混合气体ag,通入足量的$Ca(OH)_2$溶液中,充分反应后过滤、洗涤、干燥,称量沉淀质量为ag,则混合气体中CO与$CO_2$的分子个数比为(
A.1:2
B.2:1
C.11:14
D.14:11
B
)A.1:2
B.2:1
C.11:14
D.14:11
答案:
B
4[2024云南昆明模拟,中]a、b、c、d是初中化学常见的4种物质,它们之间的转化关系如图所示(“→”表示物质间的转化关系),已知a和d均为单质,b和c都是氧化物且组成元素相同,常温下b、c、d都是气体,自然界中可实现c和d的相互转化。下列说法不正确的是(
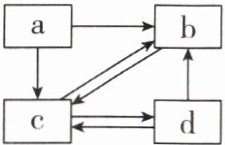
A.b是造成“煤气中毒”的主要原因
B.d的化学性质活泼,能供给呼吸
C.a→c可用化学方程式表示为$C+O_2\xlongequal{点燃}CO_2$
D.要实现b→c只有一种反应途径
D
)
A.b是造成“煤气中毒”的主要原因
B.d的化学性质活泼,能供给呼吸
C.a→c可用化学方程式表示为$C+O_2\xlongequal{点燃}CO_2$
D.要实现b→c只有一种反应途径
答案:
D
(1)装置中气球的作用是
(2)实验时利用一氧化碳还原4g氧化铜,理论上能得到铜的质量是多少?(写出具体的计算过程)
(3)为确定反应的最佳温度,兴趣小组利用原位X射线粉末衍射仪来测定不同温度下反应4小时后的固体物质成分,实验结果如图乙所示,据图回答下列问题。
①300℃时,反应的固体产物中含有Cu和
②用CO还原CuO制备Cu,最佳反应温度应控制在500℃,不选其他温度的理由是
③取纯净的CuO32g放在玻璃管中,控制温度,最终得到固体只有Cu和$Cu_2O($总质量27.2g),其中得到Cu的质量是
收集尾气,防止污染空气
。(2)实验时利用一氧化碳还原4g氧化铜,理论上能得到铜的质量是多少?(写出具体的计算过程)
解:设理论上得到铜的质量为x。CO+CuO$\stackrel{\triangle}{=}$Cu+CO₂80 644 g x$\frac{80}{64}$=$\frac{4\ \text{g}}{x}$x=$\frac{64×4\ \text{g}}{80}$=3.2 g答:理论上得到铜的质量为3.2 g。
(3)为确定反应的最佳温度,兴趣小组利用原位X射线粉末衍射仪来测定不同温度下反应4小时后的固体物质成分,实验结果如图乙所示,据图回答下列问题。
①300℃时,反应的固体产物中含有Cu和
Cu₂O
。②用CO还原CuO制备Cu,最佳反应温度应控制在500℃,不选其他温度的理由是
不会产生其他杂质,不会剩余CuO,节约能源
。③取纯净的CuO32g放在玻璃管中,控制温度,最终得到固体只有Cu和$Cu_2O($总质量27.2g),其中得到Cu的质量是
12.8
g。
答案:
(1)收集尾气,防止污染空气
(2)解:设理论上得到铜的质量为x。CO+CuO$\stackrel{\triangle}{=}$Cu+CO₂80 644 g x$\frac{80}{64}$=$\frac{4\ \text{g}}{x}$x=$\frac{64×4\ \text{g}}{80}$=3.2 g答:理论上得到铜的质量为3.2 g。
(3)①Cu₂O ②不会产生其他杂质,不会剩余CuO,节约能源 ③12.8
(1)收集尾气,防止污染空气
(2)解:设理论上得到铜的质量为x。CO+CuO$\stackrel{\triangle}{=}$Cu+CO₂80 644 g x$\frac{80}{64}$=$\frac{4\ \text{g}}{x}$x=$\frac{64×4\ \text{g}}{80}$=3.2 g答:理论上得到铜的质量为3.2 g。
(3)①Cu₂O ②不会产生其他杂质,不会剩余CuO,节约能源 ③12.8
查看更多完整答案,请扫码查看


